
题目列表(包括答案和解析)
3.理解浓度、压强和温度等条件对化学平衡的影响,理解平衡移动原理的涵义。
2.了解化学反应的可逆性,理解化学平衡的特征,了解化学平衡与化学反应速率之间的内在联系。
1.了解化学反应速率的概念及表示方法,理解浓度、压强、温度和催化剂等条件对化学反应速率的影响。
26. 3.2g Cu与过量硝酸(a mol·L-1,30mL)充分反应。硝酸的还原产物只有NO2、NO。反应后溶液中含H+为0.1mol。
(1)此时溶液中所含NO3-为 mol。
(2)求生成的气体中NO2和NO的物质的量(用含有a的式子表示)。
(3)用NaOH溶液吸收产生的气体,原理为:2NO2+2NaOH==NaNO3+NaNO2+H2O,
NO2+NO+2NaOH==2NaNO2+H2O。若生成的混合气体能被NaOH完全吸收,试讨论a的取值范围。
25. 将a g H2和b g Cl2充分混合后,点燃使其充分反应。然后将反应后的混合气用足量的氢氧化钠溶液吸收。
⑴写出可能发生的反应的化学方程式:。
⑵若H2和Cl2恰好充分反应,只生成HCl,则生成NaCl的物质的量为 ,或 。
⑶若H2过量,则剩余气体质量为 ,生成NaCl的物质的量为 。
⑷若Cl2过量,则生成NaCl的物质的量为 。
24.(8分)由磷酸形成的磷脂及其化合物(如酶)是细胞的重要组成部分,它们对调节生命活动起了积极作用。假如缺少了磷,氮就是再少也不会被植物吸收。磷酸吡醛素(结构式为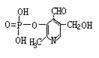 )能有效地促进植物对氮肥的吸收。 试回答:
)能有效地促进植物对氮肥的吸收。 试回答:
⑴磷酸吡醛素的分子式是 。
此物质具有的性质是(填序号) 。
A.能与金属钠反应 B能发生银镜反应
C.能与FeCl3溶液反应 D能使石蕊试液变红
⑵写出磷酸吡醛素与足量氢氧化钠溶液反应的化学方程式: 。
23. (本题8分)
(1)用间苯二甲酰氯(A)与间苯二胺(B)经缩聚反应可制得HT纤维,写出HT纤维的结构简式:

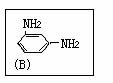

(2)阿司匹林问世已有100多年,是驰名的治感冒、头痛、发烧、风湿和缓解、治疗其他疼痛的畅销药物。英国药学家约翰·文博士及其同事们由于发现其作用机理而获得1982年诺贝尔奖。现代医学证明,它在防治心脑血管疾病方面,特别是抑制手术后血栓、心肌梗塞和抑制血小板凝聚有效,成为医学界常用药物。
①写出用水杨酸 ( 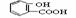 ) 与乙酸酐(
) 与乙酸酐(
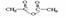 )合成
)合成
阿司匹林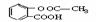 的化学方程式。
;
的化学方程式。
;
②已知A、B二种芳香族化合物均为阿司匹林的同分异构体,写出其结构简式。
A、水解后得到一种二元酸和一种醇 ;
B、水解后得到一种二元酚和两种酸 。
22.(14分) 某无色溶液,其中有可能存在的离子如下:Na+、Ag+、Ba2+、Al3+、AlO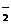 、S2-、CO
、S2-、CO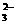 、SO
、SO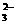 、SO
、SO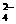 ,现取该溶液进行有关实验,实验结果如下图所示:
,现取该溶液进行有关实验,实验结果如下图所示:

试回答下列问题:
(1) 沉淀甲是____________,
(2) 沉淀乙是__________,
(3) 由溶液甲生成沉淀乙的离子方程式为:_________________________。
(4) 气体甲成分可能有哪几种?(可以不填满也可以补充,多填要扣分)
|
1 |
2 |
3 |
4 |
5 |
6 |
|
|
|
|
|
|
|
(5)综合上述信息,可以肯定存在的离子:_____________________________。
21.(12分)碳的稳定氧化物除CO、CO2外,还有C3O2、C4O3 C12O9等低氧化物,其中C3O2是一种在常温下有恶臭的气体,其分子中的每个原子都满足最外层8电子结构。
⑴C3O2的电子式为 ,分子空间构型为 。⑵在上述碳的低氧化物中,若有分子构型与C3O2相同的,可能是 。⑶不考虑反应条件,根据你现有的化学知识判断,在O2、H2O、NH3、HCl中,哪些能与发生反应,请写出能够发生反应的化学方程式 。
20.(11分)用右图的实验装置可以进行钠与水的反应实验,并可收集、检验生成的气体。钠的密度为0.9 g·cm-3,煤油的密度为0.87 g·cm-3。请回答下列问题:
⑴液体物质添加完毕后,关闭活栓,打开右边胶塞,向煤油中加入一小块钠,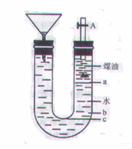 立即塞好胶塞。反应开始前钠的位置在 处(填a、b、c);
立即塞好胶塞。反应开始前钠的位置在 处(填a、b、c);
⑵反应后,钠在煤油层和水层界面之间上下跳动,反应平缓连续进行。试说明产生上述现象的原因 。 ⑶写出钠跟水反应的离子方程式 ;
⑷装置中的漏斗在反应过程中的主要作用是 ;⑸本实验除能使反应平缓连续进行、收集并检验气体外,还有一个优点是 。这是因为 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com