

题目列表(包括答案和解析)
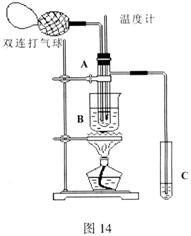
20.乙醛在催化剂存在的条件下,可以被空气氧化成乙酸。依据此原理设计实验制得并在试管C中收集到少量乙酸溶液(如图所示:试管A中装有40%的乙醛水溶液、氧化铜粉末;试管C中装有适量蒸馏水;烧杯B中装有某液体)。已知在60℃~80℃时用双连打气球鼓入空气即可发生乙醛的氧化反应,连续鼓入十几次反应基本完全。有关物质的沸点见下:
|
物质 |
乙醛 |
乙酸 |
甘油 |
乙二醇 |
水 |
|
沸点 |
20.8℃ |
117.9℃ |
290℃ |
197.2℃ |
100℃ |
 请回答下列问题:
请回答下列问题:
(1) 试管A内在60℃~80℃时发生的主要反
应化学方程式为(注明反应条件):
__________________________________
(2)在实验的不同阶段,需要调整________
(填仪器的名称)的位置;
(3)烧杯B内盛装的液体可以是__________
(写出一种即可);
(4)若想检验试管C中是否含有产物乙酸,请
你在所提供的药品中进行选择,设计一个
简便的实验方案。所提供的药物有:pH试
纸、红色的石蕊试纸、白色的醋酸铅试纸、
碳酸氢钠粉末(实验仪器任选)。该方案为______________________________。
(5)久置的乙醛水溶液会产生分层现象,上层为无色油状液体,下层为水溶液。据测定,上层物质为乙醛的环状聚合物(C2H4O)n,它的沸点比水的沸点高,分子中无醛基。当n=3时,试写出(C2H4O)n的结构简式________________。
19.氯化亚砜(SOCl2)是一种无色液体,沸点79℃,重要有机试剂,用于将ROH转化为RCl。氯化亚砜遇水水解(水解前后元素化合价无变化),需在无水条件下使用。
(1)试写出它与水完全反应的化学方程式:________________________________;
(2)设计一些简单的实验来验证你写的化学方程式是正确的。(只需给出实验原理,无须描叙实验仪器和操作。)__________________________________________
___________________________________________________________________
(3)实验室制取无水氯化锌是将ZnCl2·xH2O与SOCl2混合加热的方法。试回答:SOCl2的作用______________________________________________________。
18.两种有机物以一定比例混合,在一定条件下在aLO2(足量)中燃烧,充分反应后恢复到原状态,再通过足量Na2O2层,得到气体仍为aL,下列混合物符合此条件的是 ( )
A.CH4 C2H4 B.CH3OH CH3COOH
C.C2H6 HCHO D.HCOOH CH3COOCH3
第Ⅱ卷(非选择题 共78分)
17.6.4gCu跟足量的浓硫酸共热,充分反应后,下列说法错误的是 ( )
A.有0.2molH2SO4被还原 B.有0.1molH2SO4被还原
C.有2.24LSO2气体生成 D.有0.2molH2SO4发生反应
16.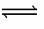 某二元酸(化学式用H2Y表示)在水中电离的方程式是:
某二元酸(化学式用H2Y表示)在水中电离的方程式是:
H2Y=H++HY- HY- H++Y2-
下列有关该酸的酸式盐NaHY水溶液的叙述中正确的是 ( )
A.若0.1mol·L-1NaHY溶液的Ph=2,则0.1mol·L-1H2Y溶液中氢离子的物质的量浓度小于0.1mol·L-1
B.在该盐的溶液中,离子浓度为:C(Na+)>C(Y2-)>C(HY-)>C(OH-)>C(H+)
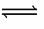 C.在该盐的溶液中,离子浓度为:C(Na+)> C(HY-)> C(H+)
>C(OH-)
C.在该盐的溶液中,离子浓度为:C(Na+)> C(HY-)> C(H+)
>C(OH-)
D.HY-水解方程式为:HY-+H2O H2Y+OH-
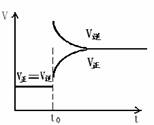
15.往一体积不变的密闭容器中充入H2和I2,发生反应H2(g)+I2(g)===2HI(g);△H<0,当达到平衡后,t0时改变反应的某一条件(混合气体总物质的量不变),且造成容器内压强增大,下列说法正确的是 ( )
 A.容器内气体颜色变深,平均相对分子质量不变
A.容器内气体颜色变深,平均相对分子质量不变
B.平衡不移动,混合气体密度增大
C.H2转化率增大,HI平衡浓度变小
D.改变条件前后,速度图象为(如右图)
14.下列各组中,两种气体的分子数一定相等的是 ( )
A.温度相同、体积相同的O2和N2 B.质量相等、密度不等的N2和C2H4
C.体积相等、密度相等的CO和C2H4 D.压力相同、体积相同的N2和O2
13.可以将反应Zn+Br2=ZnBr2设计成蓄电池,下列4个电极反应
①Br2+2e-=2Br- ②2Br- -2e-= Br2 ③Zn-2e-=Zn2+ ④Zn2+ +2e-=Zn-
其中表示充电时阳极反应和放电时的负极反应的分别是 ( )
A.②和③ B.②和① C.③和① D.④和①
12.下列各项实验操作中,正确的是 ( )
A.为使制取H2的速率加快,可向H2SO4中加少量CuSO4溶液
B.为加快过滤速度,可用玻璃棒搅拌过滤器中的食盐水
C.为迅速除去乙酸乙酯中的少量乙酸,可加入足量NaOH溶液并加热
D.为除去试管内壁上的“银镜”,可用氨水洗涤
11.下列反应的离子方程式正确的是 ( )
A.氯气溶于水:Cl2+H2O====H++HClO
B.金属铝溶于氢氧化钠溶液:Al+2OH-===AlO2-+H2↑
 C.苯酚钠溶液中通入少量二氧化碳:2C6H5O-+CO2===2C6H5OH+CO32-
C.苯酚钠溶液中通入少量二氧化碳:2C6H5O-+CO2===2C6H5OH+CO32-
D.实验室制备氢氧化铁胶体:Fe3++3H2O Fe(OH)3(胶体)+3H+
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com