
题目列表(包括答案和解析)
28.工业生产的纯碱中常含有少量的NaCl等杂质,图所示实验装置是用来测定纯碱 中Na2CO3质量分数的实验方法示意力。其操作步骤如下:
①检验装置的气密性;
②在球形干燥管内填入颗粒状碱石灰,共总质量为W1;
③称取一定量的纯碱样品,其质量为W2,将其放入装置(B)中;
④将分液漏斗中的稀H2SO4缓缓注入B中,直至不再产生气体为止;
⑤打开开关a,缓缓鼓入空气约5min后,又称得干燥管的总质为W3。
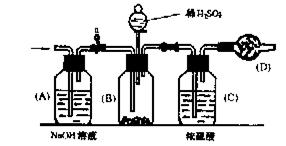
请回答下列问题:
(1)实验中鼓入空气的目的是_________________________________________________;
(2)装置(A)的作用是______________________________________________________;装置(C)的作用是________________________________________________________;
(3)Na2CO3的质量分数为_______________________。
27.称取mgNa2CO3,恰好与20mL盐酸全部反应生成CO2、H2O和NaCl。
(1)这种盐酸的物质的量浓度为_________________________________。
(2)如果上述mgNa2CO3中混有K2CO3,那么这种盐酸的实际浓度比(1)测得的值_________(填“偏大”、“偏小”、“相同”,下同);
(3)如果上述mgNa2CO3中混有NaOH,那么这种盐酸的实际浓度比(1)测得的值_______;
(4)如果上述mgNa2CO3中混有NaHCO3,那么这种盐酸的实际浓度比(1)测得的值________。
26.某无色混合气体可能含有CO2COH2O(气)H2中的一种或几种,依次进行下列处理(假设每次处理的反应完全):①通过碱石灰、气体体积变小。②通过赤热的氧化铜时,固体全部变为红色。③通过白色硫酸铜粉末时,粉末变为蓝色。④通过澄清石灰水,溶液变浑浊。由此可以确定混合气体中( )
A.一定含有CO、H2O,可能含有H2、CO中的一种或两种
B.一定含有CO、H2O,可能含有CO2、H2中的一种或两种。
C.一定含有CO和H2,可能含有H2O、CO2中的一种或两种
D.一定含有CO,可能含有H2O、H2中的一种或两种
25.把xmolCO2通入含ymolCa(OH)2的石灰水中,充分反应后,下列叙述不正确的是( )
A.当x≤y时,生成100xg沉淀 B.当x≥y时,生成100yg沉淀
C.当y<x<2y时,生成100(2y-x)g沉淀
D.当2y≤x时,无沉淀生成
24.根据硅在元素周期表中的位置推测,下列不可能具有的性质是( )
A.单质在通常状况下是固体
B.硅具有导电性 C.SiH4(硅烷)比CH4稳定
D.硅的常见化合价是+4
23.把7.4gNa2CO3·10H2O和NaHCO3组成的混合物溶于水,配成100mL溶液,其中[Na+]=0.6mol·L-1,若把等质量的混合物加热至恒重时,残留物质的质量是( )
A.5.28g B.4.22g C.3.18g D.2.12g
22.某K2CO3样品中含有Na2CO3、KNO3和Ba(NO3)2三种杂质中的一种或两种。现将13.8g样品中加放足量水,样品全部溶解。再加入过量的CaCl2溶液,得到9g沉淀。对样品所含杂质的正确判断是( )
A.肯定有KNO3,肯定没有Na2CO3
B.肯定有KNO3,可能还含有Na2CO3
C.肯定没有Ba(NO3)2,一定有KNO3和Na2CO3
D.肯定没有Na2CO3和Ba(NO3)2
21.将一小块焦炭和mg氧气,同时放入装有压力表的密闭容器中,压力为P0,当在一定条件下充分反应后恢复到原湿度,压力为P1,且P0<P1<2P0,则加入的焦炭的质量W为( )
A.W≤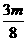 B.W≤
B.W≤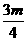
C.W>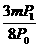 D.W=
D.W=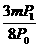
20.对于碳酸氢钠与碳酸钠的性质,下列叙述错误的是( )
A.质量相同时,跟足量的盐酸反应相同条件下碳酸钠的产生的CO2体积多
B.物质的量相同时,跟盐酸完全反应碳酸钠消耗的盐酸是碳酸氢钠的2倍(盐酸浓度相同)
C.物质的量相同时,跟足量盐酸反应,在相同状况下,得到等体积的CO2
D.将它们分别加入澄清石灰水中都会产生白色沉淀
19.该厂家不采用石英与焦炭直接制高纯硅的主要原因是( )
A.产量太低 B.产品中含SiC
C.产品中含有过量的硅石和焦炭 D.耗能太大
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com