
题目列表(包括答案和解析)
3.下列各物质中所含原子个数由大小的顺序正确的是 ( )
①0.5mol氨气;②标准状况下22.4L氦气;③4℃时9mL水;④0.2mol磷酸
A.①④③② B.④③②① C.②③④① D.①④②③
2.下列各组物理量中,都不随取水量的变化而变化的是 ( )
A.水的沸点;蒸发水所需热量
D.水的密度;水中通入足量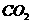 后溶液的pH值
后溶液的pH值
C.水的体积;电解水所消耗的电量
D.水的物质的量;水的摩尔质量
1.摩尔是 ( )
A.国际单位制的一个基本物理量 B.表示物质质量的单位
C.计量微观粒子的物质的量的单位 D.表示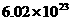 个粒子的集体
个粒子的集体
24.(10分)某液态卤代烷RX(R是烷基,X是某种卤素原子)的密度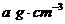 。该RX可以跟稀碱发生水解反应生成ROH(能跟水互溶)和HX。为了测定RX的相对分子质量,拟定的实验步骤如下:
。该RX可以跟稀碱发生水解反应生成ROH(能跟水互溶)和HX。为了测定RX的相对分子质量,拟定的实验步骤如下:
①准确量取该卤代烷b mL,放入锥形瓶中。
②在锥形瓶中加入过量稀NaOH溶液,塞上带有长玻璃管的塞子,加热,发生反应。
③反应完成后,冷却溶液,加稀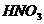 酸化,滴加过量
酸化,滴加过量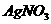 溶液得到白色沉淀。
溶液得到白色沉淀。
④过滤、洗涤、干燥后称重,得到固体c g。
回答下面问题:
(1)装置中长玻璃管的作用是_______________________________________。
(2)步骤④中,洗涤的目的是为了除去沉淀上吸附的________________离子。
(3)该卤代烷中所含卤素的名称是______________,判断的依据是___________________。
(4)该卤代烷的相对分子质量是______________________________________(列出算式)。
(5)如果在步骤③中,加入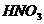 的量不足,没有将溶液酸化,则步骤④中所得的c值(填下列选项代码)______________。
的量不足,没有将溶液酸化,则步骤④中所得的c值(填下列选项代码)______________。
A.偏大 B.偏小 C.不变 D.大小不定
23.(9分)某无色溶液中可能含有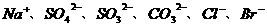 这几种离子中的若干种,依次进行下列实验,观察到的现象如下:
这几种离子中的若干种,依次进行下列实验,观察到的现象如下:
①用pH试纸检验,溶液的pH>7;②向溶液中滴加氯水无气体产生,再加入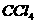 振荡、静置,
振荡、静置,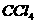 层呈橙色,用分液漏斗分液;③向分液后所得的水溶液中加入
层呈橙色,用分液漏斗分液;③向分液后所得的水溶液中加入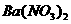 和
和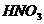 的混合溶液,只有白色沉淀产生,过滤;④在滤液中加入
的混合溶液,只有白色沉淀产生,过滤;④在滤液中加入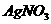 和
和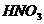 的混合溶液,有白色沉淀产生。
的混合溶液,有白色沉淀产生。
试回答下列问题:
(1)原溶液中肯定有的离子是_________________,肯定没有的离子是__________________;
(2)分液漏斗的上层液体如何转移到烧杯中?
___________________________________________________________________;
(3)若步骤③改用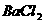 和盐酸的混合溶液,对判断①结论有无影响?
和盐酸的混合溶液,对判断①结论有无影响?
___________________________________________________________________;
(4)写出步骤②发生的有关反应的离子方程式_________________________________________________________________________。
22.(12分)如图19-4所示转化关系中,A-L均是中学化学中常见的物质。其中D为金属单质,B在常温常压下为无色液体;G为不溶于水但可溶于酸的白色固体;I为无色气体且能使湿润的红色石蕊试纸变蓝;L为无色气体,遇空气变为红棕色。
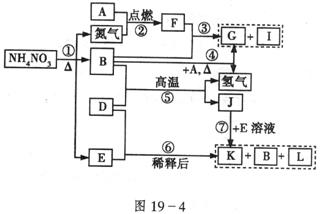
请回答:
(1)构成单质D的元素在周期表中处于____________周期,____________族。
(2)I物质的电子式为_____________,F物质的化学式为____________;它们的晶体类型分别为_______________,_____________。
(3)写出下列反应的化学方程式
③_________________________________________________;
⑤_________________________________________________。
(4)在反应⑤中如果有2mol J物质生成,则反应中转移的电子为_________________mol。
21.(10分)实验室里有如下仪器和药品,请设计如下实验的操作步骤要点(“○”可不填满),并指出可能发生的实验现象。
仪器或用品:①试管 ②烧杯 ③玻璃片 ④石棉网 ⑤滤纸
⑥火柴 ⑦镊子 ⑧酒精灯 ⑨药匙 ⑩集气瓶
药品:①金属钠(在煤油中)
② 溶液 ③蒸馏水 ④细沙
溶液 ③蒸馏水 ④细沙
|
|
操作步骤要点 |
仪器代号 |
实验现象 |
|
钠与氯化铝溶液反应 |
① |
|
① |
|
② |
② |
||
|
○ |
○ |
||
|
○ |
○ |
||
|
○ |
○ |
||
|
○ |
○ |
20.(13分)如图19-3装配好装置,待内外空气压强不变时标注出水银液面的刻度(用红漆)。取下橡皮塞,在玻璃燃烧匙中加入硫粉,用酒粉灯点燃迅速移入锥形瓶中并塞紧橡皮塞。硫粉安静地燃烧,水银柱推向左管。当火焰熄灭后,静置,水银柱又慢慢回到原先标定的刻度。
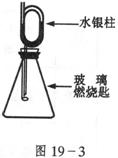
简要回答下列问题:
(1)水银柱推向左管说明什么?___________________________________________
______________________________________;
(2)硫粉未燃尽时火焰就熄灭了,说明_____________________________________
______________________________________;
(3)根据水银柱最后又回到原先标定的刻度,可得到什么结论?
__________________________________________________________________;
(4)根据反应方程式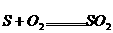 和上述结论又可推导出什么(或证明什么?)
和上述结论又可推导出什么(或证明什么?)
_____________________________________________________________________。
19.(15分)用下面两种方法可以制得白色的 沉淀。
沉淀。
方法一:用不含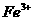 的
的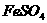 溶液与用不含
溶液与用不含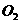 的蒸馏水配制的NaOH溶液反应制备。
的蒸馏水配制的NaOH溶液反应制备。
(1)用硫酸亚铁晶体配制上述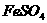 溶液时还需加入___________________________。
溶液时还需加入___________________________。
(2)除去蒸馏水中溶解的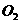 常采用______________________的方法。
常采用______________________的方法。
(3)生成白色 沉淀的操作是用长滴管吸取不含
沉淀的操作是用长滴管吸取不含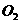 的NaOH溶液,插入
的NaOH溶液,插入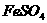 溶液液面上,再挤出NaOH溶液。这样操作的理由是________________________。
溶液液面上,再挤出NaOH溶液。这样操作的理由是________________________。
方法二:在如图19-2装置中,用NaOH溶液、铁、屑、稀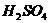 等试剂制备。
等试剂制备。
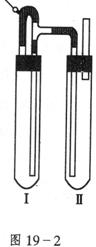
(1)在试管Ⅰ里加入的试剂是__________________________。
(2)在试管Ⅱ里加入的试剂是____________________________。
(3)为了制得白色 沉淀,在试管Ⅰ和Ⅱ中加入试剂,打开止水夹,塞紧塞子后的实验步骤是________________________。
沉淀,在试管Ⅰ和Ⅱ中加入试剂,打开止水夹,塞紧塞子后的实验步骤是________________________。
(4)这样生成的 沉淀能较长时间保持白色,其理由是______________________。
沉淀能较长时间保持白色,其理由是______________________。
18.(6分)下列各种容器,通常应分别用什么方法清洗?
(1)做过碘升华实验的烧杯__________________________________________;
(2)长期存放过三氯化铁溶液的试剂瓶______________________________________
_______________________________________________;
(3)盛过苯酚的容器________________________________________________________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com