
题目列表(包括答案和解析)
21.(6分) 为了在铝制品表面形成一层较厚的氧化膜,可将铝制品与另一种材料作电极,以某溶液作电解液进行电解,通电后在铝制品与电解液的接触面上逐渐形成一层Al(OH)3薄膜,薄膜的某些部位存在着小孔,电流从小孔通过并产生热量使Al(OH)3分解即可。某研究性学习小组根据上述原理,以铝制品和铁棒为电极,某浓度的NaHCO3溶液为电解液进行实验。
⑴铝制品应该与电源的 极相连接。
⑵电解过程中,必须使电解液的pH保持相对稳定(不能太大,也不能太小)的原因是
。
⑶使用NaHCO3溶液为电解液,会减缓阴极区溶液pH值的增大,能说明该反应的离子方程式为________________________________________________________。
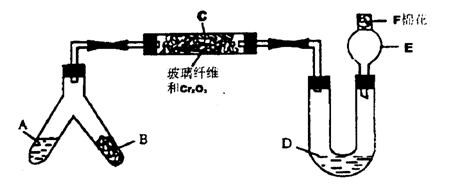
20.(13分)下图是某同学设计的NH3催化氧化并检验反应生成的酸性物质的简易装置(图中必要的铁架台、铁夹、酒精灯等均已略去)。已知:NO2+NO+2NaOH=2NaNO2+H2O。
 实验中所选用的试剂不超出下列范围,且不得重复使用。
实验中所选用的试剂不超出下列范围,且不得重复使用。
①NH4Cl和Ca(OH)2的混合物;②浓氨水;③NaOH固体;④KClO3和MnO2的混合物;⑤6mol/LNaOH溶液;⑥0.5mol/LNaOH溶液;⑦酚酞试液;⑧碱石灰;⑨浓H2SO4;⑩CuO。
试回答下列问题:
(1)图中液态物质A是(填代号) ,固体物质B是(填代号) ;
(2)C处发生的NH3催化氧化的化学方程式是
_____________________________________________________________;
(3)混合物D是为了检验酸性物质的生成而放入的,其组成是(填代号)________________,实验过程中的现象是______________________________________;
(4)E处球形玻璃管的作用是____________________________________________________;
F处的棉花应蘸取的物质是(填代号)______________,其作用是____________________
19.(9分)下列实验操作正确的是(选错扣分) 。
A.实验室制取乙烯时,必须将温度计的水银球插入反应液中。
B.分离苯和苯酚的混合液,可加入适量浓溴水,过滤、分液,即可实现。
C.取2mL 2mol/L CuSO4溶液于试管中,加入几滴 4mol/L NaOH溶液,再加入某种有机试剂,加热,可根据是否产生大量的红色沉淀判断该有机物中是否含有醛基。
D.向一支洁净的试管中加入2mL 2%硝酸银溶液,再向试管中滴加稀氨水至产生的沉淀恰好溶解为止,加入几滴乙醛溶液,水浴加热。片刻后,在试管内壁形成银镜。
E.取20mL蒸馏水于50mL烧杯中,加热至沸腾,加入数滴饱和FeCl3溶液,持续加热片刻,即可制得Fe(OH)3胶体。
F.用浓硫酸作催化剂将纤维素水解后,加入新制的氢氧化铜悬浊液,加热,可根据是否产生红色沉淀判断该水解液是否含有醛基。
18.足量的铝分别与等物质的量浓度的氢氧化钠溶液、稀硫酸反应,放出的气体体积在标准状况下相等,则所取氢氧化钠溶液和稀硫酸的体积比为
A.1:1 B.1:2 C.1:3 D.2:3
第II卷(非选择题,共78分)
17.科学家成功地在高压下将CO2转化为具有类似SiO2结构的原子晶体,下列关于CO2原子晶体的说法正确的是
A.CO2原子晶体和分子晶体互为同素异形体
B.在一定条件下,CO2原子晶体转化为分子晶体是物理变化
C.CO2原子晶体和CO2分子晶体具有相同的物理性质
D.在CO2原子晶体中,每一个碳原子周围结合4个氧原子,每一个氧原子跟两个碳原子相结合
16.制取硝酸铜现有三种设计方案可供选用:
①Cu与稀硝酸反应 3Cu+8HNO3=3Cu(NO) 2+2NO↑+4H2O
②Cu与浓硝酸反应 Cu+4HNO3=Cu(NO3)2+2NO2↑+2H2O
③通氧气于铜屑与稀硝酸的体系中 2Cu+4HNO3+O2=2Cu(NO3)2+2H2O
下列说法正确的是
A.制取相同量的硝酸铜时,③需硝酸的量最少
B.制取相同量的硝酸铜时,①产生的有毒气体比②少
C.三种方案中硝酸的利用率③>②>①
D.三种方案的反应都可以在铁制容器中进行
15.增大压强,对已达到平衡的反应
3X(g)+Y(g)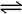 2Z(g)+2Q(g) 产生的影响是
2Z(g)+2Q(g) 产生的影响是
A.正反应速率增大,逆反应速率减小,平衡向正反应方向移动
B.正反应速率减小,逆反应速率增大,平衡向逆反应方向移动
C.正、逆反应速率都没有变化,平衡不发生移动
D.正、逆反应速率都增大,平衡不发生移动
14. L-多巴是一种有机物,它可用于帕金森综合症的治疗,其结构简式如下:
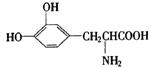
下列关于L-多巴性质的推测正确的是
A.不易被氧化 B.能与溴发生取代反应
C.有酸性,也有碱性 D.不可能形成高分子化合物
13.下列离子方程式书写正确的是
A.氯化铵溶液中加入氢氧化钠稀溶液 NH4++OH-====NH3·H2O
|
C.二氧化锰与浓盐酸混合加热 MnO2+4HCl===== Mn2++2Cl-+Cl2↑+2H2O
D.过量的碳酸氢钠溶液与氢氧化钡溶液混合 HCO3-+Ba2++OH-===H2O+BaCO3↓
12.在一定温度下,可逆反应A(g)+3B(g)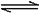 2C(g)达到平衡的标志是
2C(g)达到平衡的标志是
A.A的生成速率与C的生成速率相等 B.A、B、C的浓度不再变化
C.单位时间内生成A,同时生成3B D.A、B、C的分子数之比为1:2:3
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com