
题目列表(包括答案和解析)
5.用0.01mol·L-1NaOH溶液完全中和pH=3的下列溶液各100mL。需NaOH溶液的体积最大的是( )
A 盐酸 B 硫酸 C 高氯酸 D 醋酸
4.下列各组物质的性质比较,从强到弱的顺序正确的是( )
A 单质熔点:Li>Na>K>Mg>Al B 酸性:HClO4>H2SO4>H3PO4 >H2SiO3
C 稳定性:AsH3>PH3>NH3 D 沸点:HI>HBr >HCl>HF
3.下列实验中,仪器的下端必须插入液面下的是( )
①制备氢气的简易装置中的长颈漏斗; ②制备氯气装置中的分液漏斗;
③制备Fe(OH)2操作中的胶头滴管; ④将氯化氢气体溶于水时的导管
⑤用乙醇制取乙烯时的温度计; ⑥分馏石油时的温度计
A ①③⑤ B ②④⑥ C ①③④⑤ D 全部
2.13C-NMR(核磁共振)、15N-NMR可用于测定蛋白质、核酸等生物大分子的空间结构,KurtW ü thrich等人为此获得2002年诺贝尔化学奖。下面有关13C、15N叙述正确的是( )
A 13C与15N有相同的中子数 B 13C与C60互为同素异形体
C 15N与14N互为同位素 D 15N的核外电子数与中子数相同
1.将如下卤化物跟浓H2SO4放在烧瓶中共热,可以得到纯净卤化氢气体的是( )
A NaF B NaCl C NaBr D NaI
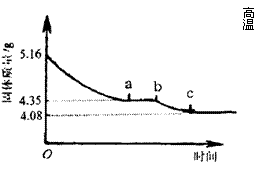
26.(12分)某化学研究性学习小组在研究某结晶水合物(MSO4·2H2O)的过程中,做了如下实验:将含结晶水合物放在坩埚中加热,加热前和加热后都进行称量。随着实验次数的增加,加热的时间不断延长,他们在实验中将数据整理如下表。
|
实验顺序(按延长加热时间) |
固体质量/g |
|
|
加热前(g) |
 加热后(g) 加热后(g) |
|
|
1 |
5.16 |
4.89 |
|
2 |
4.68 |
|
|
3 |
4.35 |
|
|
4 |
4.35 |
|
|
5 |
4.20 |
|
|
6 |
4.17 |
|
|
7 |
4.08 |
|
|
8 |
4.08 |
(注:在上述实验温度下,MSO4不分解)
利用数据可绘制成如右图所示的图像:
(1) 利用实验数据,通过计算确定M元素的相对原子质量,并写出其元素符号。
⑵ 求ab段坩埚中固体物质的化学式。
高考备考统测题
25.(8分)6.4gCu与过量硝酸(a mol / L,30mL)充分反应。硝酸的还原产物只有NO2、NO。反应后溶液中含H+为0.1mol。
⑴此时溶液中所含NO3-为 mol。
⑵求生成的气体中NO2和NO的物质的量(用含有a的式子表示)。
24.(10分)卤代烃R-C1在一定条件下可发生如下反应:
|
|||
 |
|||
 R-C1 + H2O
ROH+HCl R-C1 +
KCN
R-CN +
KCl
R-C1 + H2O
ROH+HCl R-C1 +
KCN
R-CN +
KCl
R-CN + 2H2O
+ H+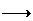 R-COOH + NH
R-COOH + NH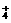
以乙烯为原料经过下图所示的反应可制取有机物W(A、B、C、D、E均为烃的衍生物) 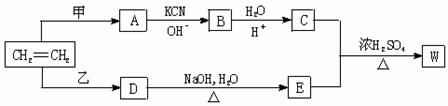
⑴若甲为Cl2 ,乙为HCl ,生成物W的分子式为C8H14O4 ,则W的结构简式为
____________________________________________________________。
⑵若甲、乙均为C12,生成的W为最小环状分子,写出C + E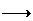 W的化学方程式
W的化学方程式
。
⑶若甲、乙均为C12,生成的W为高分子,则W的结构简式为
。
⑷若W的分子式为C5H10O3则甲为________________,乙为__________。
23.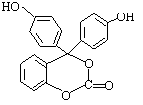 (8分)右下图为某有机物的结构简式,每个节点处代表有一个碳原子,与其结合的氢原子的元素符号省略,这种化学式称为“键线式”。又知酯类在铜铬氧化物催化下,与氢气反应得到醇,羰基双键可同时被还原,但苯环在
(8分)右下图为某有机物的结构简式,每个节点处代表有一个碳原子,与其结合的氢原子的元素符号省略,这种化学式称为“键线式”。又知酯类在铜铬氧化物催化下,与氢气反应得到醇,羰基双键可同时被还原,但苯环在
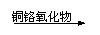 催化加氢过程中不变,其反应原理如下:
催化加氢过程中不变,其反应原理如下:
RCOOR’+2H2 RCH2OH+HO-R’
试填空:
⑴该有机物的的化学式为 。
⑵该有机物分子中的三个苯环________________共平面(选填“能”或“不能”)。
⑶1mol该有机物在铜铬氧化物催化下能与 mol氢气充分反应。
⑷该有机物与足量氢氧化钠溶液充分反应后的产物中,相对分子质量最小的钠盐的化
学式为 。
22.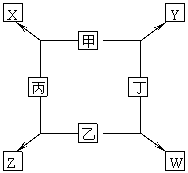 (12分)甲、乙、丙、丁四种单质在点燃条件下反应生成 X、Y、Z、W四种化合物,转化关系如右图所示,又知:
(12分)甲、乙、丙、丁四种单质在点燃条件下反应生成 X、Y、Z、W四种化合物,转化关系如右图所示,又知:
① 甲、乙、丙在常温下为气态单质,丁是目前
用量最大的金属单质。
② 常温下,X是无色液体,Y是黑色固体。
③ 丙在乙中燃烧发出苍白色火焰,丁在乙中
燃烧生成棕黄色的烟, W的水溶液呈黄色。
请填空:
(1) 丁在甲和X同时存在的条件下,可以被腐蚀,写出电极反应方程式
负极___________________________________________________,
正极___________________________________________________。
(2)丁与X在高温下反应时,氧化剂为(写化学式)___________________,其化学方程式为
______________________________________________________。
(3) 足量的丁与稀硝酸反应的离子方程式为
__________________________________________________________。
(4) 将Y看成碱性氧化物,Y与Z的溶液发生反应的离子方程式是__________ 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com