
题目列表(包括答案和解析)
33. 有一种硝酸盐晶体,分子式为M(NO3)z·nH2O,经测定其摩尔质量为242g/mol,取1.21g此晶体溶于水,配制成100mL溶液,将其置于电解池中用惰性材料作电极进行电解,当有0.01mol电子转移时,溶液中全部金属离子即在电极上析出,经测定,阴极增重0.32g (1)问1.21g此盐晶体物质的量是多少? Z值为多少?
(2)求M的原子量和n值
(3)如电解过程中溶液体积不变,计算电解结束后溶液的pH值
32.以石墨为电极,电解500mL3mol/LCuSO4溶液,当收集到5.6L(标况)气体时,再倒接电源的正负极,通电一段时间后,又收集到5.6L(标况)气体,求电解后所得溶液中各物质的物质的量的浓度(设整个过程中溶液的体积不变)和整个通电过程中电路流过的电子的物质的量。
31. 将200mL2mol/LAgNO3溶液和200mL1mol/LCu(NO3)2溶液混和,用铜片作电极进行电解,阴极上共有6.4g铜析出时停止电解,若溶液的体积变化忽略不计,则此时溶液中Cu2+的浓度为多少?
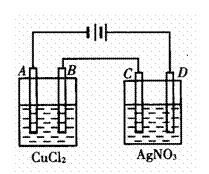
4、右图为以惰性电极进行电解:
(1)写出A、B、C、D各电极上的电极方程式:
A________________________________
B________________________________
C________________________________
D________________________________
(2)在A、B、C、D各电极上析出生成物的物质的量比________________________________________________。
2、Zn-Cu原电池的正负极与氧化还原反应 负极( )-- 电子--发生 反应--现象
正极( )-- 电子(电子流入)--发生 反应--现象 3、钢铁 电化学腐蚀中①析氢腐蚀(在酸性较强的电解质环境下)
负极 ,正极
②吸氧腐蚀(中性或弱酸性电解质溶液如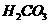 环境下)
环境下)
负极 正极
 总反应式
总反应式
1、原电池是把 能(氧化还原反应)转化为 能(电子在导线中定向移动)的装置
29. 对于下列装置中的反应,写出相应的电极反应式:
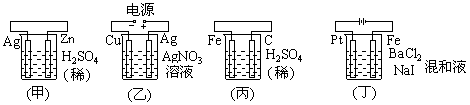
(1)甲装置中,Zn极: ; Ag极
(2)乙装置中,Cu极: ; Ag极
(3)丙装置中,Fe极: ; C极
28. 图中p、q为电源两极,A为2价金属X制成,B、C、D为铂电极,接通电源,金属X沉积于B,同时C、D产生气泡。试回答:
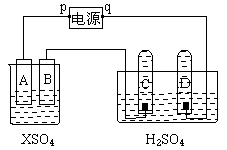
(1)p为 极
(2)A极发生了 反应;C为 极,试管里收集到 ;
D为 极,试管里收集到 ;
(3)C极的电极反应式
(4)当电路中通过0.004mol电子时,B电极上沉积金属X为0.128g,则此金属的原子量为
27. 按照下图接通线路,反应一段时间后,回答下列问题(假设所提供的电能可以保证电解反应的顺利进行):
(1)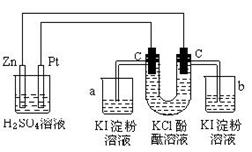 U型管内发生什么现象?
U型管内发生什么现象?
(2)写出有关反应的化学方程式:
(3)在a、b烧杯中发生什么现象:
(4)如果小烧杯中有0.508g碘析出,问大烧杯中,负极减轻多少?
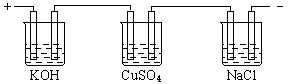
26.下图表示采用惰性电极电解相同物质量浓度,相同体积的KOH、CuSO4、NaCl溶液的情况。如果不考虑电解过程中溶液浓度变化对电极反应的影响,在相同的时间里,放出气体最多的是 溶液,放出气体最少的是 溶液。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com