
题目列表(包括答案和解析)
5. 据报道,N5是破坏力极强的炸药之一,18O2是比黄金还贵重的物质。下列说法正确的是 ( )
A、N5和N2互为同位素 B、1个18O2中含18个中子
C、原子半径:N<18O D、2N5 = 5N2是化学变化
4. 最近科学界合成一种“二重结构”的球形物质分子,是把足球型C60分子容纳在足球型Si60分子中,外面的硅原子与里面的碳原子以共价键结合。下列关于这种物质的叙述中,正确的是 ( )
A、是混合物 B、是化合物 C、不含极性键 D、其晶体属于原子晶体
3、下列各组物质的晶体中,化学键类型相同,晶体类型也相同的是 ( )
A、SO2和SiO2 B、CO2和H2O C、NaCl和HCl D、CCl4和KCl
2. 国庆50周年庆典结束时,数万只小气球腾空而起,若从安全角度考虑,气球中不应充H2,而适宜用下列气体中的 ( )
A、N2 B、He C、CH4 D、空气
1. 近年来,建筑装璜装饰材料进入家庭,调查发现经过装修的居室中由装璜装饰材料缓慢释放出来的化学污染物浓度过高,影响健康。这些污染物中最常见的是( )
A、CO B、SO2 C、甲醛、甲苯等有机物蒸气 D、臭氧
1.数据分析、处理;图象分析;范围讨论。
[例题]在标准状况下,取甲、乙、丙各30.0 mL,相同浓度的盐酸,然后分别慢慢加入组成相同的镁铝合金粉末,得下表中有关数据(假设反应前后溶液体积不发生变化);
|
实验序号 |
甲 |
乙 |
丙 |
|
合金质量/mg |
255 |
385 |
459 |
|
气体体积/Ml |
280 |
336 |
336 |
请回答:
(1)甲组实验中,盐酸(选填“适量”“过量”或“不足量”,下同) ,乙组实验中盐酸 。
(2)盐酸的物质的量浓度为 ;
(3)合金中Mg、Al的物质的量之比为 ;
(4)丙实验之后,向容器中加入一定量1.00 mol·L-1 NaOH溶液,能使合金中的铝粉恰好完全溶解,再过滤出不溶性固体,求所得滤液中各溶质的物质的量浓度(要求写出计算过程)。
 [习题]HNO3与金属反应时,还原产物可能是NO2、NO、N2O、N2或NH3的一种或几种。现有一定量的Al粉和Fe粉的混合物与100mL稀HNO3充分反应,反应过程中无任何气体放出。在反应结束后的溶液中,逐渐加入4mol/L的NaOH溶液,加入NaOH溶液的体积与产生沉淀的物质的量关系如图所示:
[习题]HNO3与金属反应时,还原产物可能是NO2、NO、N2O、N2或NH3的一种或几种。现有一定量的Al粉和Fe粉的混合物与100mL稀HNO3充分反应,反应过程中无任何气体放出。在反应结束后的溶液中,逐渐加入4mol/L的NaOH溶液,加入NaOH溶液的体积与产生沉淀的物质的量关系如图所示:
|
|
 B
B
0 3.0 15 16.5 18.5 V(NaOH)(ml)
请回答:(1)与HNO3反应后Fe元素的化合价是 +3价 。
(2)纵坐标中A点数值是 0.008 mol ,B点数值是 0.016mol 。原HNO3的浓度是 0.72mol/L 。
[习题]a g Mg在盛有b L(标准状况)CO2和O2混合气体的密闭容器中燃烧。
(1)若反应容器中CO2有剩余,则容器内的固体物质中一定含有___________。
(2)若反应后容器中O2有剩余,则容器内固体的质量为___________,此时有b L CO2和O2的混合气体中O2的体积(VO2)必须满足的条件是_______________。
(3)若反应后容器中无气体剩余,则容器内固体物质的质量(m)的取值范围为___________。
答案:(1)MgO(3分) (2)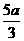 g(3分) b>VO2>
g(3分) b>VO2>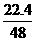 a (4分)
a (4分)
(3)(a+ ×32)<m<(a+
×32)<m<(a+ ×44) (4分)
×44) (4分)
2.有机框图推断 (含醛基)
1.有机物燃烧规律
[例题]充分燃烧只含有碳、氢、氧的一类有机物,消耗氧气的体积与生成二氧化碳的体积之比为9:8(相同条件下)。
(1)符合该条件的有机物的通式为 。
(2)若符合该通式的某有机物的相对分子质量为136,则其化学式为 ;若该有机物属于酯类且分子中含有苯环,则其可能的同分异构体有 种,写出其中任意两种的结构简式: ; 。
(3)若符合该通式的有机物相对分子质量为136,令该物质为A,它不能使FeCl3溶液显色,但可以被新制的银氨溶液氧化成B,B能在浓H2SO4存在和加热时,发生分子内的酯化反应生成C,C分子中有一个含氧的五元环,则A的结构简式为 。
 答案:(1)(C2H)n(H2O)m(3分)
答案:(1)(C2H)n(H2O)m(3分)
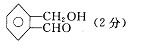 (2)C8H8O2
(2分) 6种 (2分)
(2)C8H8O2
(2分) 6种 (2分)
(3)
[习题]某类有机物CnHxOy完全燃烧需要O2的物质的量为该有机物的n倍,生成CO2
和H2O的物质的量之比为1:1
(1)该类有机物的分子通式为(CnHxOy中的x、y均以n表示) 。
(2)若n=3,写出符合下列条件的物质的结构简式(各一种):
①呈酸性,且能发生缩聚反应: 。
②呈中性,且能发生水解反应: 。
(3)有一种符合此通式的有机物,可以在一定条件下用农作物的秸秆制取,写出反应的
化学方程式(该有机物用结构简式表示): 。

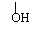 答案(1) CnH2nOn (2) ①HOCH2-CH2-COOH(或CH3-CH-COOH)
答案(1) CnH2nOn (2) ①HOCH2-CH2-COOH(或CH3-CH-COOH)
 ②H-C-O-CH2-CH2OH(或HO-CH2-C-O-CH3)
②H-C-O-CH2-CH2OH(或HO-CH2-C-O-CH3)

(3) (C6H10O5)n+ n H2O n(CHOH)4
2.装置图
[例题]用下列仪器、药品验证由铜和适量浓硝酸反应的气体中含NO(仪器可选择使用,N2和O2的用量可自由控制)。
已知:①NO+NO2+2OH-====2NO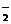 +H2O ②气体液化温度NO2 21℃;NO -152℃
+H2O ②气体液化温度NO2 21℃;NO -152℃

图2-2
试回答:(1)仪器的连接顺序(按由左→右连接,填各接口的编号)为 。
(2)反应前先通入N2,目的是 。
(3)验证反应产生的气体中含NO的现象是 。
(4)装置F的作用是 。
(5)如果O2过量,则装置B中发生反应的化学方程式为 。
答案:(1)1、5、4、10、11、6、7、2(3分,其中10和11可颠倒,错一个即不给分)
(2)驱赶装置中的空气,防止反应产生的NO被氧化(2分)
(3)通入O2后装置D中有红棕色气体生成(2分)
(4)分离NO和NO2(或使NO2液化)(其他合理回答都给分,共2分)
(5)4NO2+O2+4OH-====4NO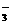 +2H2O(3分)
+2H2O(3分)
[习题]铜与硝酸在酸浓度不同时生成不同的产物,某课外活动小组为了证明并观察到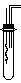 铜与稀硝酸反应的产物为NO,设计了如图所示的实验装置。
铜与稀硝酸反应的产物为NO,设计了如图所示的实验装置。
请你根据他们的思路,选择药品,完成该实验,并叙述实验步骤。
药品:稀硝酸、稀盐酸、Zn粒、CaCO3固体
(1)步骤:①检查装置的气密性;② ;③ ;④ ;⑤ ;⑥用注射器向广口瓶内推入氧气(或空气)。
(2)推入氧气或空气的目的是 。
(3)分别将等质量的铜片与等体积均过量的浓硝酸、稀硝酸反应,所得到的溶液前者成绿色,后者呈蓝色,某同学提出这可能是Cu2+浓度差异引起的,你同意这种看法吗?(填“同意”或“不同意”),原因是 ;另一同学提出溶液呈“绿色”是Cu2+与NO2混合的结果,请你设计一个实验证明之(简述实验方案和实验现象) 。
答案:(1)②向试管中加入一定量CaCO3 固体③向试管中倒入过量的稀硝酸,并迅速塞紧带铜丝和导管的橡皮塞④待反应完全后,将右边导管插入试管内接近液面⑤将铜丝插入到溶液中(2)检验生成NO气体(3)不同意 铜片质量相同,溶液体积相同,生成Cu2+ 浓度相同,加热绿色溶液,有红棕色气体产生,溶液变成蓝色。
1.基本仪器、基本操作:过滤(一贴、二低、三靠)、蒸发、萃取分液
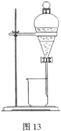 (3)依据图11所示,在萃取操作中应选取的有机溶剂为(多选不给分)_____________;
(3)依据图11所示,在萃取操作中应选取的有机溶剂为(多选不给分)_____________;
A.四氯化碳 B.甲苯 C.乙醇 D.裂化汽油
(4)在萃取、分液的过程中,把分液漏斗玻璃塞上的凹槽对准漏斗口上的小孔,其目的是 ____________ ;
如图13所示,待分液漏斗内的混合液分层后,应采取的操作是 __________________________________________________________ ;
(5)加热蒸发溶液D时,除需带有铁圈的铁架台、坩埚钳和火柴外,还必须用到的仪器有 、 、 ;
(3)若过滤使用的仪器和用品已有:滤纸、铁架台、铁圈、烧杯、漏斗,还需要补充的仪器或用品是__________________________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com