
题目列表(包括答案和解析)
4、在由水电离出的c(H+)=1×10-13mol·L-1的溶液中,可能大量共存的离子组是( )
A、Fe2+、Na+、NO3-、Cl- B、Ba2+、Na+、NO3-、Cl-
C、SO42-、S2O32-、NH4+、Na+ D、Mg2+、Na+、Br-、AlO2-
3、硫酸铵在强热条件下分解:生成NH3、SO2、N2和H2O,该反应中的氧化产物和还原产物的物质的量之比为( )
A、1:3 B、2:3 C、4:3 D、1:1
2、随着人们生活节奏的加快,方便的小包装食品已被广泛接受,为了防止富脂食品的氧化变质,延长食品的保质期,在包装袋中常放入抗氧化物质,下列不属于抗氧化物质的是( )
A、生石灰 B、还原铁粉 C、亚硫酸钠 D、维生素C
1、NA代表阿伏加德罗常数的数值,下列说法正确的是( )
A、常温常压下11.2LN2含有的原子数为NA
B、 常温常压下1molHe含有的原子数为NA
C、 71gCl2含有的原子数为NA
D、18gNH4+含有的电子数为NA
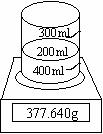
42、下图是测定Na2O2(含Na2O)杂质纯度的实验装置,不同时间电子天平的读数如下表所示:
|
实验操作 |
时间 |
 天平读数/克 天平读数/克 |
|
烧杯 |
|
370.00 |
|
烧杯 + 水 + 样品 |
0 |
377.640 |
|
30 |
376.920 |
|
|
60 |
376.400 |
|
|
90 |
376.200 |
|
|
120 |
376.200 |
|
|
|
|
试计算样品中Na2O2的质量分数,并估算最后溶液的pH。
41、以淀粉为原料制取酒精,若有1kg含质量分数为40%淀粉的植物果实,经反应制得227g质量分数为80%的酒精,则淀粉的转化率是多少?
40、 野依良治最重要的发现是成功合成了对人的生理起支配作用的激素物质“前列腺素”,有一种可用来治疗“哮喘”的“前列腺素”PGE2(Ⅱ)的结构如右:
野依良治最重要的发现是成功合成了对人的生理起支配作用的激素物质“前列腺素”,有一种可用来治疗“哮喘”的“前列腺素”PGE2(Ⅱ)的结构如右:
提示:A 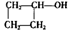 可以表示为
可以表示为 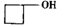
B 碳原子上连有四个不相同的基团时,称该碳原子为手性碳原子,每个手性碳原子会出现两个光学异构体。
根据材料回答下列问题:
(1)写出这种化合物的分子式 。
(2)此化合物含有的官能团有 。
A 羧基 B 醛基 C 酯基 D 酮基
E 羟基 F 酚 G 烯基
(3)1mol此物质和NaOH溶液反应,需NaOH g,如果此物质为液态,1mol该物质耗用金属钠 mol。
(4)该物质分子结构中有 个手性碳原子,有 种不同的光学异构体。
39. (1)①高空中的氧气受阳光中紫外线照射,通过下面的反应形成臭氧:
a.O2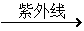 2O b.O2+O→O3写出以上a、b反应的总方程式。
2O b.O2+O→O3写出以上a、b反应的总方程式。
_______________________________________________________________________________
②人类大量使用“消耗臭氧层物质”(简称ODS),是使臭氧层被破坏的主要原因,其中CFC(氟利昂)的使用是破坏臭氧层的祸首,氟利昂在阳光下可分解产生氯原子,其破坏臭氧的反应式如下:a.O2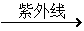 2O b.O3+Cl→O2+ClO c.ClO十O→O2+Cl
2O b.O3+Cl→O2+ClO c.ClO十O→O2+Cl
试写出b、c的总反应方程式。
______________________________________________________________________________。
(2)臭氧是一种具有鱼腥味的胆蓝色气体,能使湿润的碘化钾淀粉试纸变蓝,则反应的化学方程式为____________________________________________,反应中还原产物是____________________________________________。
38. 科学家制造出了一种神奇塑料,它能自动愈合自身内部的细微裂纹,即具有自我修复功能,它是由液态二环戊二烯和一种催化剂合成的,试根据以下信息回答有关问题:
信息一:烯烃可以发生双烯合成。
CH2=CH-CH3+CH2=CH2→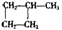 (简写为
(简写为 )
)
信息二:CH2=CH-CH=CH2与HBr反应的化学方程式为:
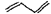 +HBr→
+HBr→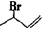 +
+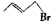
20% 80%
环戊二烯在双分子合成时一个发生1,2一加成,另一个就发生1,4-加成。
信息三:“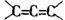 ”极不稳定。
”极不稳定。
信息四: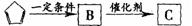
A 二环戊二烯 神奇塑料
问题:(1)写出A和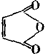 反应的化学方程式,并指出1mol产物最多能消耗多少克NaOH,写出产物和Cl2发生加成反应的产物的结构简式。
反应的化学方程式,并指出1mol产物最多能消耗多少克NaOH,写出产物和Cl2发生加成反应的产物的结构简式。
(2)写出A→B、B→C的化学方程式,并指出B→C的反应类型。
(3)写出A的所有开链不饱和烃的同分异构体。
(4)科学家看到人的身体受到伤害流血结痂的过程而想到制备出这种神奇塑料,这种原理我们称之为 学。
37. 最近,德国科学家实现了铷原子气体超流体态与绝缘态的可逆转换,该成果将在量子计算机研究方面带来重大突破。已知铷是37号元素,质量数是85。根据材料回答下列问题:
(1)铷Rb-37位于周期表的第 周期、第 族。
(2)关于铷的结构和性质判断正确的是 。
①与水反应比钠剧烈 ②它的原子半径比钠小 ③它的氧化物暴露在空气中易吸收CO2 ④它的阳离子最外层电子数和镁相同 ⑤它是还原剂
A ①③④ B ②③⑤ C ②④ D ①③⑤
(3)氢化铷与水反应可放出氢气,则下列叙述正确的是 。
A 氢化铷溶于水显酸性 B 氢化铷中氢离子被还原为氢气
C 氢化铷与水反应时,水是还原剂 D 氢化铷中氢离子最外层有两个电子
(4)现有铷和另一种碱金属形成的合金50g,当它与足量水反应时,放出标准状况下的氢气22.4L;这种碱金属可能是 。
A Li B Na C K D Cs
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com