
题目列表(包括答案和解析)
22、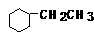 (6分)结构中没有环状的烷烃又名开链烷烃。其分子式通式是CnH2n+2(n是正整数)。分子中每减少2个碳氢键,必然同时会增加1个碳碳键。它可能是重键(双键或三键)也可能是连结成环状烃,都称为增加了1个不饱和度(用希腊字母Ω表示,又名“缺氢指数”)。例如若干烃类分子和烃基的不饱度如下:
(6分)结构中没有环状的烷烃又名开链烷烃。其分子式通式是CnH2n+2(n是正整数)。分子中每减少2个碳氢键,必然同时会增加1个碳碳键。它可能是重键(双键或三键)也可能是连结成环状烃,都称为增加了1个不饱和度(用希腊字母Ω表示,又名“缺氢指数”)。例如若干烃类分子和烃基的不饱度如下:
① CH3CH2CH3
Ω=0;②(CH3)2CH- Ω=0;③CH2=CHCH2- Ω=1;④
CH3CH2CH3
Ω=0;②(CH3)2CH- Ω=0;③CH2=CHCH2- Ω=1;④
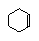
Ω=1;⑤C8H15- Ω=1;⑥ Ω=2;⑦ Ω=2;
⑧CH3C≡CCH2CH=CH2 Ω=3;
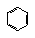
 ⑨CH3(CH=CH)3CH3 Ω=3;⑩ Ω=4;⑾
Ω=4;⑿C7H7- Ω=4。
⑨CH3(CH=CH)3CH3 Ω=3;⑩ Ω=4;⑾
Ω=4;⑿C7H7- Ω=4。
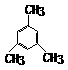 ⑴请写出下列各烃分子的Ω
⑴请写出下列各烃分子的Ω
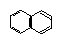
A B
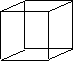 C
(立方烷,正立方体的每个顶点上有一个碳原子,每个碳原子上有一个
C
(立方烷,正立方体的每个顶点上有一个碳原子,每个碳原子上有一个
氢原子)
⑵请写出下列烃基的Ω
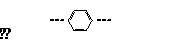
D (两价基团)Ω=
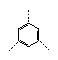
E (三价基团)Ω=
F …C≡C… (两价基团)Ω=
21、(10分)下面是3种有机物的结构式和名称(数字为碳原子编号):
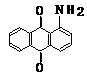
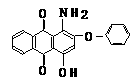
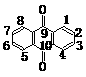
蒽 醌 1-氨基蒽醌(Ⅰ) 分散红 3B (Ⅱ)
用化合物(Ⅰ)为起始原料,经进3步主要反应可以得到化合物(Ⅱ)。

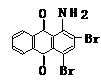
 (a)
+ Br2
→
+
(a)
+ Br2
→
+


(b)
+ H2SO4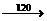 +
↑
+
↑
红棕色
+ ↑

 无色
无色
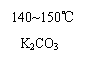
 (c)
+
(c)
+
+ HBr
⑴请在以上3个化学方程式的方框内分别填入有关的化学式和化学式的化学计量数(即“系数”)。
⑵从第()步反应的化学原理看,它既发生了取代反应又发生了氧化还原反应。其中氧化剂是 ;配平后的化学方程式中共转移了 电子。
⑶请将反应式()箭号下面的改写在化学方程式的左端,重新另写出它的化学方程式 ,并配平之。
20、(6分)在某条件下,容器中有如下平衡反应:A+4B≒2C+D+热量 此时A,B,C,的物质的量均为amol,而D的物质的量为dmol。
⑴改变a的取值,再通过改变反应条件,可以使批评重新达到平衡,并限定达到新的平衡时,D的物质量只允许在d/2到2d这间变化,则a的取值范围应是 (用a和d的关系式表示)。
⑵如果要使本反应重新建立和平衡中,D的物质的量只允许在d到2d之间取值,则应该采取的措施是 (从下面列出的选项中选择)。
A 升高反应温度 B 增大反应容器内之压强 C 增大反应容器容积
D 降低批评温度 E 减小反应容器内之压强 F 减小反应容器容积
19、(4分)已知气态氯化铝分子以双聚形式存在,其结构如下图所示:图中“Cl→Al”表示Cl原子提供
|


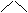
了一对电子与Al原子共享。又,已知硼酸H3BO3为白色固体,溶于水显弱酸性,但它却只是一元酸,可以用硼酸在水溶液中的电离平衡解释它只是一元弱酸的原因。请写出下面这个方程式右端的两种离子的表达式:
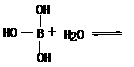
+
18、(10分)“卤块”的主要成分为MgCl2(含Fe2+、Fe3+、Mn2+等杂质离子),若以它为原料,按如下工艺流程图,即可制得“轻质氧化镁”。如果要求产品尽量不含杂质离子,而且成本较低,流程中所用试剂或pH值控制可参考下列附表确定。
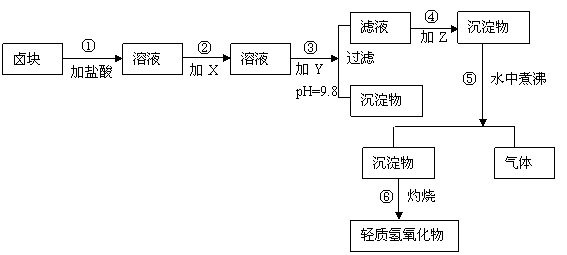
轻质氧化镁工艺流程图
表1 生成氢氧化物沉淀的值
|
物质 |
开始沉淀 |
沉淀完全 |
|
Fe(OH)3 Fe(OH)2 Mn(OH)2 Mg(OH)2 |
2.7 7.6 8.3 9.6 |
3.7 9.6Ω 9.8 11.1 |
Ω注:Fe2+氢氧化物呈絮状,不易从溶液中除去,所以常将它氧化成为Fe3+,生成Fe(OH)3沉淀而去除之。
表2 化学试剂价格表
|
试剂 |
价格(元/ t ) |
|
漂液(含NaClO25.2%) H2O2(30%) NaOH(固98%) Na2CO3(固99.5%) 卤块(MgCl2,30%) |
450 2400 2100 600 310 |
请填写以下空白:
⑴在步骤②加入试剂X,最付佳选择应是 ,其作用是 。
⑵在步骤③加入的试剂Y应是 ,之所以要控制pH=9.8,其目的是 。
⑶在步骤⑤时发生的化学反应方程式是: 。
17、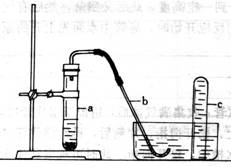 用示意图中的简易装置可以进行气体的发生和收集。
用示意图中的简易装置可以进行气体的发生和收集。
⑴实验前应如何检查该装置的气密性?答:
⑵拔开试管a的橡皮塞,加入10mL6mol/L稀硝酸和1g薄铜片,立即将带有导管的橡皮塞塞紧试管口。反应开始时速度缓慢,逐渐加快。请写出在试管a中所发生的所有反应的化学方程式。答;
⑶从反应中开始到反应结束,预期在试管a中可观察互哪些现象?依次逐一写出。答;
⑷在反应开始时,可观察到导管b中的水面先沿导管b慢慢一升到一定高度,此后又回落,然后有气泡从管回冒出。试说明反应开始时,导管中不面先上升的原因。答:
⑸试管c收集满气体后,用拇指堵住管口,取出水槽。将管口向上,松开拇指,片刻后,再次堵住管口,将试管又再倒置于水槽中,松开拇指,此时可观察到什么现象?答:
16、CaC2和ZnC2,Al4C3,Mg2C3,Li2C2等都同属离子型碳化物,请通过对CaC2制C2H2的反应进行思考,从中得到必要的启示,判断下列反应产物正确的是
A ZnC2水解生成乙烷(C2H6) B Al4C3水解生成丙炔(C3H4)
C Mg2C3水解生成丙炔(C3H4) D Li2C2水解生成乙烯(C2H4)
第Ⅱ卷
(共四大题,8小题,66分)
15、在一定条件下,全盛氨反应达到平衡后,混合气体中NH3的体积占25%。若反应前后条件保持不变,则反应后缩小的气体体积与原反应物体积的比值是
A 1/5 B 1/4 C 1/3 D 1/2
14、已知原子量:Li 6.9,Na 23,K 39,Rb 85。今有某碱金属M及其氧化物M2O组成的混合物10.8g,加足量水充分反应后,溶液经蒸发和干燥得固体16g。据此可确定碱金属M是
A Li B Na C K D Rb
13、在同温同压下,把等体积的空气和二氧化碳混合,并使之在高温下跟足量的焦炭反应。若氧气和二氧化碳最后全部转化为一氧化碳,则反应后气体中一氧化碳的体积分数约是
A 0.60 B 0.64 C 0.70 D 0.75
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com