
题目列表(包括答案和解析)
21.工业上早在十九世纪中叶便已生产的过氧化氢,随着生态环境的保护而日益被重视,成为社会需求迅速增长的化学品,过氧化氢是一种绿色氧化剂,延伸产品及其应用迅速。
⑴有人把氯气通人过氧化氢(H218O2)的水(H2O)溶液中,发生反应:
Cl2+ H218O2=H++Cl-+H18O18OCl H18O18OCl=H++Cl-+18O2
对上述反应的说明错误的是 。
A.氯气通人过氧化氢溶液产生的氧气全部来自过氧化氢
B.氯气通人过氧化氢溶液发生的反应可表示为Cl2+ H2O2=2HCl+O2
C.过氧化氢有氧化性
D.反应中,过氧化氢中氧原子之间的化学键没有变化
⑵在冶炼铜时,需要把粗铜溶解,可用:a.浓硫酸b.焙烧后用稀硫酸c.过氧化氢与稀硫酸三种方法,某厂家最终确定用c方法。
①写出用c方法溶解铜的化学反应方程式
②简述最终选用c方法的理由:
⑶过氧乙酸(CH3COOOH)是常用的一种杀菌消毒的有机物,它可以通过乙酸和过氧化氢反应制得,其化学反应方程式为
20.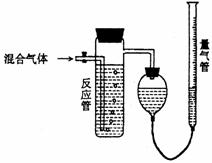 工业上测量SO2、N2、O2混合气体中SO2含量的装置如下图;反应管中装有碘的淀粉溶液。SO2和I2发生的反应为(N2、O2不与I2反应):SO2+I2+2H2O→H2SO4+2HI
工业上测量SO2、N2、O2混合气体中SO2含量的装置如下图;反应管中装有碘的淀粉溶液。SO2和I2发生的反应为(N2、O2不与I2反应):SO2+I2+2H2O→H2SO4+2HI
⑴混合气体进入反应管后,量气管内增加的水的体积等于 的体积(填写气体的分子式)。
⑵反应管内溶液蓝色消失卮,没有及时停止通气,则测得的SO2含量 (选填:偏高,偏低,不受影响)。
⑶反应管内的碘的淀粉溶液也可以用 代替(填写物质名称)。
⑷若碘溶液体积为VamL.,浓度为Cmol·L-1,N2与O2的体积为VbmL(已折算为标准状况下的体积)。用C、Va、Vb表示SO2的体积百分含量为: 。
⑸将上述装置改为简易实验装置,除导管外,还需选用的仪器为. (选下列仪器的编号)。
a.烧杯 b.试管 c.广口瓶 d.容量瓶 e.量筒 f.单孔塞 g.双孔塞
19.为测定硫酸铵和氯化铵固体混合物中氯化铵的质量分数,甲、乙两位同学按下列所示的实验步骤进行实验:称量样品、溶解、加过量试剂A、过滤出沉淀B、洗涤沉淀、烘干称量、处理实验数据,得出结果。
⑴实验时,甲同学选用硝酸银溶液作试剂A,乙同学选用氯化钡溶液作试剂A。其中 填(“甲”或“乙”)同学选择的试剂A不合理,其理由是
⑵以下都是试剂A选择正确时进行的实验:
①为进行称量、溶解、反应、过滤、洗涤沉淀的各项操作,准备了以下仪器:托盘天平与砝码、过滤器、铁架台及附件、胶头滴管、量筒,其中还缺少的必备仪器是 。
②若过滤所得沉淀未经洗涤即烘干称量,测出的氯化铵的质量分数
(填“偏高”、“偏低”或“不变”)。
③检验加入的试剂A是否过量的方法是
。
18.在一定条件下,萘可被浓硫酸、浓硝酸的混合酸硝化,生成二硝基化合物
1,5-二硝基萘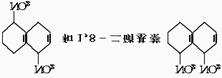 的混合物。后者可溶于质量分数大于98%的硫酸中,而前者却不能。利用这一性质可将这两种异构体分离开来。将这两种硝化产物加入适量的98%硫酸中,充分搅拌,用耐酸漏斗过滤 。要从滤液中得到固体1,8-二硝基萘,应采用的方法是
[ ]
的混合物。后者可溶于质量分数大于98%的硫酸中,而前者却不能。利用这一性质可将这两种异构体分离开来。将这两种硝化产物加入适量的98%硫酸中,充分搅拌,用耐酸漏斗过滤 。要从滤液中得到固体1,8-二硝基萘,应采用的方法是
[ ]
A.蒸发浓缩晶体
B.向滤液中加水后过滤
C.用Na2CO3溶液处理滤液
D.将滤液缓缓加入水中
第II卷(非选择题,共78分)
17.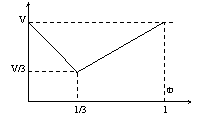 某链烃在一定条件下可和H2发生反应,取不同体积比的CnHm与H2(两者的体积和为定值V)在一定条件下反应,V与Φ(CnHm)[CnHm的体积分数]的关系如图。则m和n的关系是
某链烃在一定条件下可和H2发生反应,取不同体积比的CnHm与H2(两者的体积和为定值V)在一定条件下反应,V与Φ(CnHm)[CnHm的体积分数]的关系如图。则m和n的关系是
A.m=2n+2 B.m=2n [ ]
C.m=2n-2 D.m=2n-6
16.向10mL 0.1mol/L的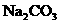 溶液中通入22.4mL(标况)
溶液中通入22.4mL(标况)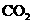 ,当气体全部溶解时,溶液中微粒浓度关系正确的是
[ ]
,当气体全部溶解时,溶液中微粒浓度关系正确的是
[ ]
A.
B.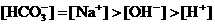
C.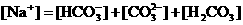
D.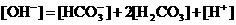
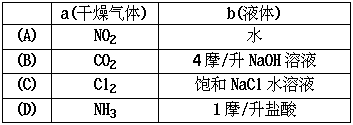
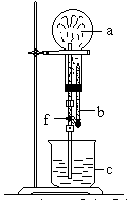
15.在下图装置中,烧瓶中充满干燥气体a,将滴管中的液体b挤入烧瓶内,轻轻振荡烧瓶,然后打开弹簧夹f,烧杯中的液体b呈喷泉状喷出,最终几乎充满烧瓶。则a和b分别是 [ ]
14.下列物质在一定条件下,既能和某些非金属单质、金属单质反应,又能和某些金属氧化物,非金属氧化物反应的是 [ ]
A.NaOH溶液 B.稀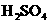 C.NaCl溶液 D.
C.NaCl溶液 D.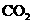
13.氯酸(HClO3)是一种强氧化性酸。若将铜粉投入氯酸溶液中,下列物质一定不可能生成的是 [ ]
A.氯酸铜 B.高氯酸铜 C.氯化铜 D.氢气
12.NaH是-种离子化合物,它跟水反应的方程式为:NaH+H2O=NaOH+H2↑,它也能跟液氨、乙醇等发生类似的反应,并都产生氢气。下列有关NaH的叙述错误的是 [ ]
A跟水反应时,水作氧化剂 B NaH中H-半径比Li+半径小
C 跟液氨反应时,有NaNH2生成 D 跟乙醇反应时,NaH被氧化
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com