
题目列表(包括答案和解析)
25.将1.05g铝和过氧化钠的混合物放入一定量的水中,充分反应后固体无剩余。再向其中加 入50mL1mol·L-1的盐酸,可恰好使反应过程中产生的沉淀刚好消失。求原混合物中铝、过氧化钠各多少克?
24.(10分)手性分子是早就为化学工作者熟知的,但美国和日本的三位科学家却因为他们在手性分子可用来加速并控制化学反应方面的创造性工作,分享了2001年诺贝尔奖。在有机物分子中,若某碳原子连接着四个不同的原子或原子团,这种碳原子称为“手性碳原子”,凡只有一个手性碳原子的物质一定具有光化学活性。
(1)写出只含有一个碳原子的手性分子的结构式 。
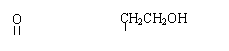
(2)某有机物A(CH3-C-O-CH2-CH-CH2CHO)是否具有光学活性 (“是”或“否”),若要使其具有或失去光学活性,其发生的反应类型可以是 。
①酯化;②消去;③加成;④水解;⑤氧化;⑥还原
(3)某有机物B(C3H7O2N)具有如下性质:a. 既能与强酸反应,又能跟强碱反应; b. 具有光学活性。试回答:
①写出B中官能团的名称 。
②写出B的结构简式 。
③若2分子B在一定条件下生成环状结构化合物C,则C的结构简式为 。
④若B在一定条件下生成高分子化合物D,写出B→D的化学方程式 。
⑤写出B的一个不属于同类别的同分异构体结构简式 。
23.(9分)CO不仅是家用煤气的主要成分,也是重要的化工原料。美国近年来报导一种低温低压催化工艺,把某些简单的有机物经“羰化”反应后可以最后产生一类具有优良性能的装饰性高分子涂料、粘胶剂等,如下图所示:
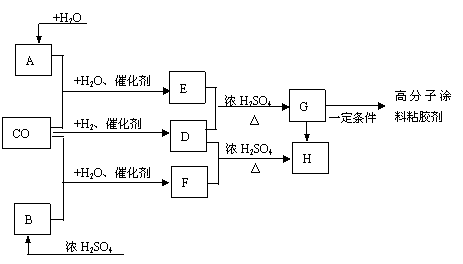
电石
酒精
图中G(RCOOR’)有一种同分异构体是E的相邻同系物;而H有一种同分异构体则是F的相邻同系物。已知D由CO和H2按物质的量之比为1:2完全反应而成,其氧化产物可发生银镜反应;H是含有4个碳原子的化合物。
试推断:
(1)写出B、E、G的结构简式
B: E: G:
写出与G同类别的两个G的同分异构体的结构简式
(2)完成下列反应的化学方程式
①A+CO+H2O
②F+D
③G 高分子化合物
高分子化合物
22.(12分)根据下面物质间转换的框图,回答有关问题:
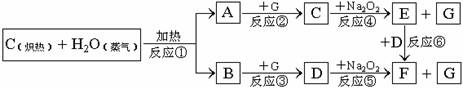
(1)由反应①产生的A、B混合物的工业名称是 。
(2)写出框图中D、E的电子式:D ;E
(3)如果2mol Na2O2与足量水蒸气反应,可得标准状况下气体的体积是多少 L,同时反应中转移电子总数是 。(NA表示阿佛加德罗常数)
(4)请设计一个课堂小实验,证实反应⑤是放热反应。
(5)如果A、B混合气体7.8g(平均摩尔质量10g·mol-1),在与G充分反应后,通过足量Na2O2层,可使Na2O2增重 g,并得到O2 mol。
21、(11分)用铁作阳极、石墨作阴极电解NaOH溶液,电极反应式别是:阳极 ,阴极 。溶液的PH变化是 。若电解质溶液与空气接触,观察到的现象是 ,原因是 (用化学方程式表示)。当放出22.4升气体(标况),欲使溶液恢复原有组成应加入 。其质量是 。
20.(10分)实验室里用下图示出的装置制取溴化亚铁。其中,A为CO2发生装置,D和d中均盛有液溴,E为外套电炉丝的不锈管,e是两只耐高温的瓷夹,其中共盛有56g细铁粉。实验开始时先将铁粉加热至600-700℃,然后将干燥、纯净的CO2气流通入D中,E管中的物质开始反应,不断地将d中的液溴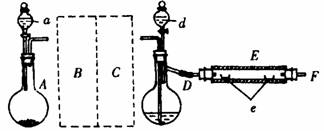 滴入100-120℃的D中,经过几小时的连续反应后在不锈钢管一端沉积有黄绿色鳞片状溴化亚铁80g。
滴入100-120℃的D中,经过几小时的连续反应后在不锈钢管一端沉积有黄绿色鳞片状溴化亚铁80g。
(1)如何检查D装置的气密性?
(2)若导入的CO2不干燥,会在E中发生副反应,其化学方程式为 。
(3)在A中盛有CaCO3,a中盛有6mol·L-1盐酸。为使A中产生的CO2在进入D之前既干燥又纯净,B、C处应设置和各仪器中应盛有何种试剂?
。
(4)实验时,D和E的橡胶塞为什么最好用铝箔包住?
(5)反应过程中要不断地通入CO2,其主要作用是:① ② 。
(6)E中进行的反应是:2Fe+3Br2=2FeBr3,2FeBr3=2FeBr2+Br2↑。此实验中溴化亚铁的产率为 。
(7)为防止污染空气,实验时应在F处连接盛有 的尾气吸收装置。
19.(10分)某学生为将含有少量杂质铜的氯化铁提纯.拟定以下实验步骤:
①把样品加蒸馏水溶解;②过滤除去杂质;③把滤液加热蒸干得到FeCl3晶体.
(1)你认为此方案是否科学,试用化学方程式和简要文字表达其理由.
答: .
(2)请你设计提纯氯化铁方案(只要求写出提纯步骤,最多只允许6步完成).
答:
18.1.92g Cu投入到一定量的浓HNO3中,Cu完全溶解,生成气体颜色越来越浅,共收集到标准状况下672ml气体,将盛有此气体的容器倒扣在水槽中,通入标准状况下一定体积的O2,恰好使气体完全溶于水,则通入O2的体积为 ( )
A.504 mL B.336 mL C.224 mL D.168 mL
第Ⅱ卷(非选择题 共76分)
17.有一铁的氧化物样品,用140mL5mol·L-1盐酸可恰好使其完全溶解。所得溶液可吸收标准状况下0.56L氯气,使其中的Fe2+全部转化为Fe3+。该样品可能的化学式为 ( )
(A)Fe4O5 (B)Fe5O7 (C)Fe2O3 (D)Fe3O4
16.乙烯酮(CH2=C=O)在一定条件下能与含活泼氢的化合物发生加成反应,反应可表示成CH2=C=O+HA→CH3COA。乙烯酮在一定 条件下与下列各试剂发生加成反应时所得产物不正确的是 ( )
(A)与HCl加成时得CH3COCl (B)与H2O加成时得CH3COOH
(C)与CH3OH加成时得CH3COCH2OH (D)与CH3COOH加成时得CH3COOCOCH3
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com