
题目列表(包括答案和解析)
3.在门窗紧闭的室内用煤炉取暖易发生煤气中毒。引起煤气中毒的主要气体是
A.CO2 B.O2 C.CO D.N2
2.下列物质中,属于纯净物的是
A.氨水 B.盐酸 C.液氯 D.漂粉精
1.人类未来理想的燃料是
A.煤 B.石油 C.天然气 D.氢气
2.在天平两端的烧杯中,分别盛有等质量、等溶质质量分数的稀硫酸,调整天平至平衡后,向天平两端的烧杯中分别加入等质量的镁和铜铝合金,恰好完全反应,且天平仍保持平衡。则铜铝合金中铜与铝的质量比为
[ ]
A.1∶1 B.2∶1
C.1∶2 D.1∶3
(答案:1.D 2.D)
例5.炭和CaCO3的混合物在空气中受强热后,CaCO3完全分解,炭完全氧化。如果生成的CO2总质量等于混合物的总质量,则混合物中炭的质量分数为 [ ]
A.82.6% B.17.4%
C.21.5% D.54.3%
分析:这是一道没有提供具体数据的计算题,但已具备了解题条件(非数据条件),这个隐藏在非数据之中的条件是生成的CO2的总质量等于混合物的总质量。抓住这一点,用炭氧化生成CO2的质量增加量等于CaCO3分解生成CO2质量的减少量,求出炭和CaCO3的质量之比,然后求出炭的质量分数。(上接第15页)
解:设混合物中炭的质量为x,CaCO3 的质量为y。
C+O2  CO2 增加质量
CO2 增加质量
12 44 44-12=32

CaCO3  CaO+CO2 减少质量
CaO+CO2 减少质量
100 44 100-44=56

同学们,理解了吗?下面的两题请解解看。
1.将4克SO3溶于46克水中,所得溶液溶质的质量分数是 [ ]
A.8% B.8.7%
C.9% D.9.8%
例4.60℃时,50克水中最多能溶解55克KNO3。把60℃时210克KNO3饱和溶液蒸发掉50克水后,再降至60℃时,析出晶体后溶液中溶质的质量分数是 [ ]
A.35.5% B.58.1%
C.17.2% D.52.4%
分析:此题中“把60℃时210克KNO3饱和溶液蒸发掉50克水后,再降至60℃时“实际上是用来迷惑学生的多余条件,不认真审题,就会钻进溶解度计算的死胡同而不得其解。因此解答此类题的关键是,明确在一定条件下饱和溶液结晶后剩余溶液仍为饱和溶液,所以,抓住定义即可得:
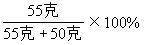
=52.4%
例 3.用 25.30毫升 98%的浓H2SO4(?=1.84克/厘米3)配制20%的H2SO4溶液(?=1.14克/厘米3)200毫升,需加水
[ ]
A.181.55毫升 B.174.70毫升
C.153. 44毫升 D.200毫升
分析:许多学生误认为需加水为200毫升25.30毫升=174.70毫升而选 B。其实,此题隐蔽着一个重要条件,即两种不同的液体相混合时其体积不等于混合前两种不同液体的体积之和,就好比1体积大豆加上1体积小米时,小米会落入大豆的空隙里。其正确解法是:
解:设需加水的体积为x。
则25.30毫升×1.84克/厘米3×98%=(x×1克/厘米3+25.30毫升×1.84克/厘米3) ×20%
解之得x≈181.55毫升
例2.已知20℃时硝酸钾的溶解度是31.6克。在此温度下,将50克硝酸钾晶体倒入50毫升蒸馏水中,充分搅拌,所得溶液的溶质质量分数为
[ ]
A.50% B.76%
C.24% D.25%
分析:某些学生忽视了硝酸钾溶于水的量要受溶解度的限制这一隐蔽条件,而误选A。其实50克水只能溶解15.8克硝酸钾,根据溶质质量分数概念,未溶解部分的溶质既不能计入溶质质量,也不能算到溶液质量之中,所以所得溶液溶质的质量分数为24%。
例1.6.2克氧化钠溶于 93.8克水中,所得溶液的溶质质量分数是
[ ]
A.等于6.2% B.大于6.2%
C.小于6.2% D.无法计算
分析:因为Na2O溶于水后,隐藏着Na2O+H2O=2NaOH的化学反应,所以溶液中的溶质不是Na2O,而是NaOH,且反应后的溶质是8克,所以溶液的溶质质量分数大于6.2%。
26.在常温常压下,把a mol的NH3和O2的混合气充入密闭容器中,在催化剂存在下加热,使其充分反应,然后恢复到原来的温度和压强.
(1)写出容器内NH3被氧化和形成HNO3的化学方程式.
(2)若原混合气中O2的体积分数为x,最后在容器中生成的HNO3为ymol.
请填写下表.
|
x的取值范围 |
用x表示的y值表示式 |
|
|
|
|
|
|
|
|
|
(3)在坐标图上画出y=f(x)的关系曲线.
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com