
题目列表(包括答案和解析)
2. 为除去MgCl2溶液中的Fe3+,可在加热条件下加入一种试剂,过滤后在滤液中加入适量盐酸.符合此要求的试剂是 [ ]
A.NaOH B.MgO C.MgCO3 D.Na2CO3
1. 在下列各化合物中属于强电解质的是 [ ]
A.H3PO4 B.HF C.BaSO4 D.HBr
22.在常压和500℃时把O2和SO2按1:2体积比混合,如果混合前O2为10mol,平衡混合气中SO3占总体积的91%,
求:(1)平衡时有多少摩O2转化?
(2)混合气中SO2占总体积的分数?
(3)SO2的转化率是多少?
(4)若在相同条件下,充入20molSO3,则达平衡时O2占混合气中的总体积的分数?
单元练习11 化学平衡(一)
1解析: 答案:C
2解析: 答案:C
3解析: 答案:AC
4解析: 答案:AD
5解析: 答案:D
6解析: 答案:AC
7解析: 答案:B
8解析: 答案:C
9解析: 答案:BD
10解析: 答案:C
11解析: 答案:C
12解析: 答案:B
13解析: 答案:B
14解析: 答案:A
15解析: 答案:B
16解析: 答案:AD
17解析: 答案:正 水解 正 盐酸
18解析:
答:
(1)0.013(2分)
(2)1.0 催化剂(各1分,共2分)
(3)> >(各1分,共2分)
(4)由吸热温度升高时,平衡向右移动(各1分,共2分)
19解析:
答: H++OH-=H2O,使平衡向脱矿方向移动 5Ca2++3PO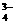 +F-=Ca5(PO4)3F↓加Ca2+(或加PO
+F-=Ca5(PO4)3F↓加Ca2+(或加PO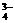 ,或其它合理的方法均给分
,或其它合理的方法均给分
20解析:
答:

21解析:答:第1空:0.94 第2空:76.5
22解析:
同温,同压下,气体体积之比等于物质的量之比
O2
+
2SO2 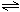 2SO3
2SO3
起始 10 20 0
转化 x 2x 2x
平衡 10-x 20-2x 2x
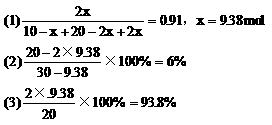
(4)
2SO3 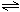 2SO2
+
O2
2SO2
+
O2
起始(mol) 20 0 0
转化(mol) 2x 2x x
平衡(mol) 20-2x 2x x
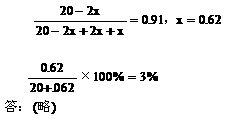
21.加热时N2O5依下式分解:
N2O5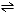 N2O3+O2;N2O3又依下式分解:
N2O3+O2;N2O3又依下式分解:
N2O3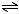 N2O+O2
N2O+O2
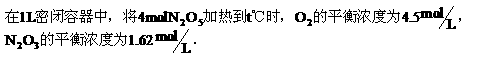
(1) t℃时N2O5和N2O的平衡浓度______mol/L.
(2)N2O5的分解率______%.
20.在一个密闭容器里 ,充入amolN2, bmolH2, cmolNH3, 当达到化学平衡时,平衡混合物中含有dmolNH3.
(1)当d>c时,该反应应表示为①______________,以H2浓度变化表示的反应速率是②___________,平衡时NH3的体积分数是③__________;起始压强与平衡压强的比值是④____________.
(2)当d<c时,该反应应表示为①____________,以H2的浓度变化表示的平均反应速率是②__________,平衡时NH3的体积分数是③______,起始压强与平衡压强的比值是④_____________.
19、(A)牙齿表面由一层硬的、组成为Ca5(PO4)3OH的物质保护着,它在唾液中存在下列平衡:
Ca5(PO4)3OH(固) 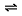 5Ca2++3PO43-+OH-
5Ca2++3PO43-+OH-
进食后,细菌和酶作用于食物,产生有机酸,这时牙齿就会受到腐蚀,其原因是
已知Ca5(PO4)3F(固)的溶解度比上面的矿化产物更小,质地更坚固。主动脉用离子方程式表示,当牙膏中配有氟化物添加剂后能防止龋齿的原因:
根据以上原理,请你提出一种其它促进矿化的方法:
18.某化学反应2A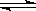 B+D在四种不同条件下进行,B、D起始浓度为见反应物A的浓度(mol/L)随反应时间(min)的变化情况如下表:
B+D在四种不同条件下进行,B、D起始浓度为见反应物A的浓度(mol/L)随反应时间(min)的变化情况如下表:
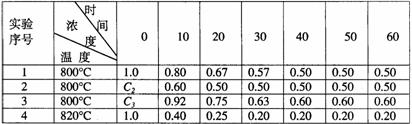
根据上述数据,完成下列填空:
(1)在实验1,反应在10至20分钟时间内平均速率为 mol/(L·min)。
(2)在实验2,A的初始浓度C2= mol/L,反应经20分钟就达到平衡,可推测实验2中还隐含的条件是 。
(3)设实验3的反应速率为V3,实验1的反应速率为V1,则V3 V1(填>、=、<且C3 1.0mol/L(填>、=、<=
(4)比较实验4和实验1,可推测该反应是 反应(选填吸热、放热)。理由是
17.氯化铁稀溶液加热时,颜色逐渐变深,最后析出红棕色沉淀.氯化铁稀溶液存在着水解平衡:FeCl3+3H2O Fe(OH)3+3HCl-Q
Fe(OH)3+3HCl-Q
①由于加热使平衡向_____反应方向移动,所以增大了____程度,使Fe(OH)3的量不断增多,最后Fe(OH)3沉淀而析出.
②若用水不断稀释,浑浊度增大,使水解平衡向_______反应方向移动.
③在配制FeCl3溶液时,为了抑制水解,常常加_______.
16. 可变的密闭容器中盛有适量N2、H2混合气体,在一定条件下反应 N2+3H2  2NH3,达到平衡时容积为VL,混合气体中氨占体积20%,若压强、温度保持不变,下列推论不正确的是
[ ]
2NH3,达到平衡时容积为VL,混合气体中氨占体积20%,若压强、温度保持不变,下列推论不正确的是
[ ]
A. 原N2、H2混合气体为100VL B. 原N2、H2混合气体为1.2VL
C. 参加反应的N2为0.1VL D. 原混合气体中N2、H2体积比为1:3
15. 在Na2PO4溶液中存在下列平衡:HPO42-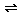 H++PO43-欲使溶液中的HPO42-、H+、 PO43-同时减少,可采取的方法有
[ ]
H++PO43-欲使溶液中的HPO42-、H+、 PO43-同时减少,可采取的方法有
[ ]
A. 加少量盐酸 B. 加入生石灰
C. 加入NaOH固体 D. 加入AgNO3溶液
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com