
题目列表(包括答案和解析)
25、铝粉是铝热焊剂的主要成分之一。在用99.9%纯度的铝锭制得的铝粉中,常含少量的三氧化二铝和二氧化硅。用气体容量法可以测定铝粉中金属铝(又称活性铝)的含量,其方法是:用盐酸或氢氧化钠溶液与样品作用,通过产生的氢气的体积计算样品中金属铝的含量。
(1)在盐酸和氢氧化钠溶液这两种试剂中,选用______较好,原因是_____________。
(2)根据你选用的试剂,写出测定过程的化学方程式 _________________。
(3)计算金属含量的基本公式是_____________________________。
(4)在常温常压下,按实测气体体积计算时,铝的百分含量往往比实际含量偏大,其原因_________________________________,为得到正确结果,应该 ________________。
24、一氯甲烷,也叫甲基氯,常温下是无色气体,密度为0.9159克/厘米3,熔点为-97.73℃,沸点为-24.2℃,18℃时在水中的溶解度为280毫升/毫升水,与乙醚、丙酮或苯互溶,能溶于乙醇。在实验室里可用下图装置制造一氯甲烷:
 制备装置的分液漏斗和烧瓶中分别盛有甲醇和浓盐酸。试填写下列空白:
制备装置的分液漏斗和烧瓶中分别盛有甲醇和浓盐酸。试填写下列空白:
(1)制备一氯甲烷的化学方程式____________,其反应类型属于___________反应;
(2)装置b的作用是_______________________;
(3)已知卤代烃能发生碱性水解,转化为醇。装置e中可能发生的反应方程式为____________;
(4)检验气体产物CH3Cl的方法是:在e的逸出口点燃CH3Cl气体,火焰呈蓝绿色(与其它烃燃烧现象有明显区别)。CH3Cl燃烧的化学方程式是____________________;
(5)实验中实际按甲醇和浓盐酸1︰2(物质量之比)进行反应的理由是_______________;
(6)某学生在关闭活塞x的情况下做此实验时发现,收集到一定体积的气体产物所消耗的甲醇-浓盐酸的混和液的量比正常情况下多(装置的气密性没有问题),其原因是_______________________________________________;
(7)实验结束后,d中收集到的液体中含有 ____________________________________。
23、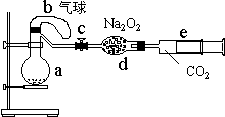 如下图的装置中:
如下图的装置中:
a是盛有标况下的空气(氧气占五分之一)和10毫升1.2mol/L硝酸的250毫升烧瓶。b是未充气(实验开始前内部没有气体)放有0.384克铜粉的气球。c是夹紧了的弹簧夹。d中盛有足量的过氧化钠。e是充有二氧化碳的针筒。整套装置已经过气密性检查合格。
(1)将气球中的铜粉小心倒入烧瓶中,充分反应后发现铜粉有余(设产生的气体不溶解于溶液中),则可观察到的是_______________________________。
(2)欲提高铜与硝酸反应的速度可采用多种不同的措施
①若用加入化学试剂法,下列试剂中可以使用的是(填代号)_____________ ;
A.蒸馏水 B .无水醋酸钠 C.石墨 D.硝酸银溶液(少量)
②将烧瓶不断振荡发现气球逐渐缩小,发生有关反应的化学方程式是 __________________,此时气球全在烧瓶外还是有一部分进入烧瓶?________________。
③打开弹簧夹将二氧化碳推入干燥管内继续振荡,使气体与气体、溶液充分接触,欲使所有的铜粉都溶解,至少需要推入二氧化碳_______________毫升。
④将上述全过程用一个总的化学方程式表示__________________________。
22、某学生为了测定由两种元素形成的气态化合物X的组成,做了如图所示的实验。他把气体X由注射器A缓慢送入装有CuO的B装置,使之完全反应,得到如下结果:

①实验前B管及药品的质量为21.32克,实验后为21.16克。
②C管中收集到的物质电解后得到H2和O2,在D中收集到的是N2。
③X中两元素的质量比是14︰3。
(1)C中收集到的液体,质量是______________克。
(2)在实验中看到的现象是 _________________。
(3)B中反应的化学方程式是 ____________________________。
21、下图中的几种仪器装置都可以制得氢气,其中:
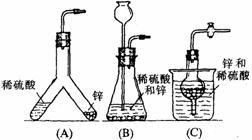
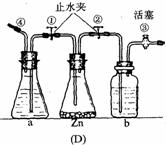
(1)能使发生或停止发生氢气操作均比较方便的装置是(写编号)_________,能够灌充升空的小氢气球的装置是____________。
(2)在(D)装置中a中的液体应是__________;b中的液体应是______________,其作用是___________________。
(3)使(D)装置发生氢气的操作顺序应该是_______________________。
20、从下列仪器、试剂中选用适当的用品进行简便的实验,证明浓硝酸比稀硝酸具有更强的氧化性,要求简要地叙述实验的方法和现象。
试剂:NaOH溶液、石蕊试液、酚酞试液、浓硝酸、稀硝酸、蒸馏水
用品:酒精灯、火柴、玻璃棒、试管、胶头滴管
______________________________________。
19.磷酸镁铵NH4MgPO4是一种重要的盐,难溶于水。化学上制备NH4MgPO4从反应原理看,是用氯化镁溶液、磷酸氢二钠的氨水混合反应的方法。写出制备磷酸镁铵反应的离子方程式__________________;而实际上在制备反应中,要向混合溶液中加入适量的铵盐(NH4+),请分析说明加入铵盐的目的是________________。
18、验证某有机物属于烃的含氧衍生物,应完成的实验内容是
A.只要验证它完全燃烧后产物只有H2O和CO2
B.只要测定其燃烧产物中H2O和CO2物质的量的比值
C.测定完全燃烧时消耗有机物与生成的CO2、H2O的物质的量之比
D.测定该试样的质量及其试样完全燃烧后生成CO2和H2O的质量
17.、以下仪器:①中和滴定实验用的锥形瓶 ②中和滴定实验用的滴定管 ③容量瓶 ④配制一定物质的量浓度的NaOH溶液用于称量的烧杯 ⑤测定硫酸铜晶体中结晶水含量用的坩埚,用蒸馏水洗净后便可立即使用而不会对实验结果造成误差的是
A.①和② B.①和③ C.①③⑤ D. ②④⑤
16.有人将浓度均为0.1mol/L的氨水和氯化铵溶液等体积混合对比混合液进行实验测定,来验证NH3·H2O的电离倾向大于NH4+的水解倾向,并设想出以下几个实验方案。这些方案中不科学、不合理的是①测定Cl-浓度 ②测定混合液的PH
③用滴定法测定NH4+的浓度 ④用滴定法测出氢氧根离子的浓度
A.①③④ B.只有① C.只有② D.全部
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com