
题目列表(包括答案和解析)
28、(12分) 以石墨为电极,电解1LCuSO4和NaCl的混合溶液,其中CuSO4与NaCl的物质的量之和为0.2mol,CuSO4的物质的量占总物质的量的比值为x。
(1)x=0.5,当Cu2+在阴极恰好全部析出时,产生的气体是什么?物质的量为多少?所得溶液的pH值为多少?(忽略溶液体积的变化)
(2)电解一段时间后,阴、阳极产生气体的物质的量恰好相等,均为0.16mol,试求x值。
27、(8分)将10.08g铁粉溶于过量的稀硫酸,所得溶液加入5.05gKNO3氧化溶液中的Fe2+,待反应完毕后,剩余的Fe2+尚需30ml 0.5mol/L的溴水才能全部氧化,试写出三步反应的化学方程式。
26、(12分)、已知浓硫酸与木炭粉在加热条件下反应生成SO2、CO2和H2O。试用下图所列各装置设计一个实验,来验证上述反应所产生的各种产物。
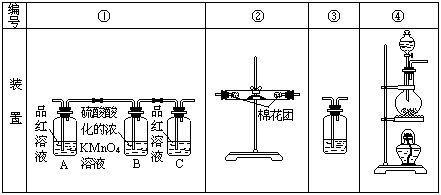 (1)这些装置的连接顺序(按产物气流从左至右的方向)是(填装置的编号):
(1)这些装置的连接顺序(按产物气流从左至右的方向)是(填装置的编号):
→ → → 。(3分)
(2)实验时可观察到装置①中A瓶的溶液褪色,C瓶的溶液不褪色.A瓶溶液的作用是 ;B瓶溶液的作用是 ;C瓶溶液的作用是 。(3分)
(3)装置②中所加的固体药品是 ,可验证的产物是 ,确定装置②在整套装置中位置的理由是 。(4分)
(4)装置③中所盛溶液是 ,可验证的产物是 。(2分)
25、 (10分)、A、B、C和D分别是NaNO3、NaOH、HNO3和Ba(NO3)2四种溶液中的一种.现利用另一种溶液X,用如下图所示的方法,即可将它们一一确定.试确定A、B、C、D、X各代表何种溶液.
(10分)、A、B、C和D分别是NaNO3、NaOH、HNO3和Ba(NO3)2四种溶液中的一种.现利用另一种溶液X,用如下图所示的方法,即可将它们一一确定.试确定A、B、C、D、X各代表何种溶液.
A: B: C: D: X:
24、(10分).A+、B+、C-、D、E五种微粒(分子或离子),每个微粒均含有10个电子.已知 ①A++C- D+E↑ ②B++C-
D+E↑ ②B++C- 2D
2D
请回答以下问题:
(1)C-的电子式为____________
(2)具有相同空间构型的微粒是______和________
(3)分别写出A+和D反应,B+和E反应的离子方程式。
A++D:_______________________ B++E:________________________
23、 (6分)、按要求回答下列问题
(6分)、按要求回答下列问题
(1)金刚石晶体中含有共价键形成的C原子环,其中最小的C环上有 个C原子。
(2)NaCl晶体中每个Na+周围有 个Cl-,每个Na+周围与它最近且距离相等的Na+共有 个。
(3) 观察干冰晶体结构,试分析:与二氧化碳分子距离最近且相等的二氧化碳分子有______个。
(4)NH3分子的空间结构为 ,当结合H+后,形成的NH4+离子的空间结构为 。
22、(7分)铁酸钠(Na2FeO4)是水处理过程中使用的一种新型净水剂,已知它的氧化性强于KMnO4,在反应中本身被还原为Fe3+,将它溶入浑浊的泥水中,既能起杀菌消毒作用,又能使泥浊沉降,试回答:
(1)配平制取铁酸钠的反应方程式:
_ _Fe(NO3)3+_ __NaOH+_ _Cl2-_ _Na2FeO4+_ _NaNO3+_ _NaCl+_ _H2O
该反应中的还原产物是___ _。
(2)铁酸钠能沉降泥浊的原因是_______________ __ ___。
21、(10分)(1)卫星发射时可用肼(N2H4)为燃料,1 gN2H4(气态)在O2(气态)中燃烧,生成N2(气态)和H2O(气态),放出16.7kJ的热量,写出有关的热化学方程式
。
(2)氢氧化钡溶液中通入足量的CO2气体,写出其离子方程式 。(3)18g普通水(H2O)和40g重水(D2O)分别与足量的金属钠反应,在同温同压下产生气体的体积比______,质量比______,消耗金属钠的质量比_______。
20、已知同周期X、Y、Z三种元素的最高价氧化物的酸性由强到弱的顺序是HXO4>H2YO4>H3ZO4,则 ( )
A.元素的非金属性按X、Y、Z的顺序增强
B.单质的氧化性按X、Y、Z的顺序减弱
C.阴离子的还原性按X、Y、Z的顺序减弱
D.气态氢化物的稳定性按X、Y、Z的顺序减弱
19、A,B,C分别代表3种不同的短周期元素,A元素原子的最外层只有2个电子,B元素原子的M电子层上的电子数比电子层数的2倍多1个,C元素原子核内有8个质子, 则这3种元素组成的化合物的化学式不可能是 ( )
A、ABC3 B、A(BC4)2 C、A(BC3)2 D、A(BC2)2
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com