

题目列表(包括答案和解析)
3.A、B、C、D是四种人们熟悉的与生命运动密切相关的化合物,它们所含的元素不超过三种,并有下列关系(反应条件均未注明)
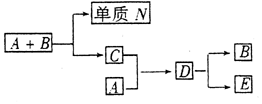
目前化合物B在自然界含量呈上升趋势,对环境产生了不利影响,E是一种生活中常见的化合物,在一定条件下可与单质N进一步发生如下变化:E+3N→3A+2B (1)A、B、C、D分别是什么物质,常温下,A和B转化为C的途径是什么? (2)假设在上述转化中无损耗,如有0.1molE生成,求A和B转化为C时能产生多少克单质N?
2.A、B、C、D、E、F是中学化学中常见的六种物质,它们之间有如下转化关系:其中B、D在通常情况下是气体物质,F溶液呈强碱性。
 (1)写出C的化学式_____________。
(2)写出反应①的化学方程式________________________。
(3)配制F溶液时必须注意:①_____________;②____________;③ (“ ”有示有则填写,无则不填写)
(4)写出F与盐酸反应的离子方程式______________________。
(1)写出C的化学式_____________。
(2)写出反应①的化学方程式________________________。
(3)配制F溶液时必须注意:①_____________;②____________;③ (“ ”有示有则填写,无则不填写)
(4)写出F与盐酸反应的离子方程式______________________。
1.下列关系中,A是一种正盐,D的分子量比C的分子量大16,E是酸;当X无论是强碱还是强酸时都有如下转化关系:
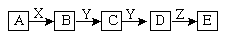 当X是强酸时,A、B、C、D、E均含同一种元素;当X是强酸时,A、B、C、D、E均同时含有另一种元素。
回答下列问题:(用化学式填写)
(1)A是________,Y是_________,Z是_________。
(2)当X是强碱时,B是__________,C是_________,D是__________,E是_________。
(3)当X是强酸时,B是__________,C是_________,D是_________, E是_________。
(4)写出A与X反应的离子方程式:
①_______________________________________________。
②_______________________________________________。
当X是强酸时,A、B、C、D、E均含同一种元素;当X是强酸时,A、B、C、D、E均同时含有另一种元素。
回答下列问题:(用化学式填写)
(1)A是________,Y是_________,Z是_________。
(2)当X是强碱时,B是__________,C是_________,D是__________,E是_________。
(3)当X是强酸时,B是__________,C是_________,D是_________, E是_________。
(4)写出A与X反应的离子方程式:
①_______________________________________________。
②_______________________________________________。
3.假设思维模式是由题设条件和转化关系图找出题目突破口,并对有关内容建立假设,然后将假设结果代入题中验证分析,由此可使问题得以解决。假设模式的思维途径可表示为:

例3.下图①-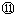 分别代表反应中的一种物质,请填空白:
分别代表反应中的一种物质,请填空白:
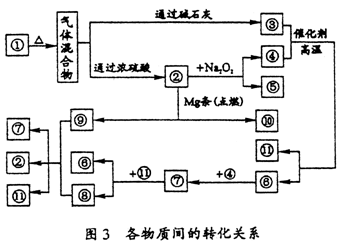 (1)①、③、④的化学式分别是_______。
(2)⑧与⑨反应的化学方程式是________。
分析:由题设条件“物质①受热分解得气体混合物”可判断①可能为浓HNO3或不稳定酸的铵盐等。常见的不稳定酸的铵盐有NH4HCO3,(NH4)2CO3,NH4HSO3等。假设①为NH4HCO3,则气体混合物将为NH3,CO2,H2O蒸气,代入题中可推知③为NH3,④为O2,②为CO2;又由转化关系可推知⑥为NO,⑦为NO2,⑧为HNO3,⑨、⑩一种为MgO,一种为C,因⑧⑨反应生成三种产物,则⑨为C。以上结果都是符合题意的,可见假设①为NH4HCO3是成立的。同理(NH4)2CO3亦合题意。故参考答案为(1)①--NH4HCO3[(NH4)2CO3];③--NH3;④--O2;(2)C+4HNO3===2H2O+4NO2↑+CO2↑
(1)①、③、④的化学式分别是_______。
(2)⑧与⑨反应的化学方程式是________。
分析:由题设条件“物质①受热分解得气体混合物”可判断①可能为浓HNO3或不稳定酸的铵盐等。常见的不稳定酸的铵盐有NH4HCO3,(NH4)2CO3,NH4HSO3等。假设①为NH4HCO3,则气体混合物将为NH3,CO2,H2O蒸气,代入题中可推知③为NH3,④为O2,②为CO2;又由转化关系可推知⑥为NO,⑦为NO2,⑧为HNO3,⑨、⑩一种为MgO,一种为C,因⑧⑨反应生成三种产物,则⑨为C。以上结果都是符合题意的,可见假设①为NH4HCO3是成立的。同理(NH4)2CO3亦合题意。故参考答案为(1)①--NH4HCO3[(NH4)2CO3];③--NH3;④--O2;(2)C+4HNO3===2H2O+4NO2↑+CO2↑
例4.图4里每一方程中的字母代表一种反应物或生成物。
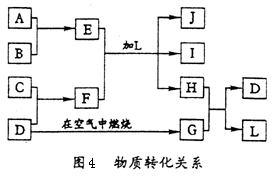 产物J是含A金属元素的胶状白色沉淀,I为NaCl溶液,D是淡黄色固体单质。试填写下列空白:
(1)L的化学式为:__________。
(2)F的化学式为:__________。
(3)写出J受热分解反应的化学方程式:_______。
(4)H和G之间反应的化学方程式为:________。
解析:本题的切入点是物态:J为含A金属元素的胶状白色沉淀,D为淡黄色固体单质。推测J为Al(OH)3,D为S,A为Al,E为Al的化合物。
E+F
产物J是含A金属元素的胶状白色沉淀,I为NaCl溶液,D是淡黄色固体单质。试填写下列空白:
(1)L的化学式为:__________。
(2)F的化学式为:__________。
(3)写出J受热分解反应的化学方程式:_______。
(4)H和G之间反应的化学方程式为:________。
解析:本题的切入点是物态:J为含A金属元素的胶状白色沉淀,D为淡黄色固体单质。推测J为Al(OH)3,D为S,A为Al,E为Al的化合物。
E+F  Al(OH)3↓+NaCl+H
(J) (I)
F为S的化合物,结合产物Al(OH)3,容易想到该反应是Al3+与S2-的双水解反应,L为H2O,H为H2S。再结合:D(S)
Al(OH)3↓+NaCl+H
(J) (I)
F为S的化合物,结合产物Al(OH)3,容易想到该反应是Al3+与S2-的双水解反应,L为H2O,H为H2S。再结合:D(S)  G(SO2)及H(H2S)+G(SO2)→D(S)+L(H2O)可知上面的推测是合理的。
反过来可确定E,F。
E(Al的化合物)+F(S的化合物)
G(SO2)及H(H2S)+G(SO2)→D(S)+L(H2O)可知上面的推测是合理的。
反过来可确定E,F。
E(Al的化合物)+F(S的化合物) 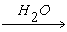 Al(OH)3↓+NaCl+H2S↑
F应为Na2S,E为AlCl3。进而可推B为Cl2,C为Na。
答案:(1)H2O
(2)Na2S
(3)2Al(OH)3
Al(OH)3↓+NaCl+H2S↑
F应为Na2S,E为AlCl3。进而可推B为Cl2,C为Na。
答案:(1)H2O
(2)Na2S
(3)2Al(OH)3 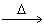 Al2O3+3H2O
(4)2H2S+SO2=3S+2H2O
Al2O3+3H2O
(4)2H2S+SO2=3S+2H2O
2.有的推断题,最初条件意义并不明确,但某一结果有较明确的含义,求解时,从这一结果入手,采用逆推模式,逆向逐层推理,可顺利达到解决问题的目的。
例2.提示:某些金属氧化物跟熔融烧碱反应可生成盐,根据图2化学反应方框图填空:
 (1)单质F是________;
(2)写出由E生成G的离子方程式(或化学方程式)_______;
(3)溶液I中所含金属离子是________;
(4)由C
(1)单质F是________;
(2)写出由E生成G的离子方程式(或化学方程式)_______;
(3)溶液I中所含金属离子是________;
(4)由C 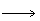 E+F若改用浓酸,则不能选用的浓酸是(写分子式)________。
分析:从题设最初条件看,其意义并不明确,但从转化关系方框图中的结果“红褐色沉淀G”可知,其含义明确,故从此入手运用逆推。由红褐色沉淀G逆推可知溶液E中含Fe2+,再由E逆推知单质C为Fe,单质F为H2;又由单质F(H2)逆推知单质B可为金属Al或Zn或者为非金属单质Si,另由溶液I加NH3·H2O转化为沉淀J,J溶于强碱溶液,可确定单质B为Al,化合物A为铁的氧化物。故参考答案为:
(1)H2;
(2)4Fe2++8NH3·H2O+O2+2H2O===4Fe(OH)3↓+8NH
E+F若改用浓酸,则不能选用的浓酸是(写分子式)________。
分析:从题设最初条件看,其意义并不明确,但从转化关系方框图中的结果“红褐色沉淀G”可知,其含义明确,故从此入手运用逆推。由红褐色沉淀G逆推可知溶液E中含Fe2+,再由E逆推知单质C为Fe,单质F为H2;又由单质F(H2)逆推知单质B可为金属Al或Zn或者为非金属单质Si,另由溶液I加NH3·H2O转化为沉淀J,J溶于强碱溶液,可确定单质B为Al,化合物A为铁的氧化物。故参考答案为:
(1)H2;
(2)4Fe2++8NH3·H2O+O2+2H2O===4Fe(OH)3↓+8NH
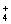 或Fe2++2NH3·H2O====Fe(OH)2↓+2NH
或Fe2++2NH3·H2O====Fe(OH)2↓+2NH
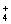 ;
4Fe(OH)2+O2+2H2O===4Fe(OH)3;
(3)Al3+和Na+;
(4)H2SO4或HNO3
;
4Fe(OH)2+O2+2H2O===4Fe(OH)3;
(3)Al3+和Na+;
(4)H2SO4或HNO3
1.顺推是根据题设条件和转化关系方框图,从最初反应物入手,利用给定反应物的结构和性质特点,顺着转化关系往后推,从而解决问题。
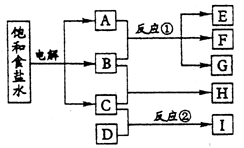
例1.图1每一方框中的字母代表一种反应物或生成物:

附表 各物质的量
|
C D 1 |
|
起始组成/mol 6 4 0
某时刻组成/mol 3 3 2 |
物质A跟B反应生成物E、F和G,物质C跟D反应生成物质I,某温下该反应起始和某时刻的反应混合物组成如附表所示。请填写下列空白:(1)物质H的分子式_______;(2)反应①的化学方程式_______;(3)反应②的化学方程式(须注明反应条件)是________。
分析:本题首先给出饱和食盐水的电解,然后是电解产物间的作用。最初条件意义清楚,故进行顺推。饱和食盐水的电解产物是Cl2、H2、NaOH,其中两两反应可生成三种产物的是Cl2、NaOH中的一种,C为H2,又B、C作用生成H物质,则B为Cl2,A为NaOH,H为HCl。又由表中数据推知C、D、I三种物质在方程式中的系数比为(6-3)∶(4-3) ∶(2-0)=3∶1∶2,因C为H2,则D为N2,I为NH3。故参考答案为(1)HCl;
(2)Cl2+2NaOH=NaCl+NaClO+H2O;
(3)3H2+N2 2NH3
2NH3
21.(10分)在一定条件下,某元素的氢化物X可完全分解为两种单质:Y和Z。若已知:
①反应前的X与反应后生成的Z的物质的量之比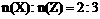
②单质Y的分子为正四面体构型。
请填写下列空白。
(1)单质Y是___________,单质Z是___________(填写名称或分子式)。
(2)Y分子中共含___________个共价键。
(3)X分解为Y和Z的化学方程式为:______________________。
答案:(1)白磷(或 ),氢(或
),氢(或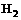 (3分)
(3分)
(2)6 (3分)
(3)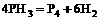 (4分)
(4分)
(6分)若以X、Y和Z代表三种元素,且知X与Y可形成原子数之比为1︰1的化合物甲,Y与Z也可形成原子数之比为1︰1的化合物乙,又知甲分子含18个电子,乙分子含38个电子,请填空:
(1)元素Y在第 周期。
(2)化合物甲的分子式是 。
(3)化合物乙的分子式是 。
答案:(6分)
(1) 第二周期(2)H2O2(3)Na2O2
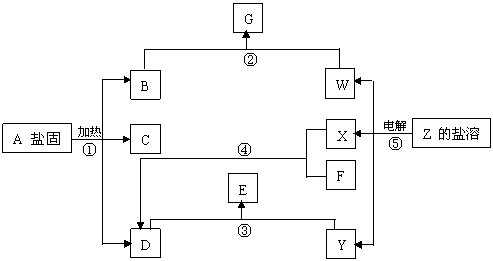 (11分)
(11分)
在一定条件下(不许添加别的反应物),经不同的化学反应,可实现如上图的各种变化。其中,反应③、④、⑤属氧化还原反应,而反应①、②属非氧化还原反应。X、F和Y为单质,且F是空气的主要成分之一,其余为化合物,据此请填空:
(1)物质A是 ,F是 ,X是 ,Y是 。
(2)写出反应②的化学方程式 。
(3)写出反应④的化学方程式 。
答案:(11分)
(1)A是(NH4)2CO3(或NH4HCO3),F是N2,X是H2,Y是Cl2。
 (2)CO2+2NaOH=Na2CO3+H2O(或CO2+NaOH=NaHCO3)
(2)CO2+2NaOH=Na2CO3+H2O(或CO2+NaOH=NaHCO3)

(3)N2+3H2 2NH3
2NH3
10分)
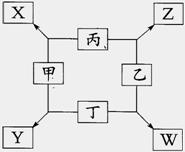
如图所示已知:
①甲、乙、丙、丁均为前三周期元素的单质。
②在一定条件下甲与丙和甲与丁都按物质的量之比1︰3反应,分别生成X和Y,在产物中元素甲呈负价。
③在一定条件下乙与丙和乙与丁都按物质的量之比1︰2反应,分别生成Z和W,在产物中元素乙呈负价。
请填空:
(1)甲是 ,乙是 。
(2)甲与丙反应生成X的化学方程式是
(3)乙与丁反应生成W的化学方程式是
利用天然气合成氨的工艺流程示意如下:
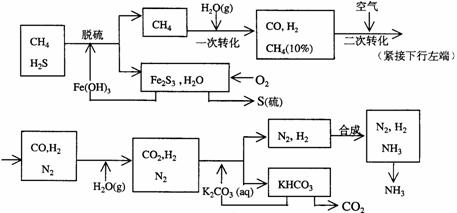
依据上述流程,完成下列填空:
(1)天然气脱硫时的化学方程式是
(2)n mol CH4经一次转化后产生CO 0.9n mol、产生H2 mol(用含n的代数式表示)
(3)K2CO3(aq)和 CO2反应在加压下进行,加压的理论依据是 (多选扣分)
(a)相似相溶原理 (b)勒沙特列原理 (c)酸碱中和原理
(4)由KHCO3分解得到的CO2可以用于 (写出CO2的一种重要用途)。
(5)整个流程有三处循环,一是Fe(OH)3循环,二是K2CO3(aq)循环,请在上述流程图中标出第三处循环(循环方向、循环物质)。
答案:(本题共12分)
(1)3H2S+2Fe(OH)3→Fe2S3+6H2O(2分)
(2)27n(3分)
(3)b(3分)
(4)生产纯碱(或作制冷剂等,其它合理答案也给分)(2分)
(5)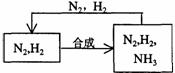 (2分)
(2分)
(12分)室温下,单质A,B,C分别为固体、黄绿色气体、无色气体,在合适反应条件下,它们可以按图2进行反应。又知E溶液是无色的,请回答:
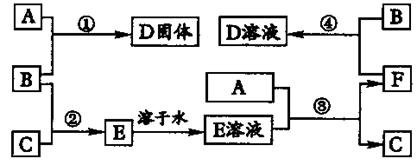
图2 反应流程
(1)A是 、B 是、C是 (请填化学式)。
(2)反应①的化学方程式为: 。
(3)反应③的化学方程式为: 。
(4)反应④的化学方程式为:
。
答案:(1)Fe
Cl2 H2 (2)2Fe+3Cl2 2FeCl3
2FeCl3
(3)2HCl+Fe=FeCl2+H2↑
(4)2FeCl2+Cl2=2FeCl3
(7分)甲、乙、丙、丁分别是盐酸、碳酸钠、氯化钙、硝酸银4 种溶液中的一种。将它们两两混合后,观察到的现象是:①甲与乙或丙混合都产生沉淀;②丙与乙或丁混合也产生沉淀;③丁与乙混合产生无色气体。回答下面问题:
(1)写出丁与乙反应的离子方程式: 。
(2)这四种溶液分别是:甲: 、乙: 、丙: 、丁: 。
答案:(1)2H++CO32-=H2O+CO2↑
(2)甲:氯化钙、乙:碳酸钠 、丙:硝酸银、丁:盐酸 (或写化学式)。
(6分)下图中①-⑾分别代表有关反应中的一种物质,请填写以下空白。(1)①、③、④的化学式分别是_____、_____、_____。 (2)⑧与⑨反应的化学方程式是_____。 答案:(1)NH4HCO3; NH3; O2
(2)C+4HNO3=2H2O+4NO2↑+CO2↑
4、2NH4++SO42-+Ba2++2OH-=BaSO4↓+2NH3↑+2H2O。
[例3]A,B,C是在中学化学中常见的三种化合物,它们各由两种元素组成,甲、乙是两种单质。这些化合物和单质之间存在如图1所示的关系。
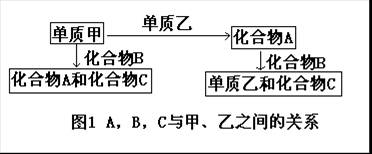
由此判断:
(1)在A,B,C三种化合物中,必定含有乙元素的是_________(用A,B,C字母填写)。
(2)单质乙必定是________(填“金属”或“非金属”),其理由是________。
(3)单质乙的分子式可能是_________。则化合物B的分子式是___________。
[解析]本题主要考查思维能力,包括逻辑思维和发散思维的能力等。
(1)题中指出,A,B,C都是由两种元素组成的化合物,因此由:单质甲+单质乙→化合物A,可知化合物A中肯定含有乙元素。由:单质甲+化合物B→化合物A+化合物C,可知化合物B中也肯定含有乙元素(因为化合物A中的乙元素只能来自化合物B)。
但是化合物C中是否含有乙元素则是不能确定的,我们从2H2S+SO2=3S↓+2H2O的反应中可以看出化合物C中不含乙元素,我们从PbO2+H2O2=O2↑+PbO+H2O的反应中可以看出,反应的两种生成物中仍含有氧元素。所以(1)小题的答案为A,B。
(2)我们知道,金属元素在化合物中只显正价,而非金属元素在化合物中可显正价也可显负价。在反应化合物A+化合物B→单质乙+化合物C中,由于A,B都含有乙元素,反应之后有单质乙生成。这说明A,B两种化合物中必有一种乙元素显正价,另一种乙元素显负价。如果两种化合物中乙元素都显正价或负价,则不可能反应生成显零价的单质。所以(2)小题的答案是:乙必定是非金属。
(4) 回答本小题要求元素及其化合物知识十分熟悉,而且要习惯于发散思维,要注意寻找发散思维的出发点。本题中就应该从两种含有相同元素的化合物(其中一个该元素显正价,另一个显负价)发生反歧化反应,生成该元素单质作为思维的出发点,立足于这一点就可能想到反应:2H2S+SO2=3S↓+2H2O。
还可能想成:4NH3+6NO
 5N2+6H2O,将这几种物质放到所给出的反应关系中去试验,就可得出(3)小题的答案为单质甲可能是O2,单质乙可能是S(或N2);A可能是SO2(或NO);B可能是H2S(或NH3);C则是H2O。
5N2+6H2O,将这几种物质放到所给出的反应关系中去试验,就可得出(3)小题的答案为单质甲可能是O2,单质乙可能是S(或N2);A可能是SO2(或NO);B可能是H2S(或NH3);C则是H2O。
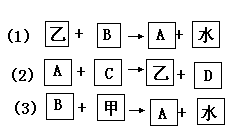 [例4]今有甲、乙两种固体物质,已知其中之一为氧化镁;另有A、B、C、D 4种无色溶液分别为氢氧化钠溶液、硝酸镁溶液、硝酸钠溶液和稀硝酸中的某一种,它们之间的相互关系如图表示:
[例4]今有甲、乙两种固体物质,已知其中之一为氧化镁;另有A、B、C、D 4种无色溶液分别为氢氧化钠溶液、硝酸镁溶液、硝酸钠溶液和稀硝酸中的某一种,它们之间的相互关系如图表示:
试判断:A、B、C、D各是什么溶液(用化学式表示)?甲、乙各是什么物质?
[解析]本题6种物质的名称均未确定,且甲、乙均可能为MgO,不妨设甲为MgO,参照试题提供的反应线索论证,可使此题错综复杂的关系变得明朗,从而使各物名称逐一确定。若甲为MgO,则甲与B反应生成A和H2O,可推知A是Mg(NO3)2,B是稀硝酸(因MgO是碱性氧化物,与硝酸反应生成硝酸盐和水)。然后,以B(HNO3)这个已确定物质为起点,结合(1)并知A为Mg(NO3)2,运用反应规律推知乙为Mg(OH)2。C不可能为MgO,因已假定甲为MgO,由于A、乙名称已确定,结合(2)和无机物相互反应规律,不难推知C必为NaOH,D为NaNO3了。
当然,也可假定乙为MgO,但在按上述框图推新时,会产生假设与反应事实相矛盾的结果,故乙为MgO的假设不成立。 所以本题的正确答案是:A是Mg(NO3)2溶液,B是HNO3,CNaOH溶液,D是NaNO3溶液,甲为MgO,乙为Mg(OH)2。
[例5]从某物质A的水溶液出发,有下图所示的一系列变化(参加反应或反应生成的水没有标出)。
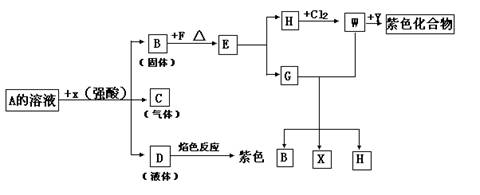
(1)写出下列物质的名称:H___________,G__________,W___________。
(2)写出A+X→B+C+D的化学方程式_____________。
(3)写出G+W→B+X+H的化学方程式_____________。
[解析]此题涉及无机、有机化学多方面的知识点,它是突破口极为隐蔽也极易出错的难度较大的综合推断题。乍看此题,有两个切入口:①焰色反应D为紫色(含K+),
②W+Y→紫色化合物(含苯酚络离子[Fe(C6H5O)6]3-)逆向追踪,A可能为钾盐,是什么钾盐,茫茫然难以确定。若假设为KHSO3和KHCO3,而加X(强酸)生成产物分别为固、液、气三态的B、C、D,不可能(与反应事实不符)。满足此条件的化合物A必为K2S2O3,与强酸反应生成物;S(固态)、SO2(气体)、KCl+H2O(液体)。但B(硫)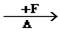 E,无法确定,至此,正向思维的线
E,无法确定,至此,正向思维的线
索中断。此时应倒过来思考:以紫色化合物为起点倒推W是什么。在中学化学中紫色化合物只有三价铁的苯酚络离子[Fe(C6H5O)6]3-,故推断W为Fe3+,Y则为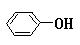 。继而逆推H为Fe2+,联系B→E的变化,E只能是FeS,才可能是FeS+2HCl=FeCl2+H2S↑,故H为FeCl2,2FeCl2+Cl2=2FeCl3(W)。解答本题的关键在于选准A和紫色化合物两个题眼(突破口)运用正、逆向思维和“两头堵”--双向进逼的方法破译如此极为隐蔽的“密码”。解码的武器是掌握硫、铁两章知识网络、有关络合物知识,培养统摄知识的能力。
。继而逆推H为Fe2+,联系B→E的变化,E只能是FeS,才可能是FeS+2HCl=FeCl2+H2S↑,故H为FeCl2,2FeCl2+Cl2=2FeCl3(W)。解答本题的关键在于选准A和紫色化合物两个题眼(突破口)运用正、逆向思维和“两头堵”--双向进逼的方法破译如此极为隐蔽的“密码”。解码的武器是掌握硫、铁两章知识网络、有关络合物知识,培养统摄知识的能力。
所以本题的正确答案为:(1)H:Fe2+ ,G:H2S,W:FeCl3。
(2)Na2S2O3+2HCl=2NaCl+S↓+SO2↑+H2O
(3)H2S+2FeCl3=S↓+2HCl+2FeCl2
附:近几年高考推断及框图题
99’.(8分)提示:某些金属氧化物跟熔融烧碱反应可生成盐。根据以下化学反应框图填空:
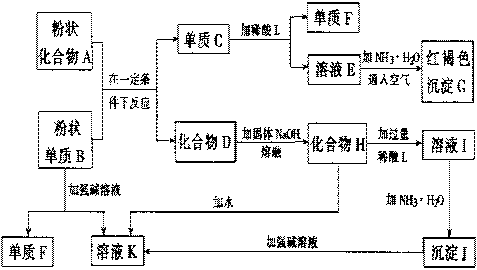
(1)单质F是_____________________。 (2)写出由E生成G的离子反应方程式(或化学方程式)________________________。 (3)溶液I中所含金属离于是_____________________。 (4)由CEF若改用浓酸,则不能选用的浓酸是(写分子式)____________________。
答案:(1)H2 (2)4Fe2++8NH3·H2O+O2+2H2O=4Fe(OH)3↓+8NH4+或Fe2++2NH3·H2O=Fe(OH)2↓+2NH4+ 4Fe(OH)2+O2+2H2O=4Fe(OH)3 (3)Al3+和Na+ (4)H2SO4(或HNO3) (每空2分,共8分) (2000’天津江西卷--25)(9分)下图每一方框中的字母代表一种反应物或生成物:
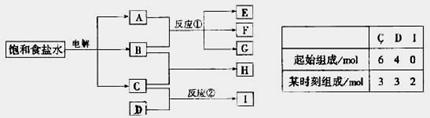
物质A跟B反应生成物质E、F和G;物质C跟D反应生成物质I,某温度下该反应起始和某时刻的反应混合物组成如右上表格所示。请填写下列空白:
(1) 物质H的分子式是___________。
(2) 反应①的化学方程式是________________________。
(3) 反应②的化学方程式(须注明反应条件)是_______________。
答案:(1)HCl (2分)
(2)Cl2+2NaOH?NaCl+NaClO+H2O (2分)
(3)N2+3H2 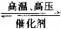 2NH3(化学方程式3分,反应条件2分)
2NH3(化学方程式3分,反应条件2分)
3、Ba2++CO32-=BaCO3↓, BaCO3+2H+=Ba2++CO2↑+H2O;
2、2Al3++3CO32-+3H2O=2Al(OH)3↓+3CO2↑;
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com