
题目列表(包括答案和解析)
1、下列六种工业生产:①用海水为原料制镁② 制硅酸盐水泥 ③ 制普通玻璃 ④ 冶炼生铁 ⑤制漂白粉 ⑥接触法制硫酸,用石灰石作为一种原料的是
A ①②③④⑤ B ②③④⑤⑥ C ①②③⑤⑥ D ①②③④⑤⑥
15.有一混合液可能由NaOH、NaHCO3、Na2CO3中的一种或两种组成。现取等体积的两份上述溶液分别以酚酞和甲基橙为指示剂,用同样浓度的盐酸进行滴定,当达到滴定终点时,消耗盐酸的体积分别为V1mL和V2mL,如V1<V2<2V1,则上述溶液中的溶质是
A NaHCO3 B Na2CO3 C Na2CO3、NaHCO3 D Na2CO3、NaOH
阳泉一中高考化学复习单元过关-《电离平衡》
班级 姓名 成绩
14.在相同温度下,等体积等物质的量的浓度的4种稀溶液:①Na2SO4、②H2SO4、③NaHSO4、④Na2S中所含带电微粒数由多到少的顺序是
A ①=④>③=② B ④=①>③>②
C ①>④>③>② D ④>①>③>②
13.在等物质的量浓度的两种弱酸的钠盐(NaR、Na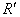 )溶液中分别通入适量的CO2,发生如下反应: NaR+CO2+H2O=HR+NaHCO3
)溶液中分别通入适量的CO2,发生如下反应: NaR+CO2+H2O=HR+NaHCO3
2Na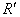 +CO2+H2O==2H
+CO2+H2O==2H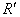 +Na2CO3
+Na2CO3
把HR和H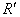 在水中电离出H+的能力作比较,正确的判断是
在水中电离出H+的能力作比较,正确的判断是
A HR较强 B H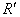 较强 C 两者相同 D 无法比较
较强 C 两者相同 D 无法比较
12.将0.2mol/LCH3COOK与0.1mol/L盐酸等体积混合,溶液中下列微粒物质的量的浓度关系正确的是
A [CH3COO-]=[Cl-]=[H+]>[CH3COOH]
B [CH3COO-]>[Cl-]>[CH3COOH]> [H+]
C [CH3COO-]>[Cl-]>[H+]>[CH3COOH]
D [CH3COO-]+[Cl-]+[OH-]=[H+]+[K+]
11. 设NA为阿伏加德罗常数,下列说法正确的是
A 1L0.1mol/L的Na2CO3溶液中,含Na+0.2 NA个,CO32-0.1 NA个
B 1L0.3mol/L的K2SO4溶液中,含K+和SO42-离子总数为0.9 NA个
C 2L0.6mol/L的Fe2(SO4)3溶液中,含SO42-离子总数为2.4 NA个
D 0.1mol/L的H3PO4溶液中,[H+]∶[PO43-]<3∶1
10.某酸的酸式盐NaHY在水溶液中,HY-的电离度小于HY-的水解程度。有关的叙述中,正确的是
A H2Y在电离时为:H2Y+H2O HY-+H3O+
HY-+H3O+
B 在该盐的溶液中,离子浓度为:(Na+)>(Y2-)>(HY-)>(OH-)>(H+)
C 在该盐的溶液中,离子浓度为:(Na+)>(HY-)>(OH-)>(H+)
D HY-的水解方程式为:HY-+ H2O H3O++Y2-
H3O++Y2-
9.25℃时将水不断滴入0.1mol/L的氨水中,下列变化的图象合理的是
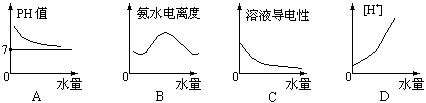
8.在25℃时,浓度均为1 mol·L-1 的(NH4)2SO4、(NH4)2CO3、(NH4)2Fe(SO4)2(硫酸亚铁铵)三种溶液中,测得其中[NH4+]分别为 a、b、c(mol/L),则下列判断正确的是
A a>b>c B c>a>b C b>a>c D a>c>b
7.在相同温度下,在水中分别加入下列物质,若用Kw表示水的离子积,α表示水的电离度,则能使α/Kw值增大的是
A Na2CO3 B NaHSO4 C NaOH D AI2(SO4)3
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com