
题目列表(包括答案和解析)
37.在碘化钾和硫酸的混合溶液里,加入过氧化氢(H2O2),放出大量不溶于水的无色气体(现象是从溶液内部析出大量的小气泡),同时溶液呈现红棕色,可使淀粉变蓝。用化学反应方程式说明发生此现象的原因______________。
36.将0.1mol铁粉和0.05mol硫粉均匀混合后,铺在石棉网上加热引燃,完全反应后,将残渣全部放入过量的稀H2SO4中充分反应。结果所产生的气体的体积在标准状况下明显少于2.24L,其主要原因是_______________。
35.A、B、C是常见的三种化合物,各由两种元素组成,转化关系如下图。

(1)在A、B、C中,必定含有乙元素的是_______。
(2)单质乙必定是_________(填“金属”或“非金属”);其理由是_________________。
(3)单质乙的分子式可能是________,则化合物B的分子式为____________。
34.说明:某金属氧化物跟熔融烧碱反应可生成盐。根据以下化学反应框图填空:
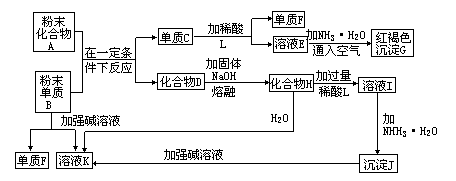
(1)单质F是_________。
(2)写出由E生成C的离子反应方程式(或化学方程式)_______________________________________________
________________________。
(3)溶液I中所含的金属离子是___________________。
(4)由C-→E+F,若改用浓酸,则不能选用的浓酸是(写分子式)_________________________。
33.已知硫粉跟亚硫酸钠溶液共热可制得硫代硫酸钠。现以硫化亚铁为主要原料,按下图制取硫代硫酸钠。图中A、B、C、D是硫单质或硫的化合物,其它不含硫的反应物已被略去,各步反应可以添加必要的试剂。

(1)反应(I)的化学方程式为___________。
(2)D的分子式为____________,硫代硫酸钠的分子式为_______________。
(3)硫代硫酸钠与稀H2SO4反应生成C,反应的离子方程式为_______________。
32.甲、乙、丙、丁4种化合物都是由短周期元素A、B、C、D、E中的两种元素组成。在常温常压下,甲为气体,乙为液体,丙和丁为固体。元素A、B、C、D、E的原子序数依次增大, A、D同主族, B、 E同主族,B、C同周期。甲是由A、 C组成,原子个数比为1∶1;乙是由A、B组成,原子个数比为1∶1;丙是由B、D组成,丙是1种强氧化剂,可以用来漂白织物等;丁是由D和E组成的离子化合物,阴离子比阳离子多1个电子层。由此判断这4种化合物的化学式分别为:甲______,乙_________,丙_______,丁________。丙的电子式为_________。
31.某待测液可能含有Fe3+、Fe2+、Ag+、Al3+、Ba2+、Ca2+、NH4+等离子。进行了下述实验(所加试剂均过量):
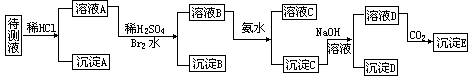
(1)判定待测液中有无Ba2+、Ca2+,并说明理由________________________。
(2)加Br2水的作用是____________________。
(3)写出沉淀C与NaOH溶液反应的离子方程式_____________。
(4)沉淀D的分子式为_______________。
(5)生成沉淀E的离子方程式为___________。
29.常温下,向 20L真空容器中通入 a molH2S和 b molSO2(a、b都是正整数,且a≤b,b≤5),反应完毕后,容器内气体可能达到的最大密度约是 [ ]
A.24.5g/L
B.14.4g/L
C.8g/L
D.5.1g/L

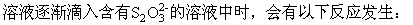

A.该鉴定可在酸性或碱性溶液中进行
B.该鉴定只能在中性溶液中进行
C.AgNO3必须过量
D.S2-对该鉴定有干扰
28.过氧化氢与硫酸酸化的高锰酸钾溶液进行反应生成硫酸钾、硫

后,含有示踪原子的物质是 [ ]
A.氧气
B.水
C.硫酸钾
D.硫酸锰
27.下列物质所发生的化学反应中,由于反应物的用量不同,而得到不同的产物的是 [ ]
①H2S+O2 ②P+Cl2 ③NaCl(固)+H2SO4(浓) ④P2O5+H2O ⑤ CH3CH2OH+浓 H2SO4 ⑥ Na2CO3+ HCl ⑦Cu+HNO3
A.全部都是
B.①②⑥
C.③④⑤⑥
D.①②⑥⑦
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com