
题目列表(包括答案和解析)
11.下列离子方程式正确的是 ( )
A.氢氟酸与氢氧化钾溶液反应: H++OH-=H2 O
B.硫化钠溶于水显碱性: S2-+ 2H2O=H2S↑+ 2OH--
C. 硝酸铁溶液中加过量氨水: Fe3++3NH3·H2O=Fe(OH)3↓+3NH4+
D. 硫酸铜溶液中加入氢氧化钡溶液:Ba2++ SO42-=BaSO4 ↓
10.用pH大小表示溶液的酸碱性相对强弱有许多不足之处。因此,荷兰科学家Henk Van Lubeck引入了酸度(AG)的概念,即把电解质溶液中的酸度定义为c(H+)与c(OH一)比值的对数,用公式表示为AG=lg [c(H+)/c(OH一)] 。常温下,在AG=10的溶液中能大量共存的离子是: ( )
A.Ca2+、K+、Cl-、SO32- B.NH4+、Fe2+、 I一、SO42-
C.Na+ 、K+、ClO-、S2- D.Na+、S2O32-、AlO2-、K+
9.已知物质的量浓度为10.84mol/L的氨水的溶质质量分数为20.00%,则10.00%的氨水的物质的量浓度应为 ( )
A.大于5.42 B.等于5.42 C.小于5.42 D.无法判断
8.若某池(电解池或原电池)的总反应离子方程式是 :Cu+2H+=== Cu2+ +H2↑,关于此池的有关说法正确的是 ( )
A.该池可能是原电池,也可能是电解池
B.该池只能是原电池,且电解质溶液为硝酸
C.该池只能是电解池,且金属铜为该电解池的阳极
D.该池只能是电解池,电解质溶液可以是硝酸
7.维生素E在国外美称之“生命奇迹丸”,是一种脂溶性维生素,对抗衰老等有特殊作用,经研究发现维生素E有α、β、γ、δ四种类型,其结构简式如下:
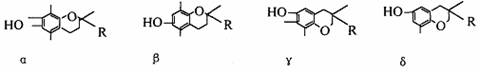
其中R为-CH2CH2CH2[CH(CH3)CH2CH2]2CH(CH3)2即:
上述互为同分异构体的是 ( )
A.α β B.β γ C.γδ D.α δ
6.硝酸铜是制备Cu-Zn-AI系催化剂的重要原料,制取硝酸铜现有三种设计方案可供选用 ( )
①Cu与稀硝酸反应制取,3Cu+8HN03=3Cu(NO)2+2NO↑+4H20
②Cu与浓硝酸反应制取,Cu+4HN03=Cu(NO3)2+2N02↑+2H20
③通氧气于铜屑与稀硝酸的体系中制2Cu+4HN03+02=2Cu(N03)2+2H2O
下列说法不正确的是 ( )
A.制取相同量的硝酸铜需硝酸的量③最少
B.制取相同量的硝酸铜①产生的有毒气体比②少
C.三种方案中硝酸的利用率③>①>②
D.三种方案的反应都可以在铁制容器中进行
5.某氯原子的质量是a g ,12C原子的质量是bg ,用NA表示阿伏加德罗常数,下列说法中正确的是。 ( )
A.氯元素的相对原子质量为 12b/a B.m g该氯原子的物质的量一定是m/a NA
C.该氯原子的摩尔质量是aNA D.n g该氯原子所含的电子数为17n/b
4.一定条件下硝酸铵受热分解的反应式为:NH4NO3→HNO3+N2+H2O 在反应中,被氧化与被还原的氮原子个数之比为 ( )
A.5:3 B.5:4 C.1:1 D.3:5
3.下列各组在溶液中的反应,不管反应物相对量是多少,都只能用同一个离子方程式来表示的是 ( )
A. FeBr2与Cl2 B. Ba(OH)2与H2SO4
C. HCl与Na2CO3 D. Ca(HCO3)2与NaOH
2.法国里昂的科学家最近发现一种只由四个中子构成的粒子,这种粒子称为“四中子”,也有人称之为“零号元素”。下列有关“四中子”粒子的说法不正确的是 ( )
A.该粒子不显电性 B.该粒子质量数为4
C.在周期表中与氢元素占同一位置 D.该粒子质量比氢原子大
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com