
ЬтФПСаБэ(АќРЈД№АИКЭНтЮі)
(ЫФ)ЪЕбщЙ§ГЬЃК
(1)ЯДЕгвЧЦїЃЌМьВщЕЮЖЈЙмЪЧЗёТЉвКЃЌШѓЯДКѓзАКУБъзМЕтШмвКД§гУЁЃ
(2)ДђПЊГШжАќзАЃЌФПВтЃКбеЩЋ--ГШЛЦЩЋЃЌГЮЧхЖШ--КУЁЃгУЁЁЁЁЁЁЁЁЁЁЁЁ (ЬювЧЦїУћГЦ)ЯђзЖЦПжавЦШы20.00mLД§ВтГШжЃЌЕЮШы2ЕЮжИЪОМСЁЃ
(3)гУзѓЪжПижЦЕЮЖЈЙмЕФЁЁЁЁЁЁ ЁЁЁЁЁЁЁЁ(ЬюВПЮЛ)ЃЌгвЪжвЁЖЏзЖаЮЦПЃЌблОІзЂЪгЁЁЁЁЁЁЁЁЁЁ ЃЌжБЕНЕЮЖЈжеЕуЁЃЕЮЖЈжСжеЕуЕФЯжЯѓЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
(Ш§)ЪЕбщгУЦЗМАЪдМСЃК
(1)вЧЦїКЭгУЦЗЃК(здбЁЃЌТд)
(2)ЪдМСЃКжИЪОМСЁЁЁЁЁЁЁЁЁЁЁЁ (ЬюУћГЦ)ЁЂХЈЖШЮЊ7.5ЁС10Ѓ3mol/LБъзМЕтШмвКЁЂеєСѓЫЎЕШ ЁЃ
(Жў)ВтЖЈдРэЃКC6H8O6+I2 C6H6O6+2H++2IЃЁЃ
C6H6O6+2H++2IЃЁЃ
(вЛ)ВтЖЈФПЕФЃКВтЖЈЁСЁСХЦШэАќзАГШжЮЌЩњЫиCКЌСПЁЃ
1.ЯТЭМЮЊгУЧтЦјЛЙдбѕЛЏЭЕФЮЂаЭПьЫйЪЕбщзАжУЁЃ
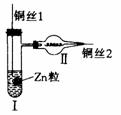
ЪЕбщЧАЯШНЋЭЫП1ДІРэГЩЯТЖЫБфЧњЕФвЛаЁдВЛЗЃЌВЂгУЬњДИЛїГЩДјаЁПзЕФаЁГзЃЛНЋЭЫП2вЛЖЫЭф ЧњГЩТна§зД(МћЭМ)ЁЃЪдЛиД№ЯТСаЮЪЬтЃК
(1)дкОпжЇЪдЙмЂёжаЯШМгШыЕФЪдМСЪЧЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
(2)ВйзїЭЫП2ЕФЗНЗЈЪЧЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
(3)ЪЕбщЯжЯѓЃКЂёжаЁЁЁЁЁЁЁЁЁЁЁЁ ЃЛЂђжаЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
(4)етбљДІРэЭЫП1ЕФгХЕуЪЧЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃетбљДІРэЭЫП2ЕФФПЕФЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
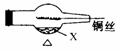
ЁЁ(5)ФГбЇЩњАбЭМAИФГЩЭМBЃЌШнЦїФкМггаФГвКЬхXЃЌЩдМгШШЃЌЭЫПЕФВйзїЗНЗЈЭЌЭЫП2ЁЃШєЗЂЯжЭЫПгЩКкБфКьЃЌдђвКЬхПЩФмЪЧЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
2.ЮЌЩњЫиCЪЧвЛжжЫЎШмадЮЌЩњЫи(ЦфЫЎШмвКГЪЫсад)ЃЌЫќЕФЗжзгЪНЪЧC6H8O6ЁЃШЫЬхШБЗІетжжЮЌЩњЫивзЕУЛЕбЊжЂЃЌЫљвдЮЌЩњЫиCгжГЦПЙЛЕбЊЫсЁЃЮЌЩњЫиCвзБЛПеЦјжаЕФбѕЦјбѕЛЏЁЃдкаТЯЪЕФЫЎЙћЁЂЪпВЫЁЂШщжЦЦЗжаЖМИЛКЌЮЌЩњЫиCЃЌШчаТЯЪГШжжаЮЌЩњЫиCЕФКЌСПдк500mg/Lзѓгв ЁЃ
аЃПЮЭтЛюЖЏаЁзщВтЖЈСЫФГЦЗХЦЕФШэАќзАГШжжаЮЌЩњЫиCЕФКЌСПЁЃЯТУцЪЧВтЖЈЪЕбщЗжЮіБЈИцЁЃ(ЧыЬюаДгаЙиПеАз)
7.Н№ИеЪЏЪЧЕфаЭЕФдзгОЇЬхЃЌОЇЬхжаЕФЛљБОНсЙЙЮЂСЃЪЧЬМдзгЁЃУПИіЬМдзгКЭжмЮЇЫФИіЬМдзгаЮГЩЭъШЋЯрЭЌЕФЙВМлЕЅМќЃЌЙЙГЩе§ЫФУцЬхЁЃ
ЂйдкН№ИеЪЏжаЕФЬМдзгЫљЙЙГЩЕФе§ЫФУцЬхжаЃЌМќНЧЕФгрЯвжЕЪЧЁЁЁЁЁЁЁЁЁЁЁЁ (ЬюЪ§жЕ)ЁЃ
ЂкН№ИеЪЏжаЕФЬМдзгЮЛгке§ЫФУцЬхЕФжааФЃЌжмЮЇЫФИіЬМдзгЮЛгкЫФИіЖЅЕуЩЯЃЌдкПеМфЙЙГЩСЌ ајЕФЁЂМсЙЬЕФЙЧМмНсЙЙЁЃвђДЫЃЌПЩвдАбвЛПщЭъУРЕФН№ИеЪЏОЇЬхПДГЩвЛИіОоДѓЕФЗжзгЁЃШєгавЛПХжЪСПЮЊ0.2ПЫРЕФЭъУРН№ИеЪЏЃЌПЩвдШЯЮЊЫќЕФЁАЗжзгСПЁБЪЧ(АЂЗќМгЕТТоГЃ Ъ§ШЁ6.0ЁС1023molЃ1)ЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
ЂлИпЗжзгЕФЗжзгСПЖМдкЮхЧЇвдЩЯЁЃЩЯЪіетПХН№ИеЪЏЪЧЗёЪєгкИпЗжзгЛЏКЯЮя?
Д№ЃКЁЁЁЁЁЁЁЁ (Ью ЁАЪЧЁБЛђЁАВЛЪЧЁБ)ЁЃвђЮЊЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
6.ШЫЬхЕФбЊвКжаДцдквЛЖЈХЈЖШЕФH2CO3ЁЂ ЃЌНЈСЂШчЯТЦНКтЃК
ЃЌНЈСЂШчЯТЦНКтЃК
H2CO3
 +H+
ЬхФкH2CO3ХЈЖШдіДѓЪБЃЌПЩЗжНтЃЌЭЈЙ§ЗЮВПХХГіCO2 ЁЃЖј
+H+
ЬхФкH2CO3ХЈЖШдіДѓЪБЃЌПЩЗжНтЃЌЭЈЙ§ЗЮВПХХГіCO2 ЁЃЖј ХЈЖШЬЋДѓЪБЃЌПЩДгЩідрдіМгХХГіСПЁЃбЊвКжавЛЖЈХЈЖШЕФH2CO3ЁЂ
ХЈЖШЬЋДѓЪБЃЌПЩДгЩідрдіМгХХГіСПЁЃбЊвКжавЛЖЈХЈЖШЕФH2CO3ЁЂ ЕФДцдкЃЌФмАяжњШЫЬхбЊвКЮЌГжвЛЖЈЕФpHжЕ(7.35-7.45)ЁЃ
ЕФДцдкЃЌФмАяжњШЫЬхбЊвКЮЌГжвЛЖЈЕФpHжЕ(7.35-7.45)ЁЃ
(1)ШЫЬхбЊвКЕФpHжЕБфЛЏ0.4ИіЕЅЮЛвдЩЯЃЌОЭЛсгаЩњУќЮЃЯеЁЃФГВЁШЫбЊвКЕФpHжЕНЯе§ГЃШЫ(pH вд7.4МЦ)БфЛЏСЫ0.3ИіЕЅЮЛЃЌЫћЬхФкбЊвКЕФH+ХЈЖШЪЧе§ГЃШЫЕФЁЁЁЁЁЁ ЛђЁЁЁЁЁЁ БЖЁЃ(вбжЊЃКlg2=0.3,lg3=0.48)
(2)ЕБФГаЉвђЫив§Ц№бЊвКжаЫсЖШдіМгЪБЃЌбЊвКЕФpHжЕЮЊЪВУДФмЮЌГжЛљБОВЛБф?гУМђвЊЮФзжЫЕУїЁЃ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
5.ЗДгІmA(g)+nB(g)  pC(g)дквЛЖЈЮТЖШКЭВЛЭЌбЙЧПЯТДяЕНЦНКтЪБЃЌЗжБ№ЕУЕНAЕФЮяжЪЕФСПХЈЖШШчЯТБэЫљЪОЃК
pC(g)дквЛЖЈЮТЖШКЭВЛЭЌбЙЧПЯТДяЕНЦНКтЪБЃЌЗжБ№ЕУЕНAЕФЮяжЪЕФСПХЈЖШШчЯТБэЫљЪОЃК
|
бЙЧП/Pa |
2ЁС105 |
5ЁС105 |
1ЁС106 |
|
c(A)mol/L |
0.08 |
0.20 |
0.44 |
ЗжЮіБэжаЪ§ОнЃЌЛиД№ЃК
(1)ЕБбЙЧПДг2ЁС102PaдіМгЕН5ЁС105PaЪБЃЌЦНКтЁЁЁЁЁЁЁЁЁЁЁЁ вЦЖЏЃЌ(ЬюЁА Яђ зѓЁБЁЂЁАЯђгвЁБЛђЁАВЛЁБ)РэгЩЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
(2)ЕБбЙЧПДг5ЁС105PaдіМгЕН1ЁС106PaЪБЃЌИУЗДгІЕФЛЏбЇЦНКтЁЁЁЁЁЁЁЁЁЁЁЁ вЦЖЏЃЌХаЖЯЕФвРЕФвРОнЪЧЁЁЁЁЁЁЁЁЁЁЁЁ ЃЌПЩФмЕФдвђЪЧЂйЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЃЌЂкЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЃ
4.ФГПЦбааЁзщгУИпСыЭС(жївЊГЩЗжЪЧAl2(Si2O5)(OH)4ЃЌВЂКЌгаЩйСПCuOЁЂFe2O 3)бажЦаТаЭОЛЫЎМСЃЌЦфЪЕбщВНжшШчЯТЃКНЋЭСбљКЭДПМюЛьКЯОљдШМгШШШлШкЃЌРфШДКѓгУЫЎНў ШЁШлПщЃЌЙ§ТЫЃЌЦњШЅВадќЃЌТЫвКгУбЮЫсЫсЛЏЃЌОЙ§ТЫЗжБ№ЕУГСЕэКЭШмвКЃЌШмвКМДЮЊОЛЫЎМСЁЃ ЪдЛиД№ЯТСаЮЪЬтЃК
(1)гУбѕЛЏЮяБэЪОИпСыЭСЕФжївЊГЩЗжЃКЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
(2)аДГіШлШкЪБжївЊГЩЗж(МДИїбѕЛЏЮя)ЗжБ№гыДПМюЗДгІЕФЛЏбЇЗНГЬЪНЃКЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
(3)зюКѓЕУЕНЕФГСЕэЪЧЁЁЁЁЁЁЁЁ ЃЌЩњГЩГСЕэЕФРызгЗНГЬЪНЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
(4)БОЪЕбщдкШлШкЭСбљЪБгІбЁгУЕФлсліЪЧЁЁЁЁЁЁЁЁЁЁЁЁ (ЬюЁАДЩлсліЁБЁЂЁАбѕЛЏТСлсліЁБЁЂЁАЬњлс ліЁБ)ЁЃ
3.ЫеДђКЭаЁЫеДђгазХЙуЗКЕФгІгУЁЃЪдДгЯћКФЗДгІЮяЕФСПЕФНЧЖШЃЌЛиД№ЯТСаЮЪЬтЃК
(1)зіУцЬѕЪБЗРжЙУцЗлНЯГЄЪБМфДЂДцБфЫсЮЖЃЌГЃМгШыЪЪСПЕФУцМюЃЌбЁгУЁЁЁЁЁЁЁЁЁЁЁЁ ЃЌвђЮЊ
ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
(2)зїЮЊХнФУ№Л№ЦїЕФвЉЦЗЃЌбЁгУЁЁЁЁЁЁЁЁЁЁЁЁ ЃЌвђЮЊЁЁЁЁЁЁЁЁЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЃ
(3)гУгкЯДЕгВЭОпМАЪЕбщЪвЕФВЃСЇвЧЦїЕШЃЌбЁгУЁЁЁЁЁЁЁЁЁЁ ЃЌвђЮЊЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
АйЖШжТаХ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com