
题目列表(包括答案和解析)
6、下列事实不能用电化学原理解释的是( )
A、 常温条件下,在空气中铝不容易被腐蚀
B、 镀锌铁片比镀锡铁片更耐腐蚀
C、 用锌与硫酸制氢气时,往硫酸中滴少量硫酸铜
D、 远洋海轮的尾部装上一定数量的锌板
5、X、Y、Z是三种单质。已知:Y能够把Z从其化合物的水溶液中置换出来,而Z又能在一定条件下把X从其化合物的水溶液中置换出来。由此可推知下列说法可能正确的是( )
①单质的氧化性:Y>Z>X ②单质的还原性:Y>Z>X
③对应离子的氧化性:X>Z>Y ④对应离子的还原性:X>Z>Y
A、只有② B、只有②③ C、只有①④ D、①②③④
4、已知,往0.1mol/L的氨水中滴入酚酞试液时,溶液将呈现粉红色。现采取下列措施,滴有酚酞的氨水溶液颜色不会变浅的是( )
A、往溶液中滴入稀硫酸 B、往溶液中加入NH4Cl
C、把溶液加热至沸腾 D、往溶液中加入NaOH
3、一般认为:原子在相互作用形成化合物时,需要通过电子转移(得
失或共用)形成最外层8电子稳定结构(H 除外)。但是,也有许多化合物例外,即最外层电子不足或超过8个电子。下面所列的化合物中,各原子无法满足最外层8电子的是( )
A、PCl3 B、NaCl C、NO D、CCl4
2、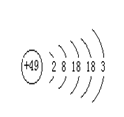 张清莲是我国著名的化学家。1991年,他准确测得In
张清莲是我国著名的化学家。1991年,他准确测得In
的原子量为114.818,被国际原子量委员会采用为新的标准值。
这是原子量表中首次采用我国测定的原子量值。已知In的原子结
构如图所示,则下列关于In的说法不正确的是( )
A、In为长周期元素 B、In为过渡元素
C、In易导电导热 D、In在反应中容易失电子
1、氧气和臭氧都是由氧原子组成,氧气是生命活动中不可缺少的物质之一,而臭氧是一种有刺激性气味的气体,浓度较高时会对人体健康造成危害,如使脑干受损、干扰体温调节及严重影响视力等。氧气和臭氧应属于( )
A.同系物 B.同素异形体 C.同位素 D. 同分异构体
 32.一定条件下,可逆反应A2+B2 2C达到了化学平衡状态,经测定平衡时C(A2)=0.5
mol/L,C(B2)=0.1
mol/L,C(C)=1.6
mol/L,若A2、B2、C的起始浓度分别为a mol/L、b mol/L、c mol/L,请回答:
32.一定条件下,可逆反应A2+B2 2C达到了化学平衡状态,经测定平衡时C(A2)=0.5
mol/L,C(B2)=0.1
mol/L,C(C)=1.6
mol/L,若A2、B2、C的起始浓度分别为a mol/L、b mol/L、c mol/L,请回答:
(1)a、b应满足的关系是______________________________
(2)a的取值范围_____________________________________
31.(14分)
(1)使用容量瓶配制溶液时,由于操作不当,会引起误差,下列情况会使所配溶液浓度偏低的是______________________。
①用天平(使用游码)称量时,被称量物与砝码的位置放颠倒了
②用滴定管量取液体时,开始时平视读数,结束时俯视读数
③溶液转移到容量瓶后,烧杯及玻璃棒未用蒸馏水洗涤
④转移溶液前容量瓶内有少量蒸馏水
⑤定容时,俯视容量瓶的刻度线
⑥定容后摇匀,发现液面降低,又补加少量水,重新达到刻度线
(2)工业上测量SO2、N2、O2混合气体中SO2含量的装置如下图;反应管中装有碘的淀粉溶液。SO2和I2发生的反应为(N2、O2不与I2反应):SO2+I2+2H2O→H2SO4+2HI
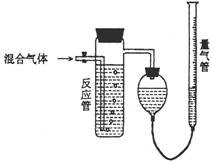 ①混合气体进入反应管中,量气管内增加的水的体
①混合气体进入反应管中,量气管内增加的水的体
积等于 _____ 的体积(填写气体的分子式)。
②反应管内溶液蓝色消失后,没有及时停止通气,则测得的SO2含量 (选填:偏高,偏低,不受影响)。
③反应管内的碘的淀粉溶液也可以用 代替
(填写物质名称)。
④若碘溶液体积为VamL.,浓度为cmol·L-1,N2与O2的体积为VbmL(已折算为标准状况下的体积)。用c、Va、Vb表示SO2的体积百分含量为: 。
⑤将上述装置改为简易实验装置,除导管外,还需选用的仪器为. (选下列仪器的编号)。
a.烧杯 b.试管 c.广口瓶 d.容量瓶 e.量筒 f.单孔塞 g.双孔塞
30.(9分)据报道,目前我国结核病的发病率有抬头的趋势。抑制结核杆菌的药物除雷米封外,PAS-Na(对氨基水杨酸钠)也是其中一种,它与雷米封同时服用,可以产生协同作用。
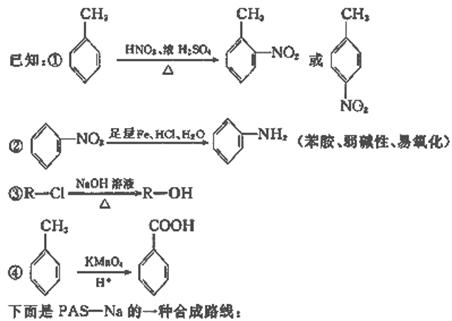
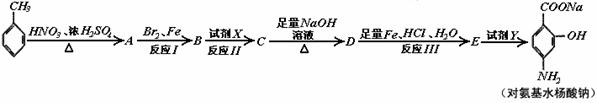
请按要求回答下列问题:
(1)写出下列反应的化学方程式并配平:
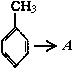
:__________________________________________。
A→B: _______________________ 。
(2)写出下列物质的结构简式:C ;D 。
(3)指出反应类型:Ⅰ ;Ⅱ ;Ⅲ 。
(4)所加试剂名称:X ;Y
29.(6分)
①有机物A在浓H2SO4存在的条件下,相互作用生成一种环状酯,结构如图所示:
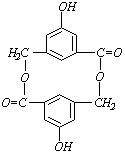 则有机物A的结构简式为____________________。
则有机物A的结构简式为____________________。
②等物质的量的A分别与Na、NaOH、NaHCO3充分反应,消耗Na、NaOH、NaHCO3的物质的量之比为________________
③B与A互为同分异构体,且知苯环上的一氯代物只有2种,B不与NaHCO3反应,能与Na、NaOH溶液反应,等质量的B消耗Na、NaOH物质的量之比为2:3,则B的结构简式为________(只写一种)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com