
题目列表(包括答案和解析)
3、为了测定某铜银合金的成分,将30.0g金属完全溶于80mL 13.5 mol·L-1的浓HNO3中,待合金完全溶解后,收集到气体6.72L(标准状况)并测得溶液的PH=0,假设反应后溶液的体积仍为80mL,试计算
(1)被还原的HNO3的物质的量
(2)合金中银的质量分数
2、有一包白色固体,可能由Na2CO3、NaHCO3、(NH4)2CO3、NH4HCO3中的二种或几种组成,把它溶于水配成100mL溶液,测得其中[NH4+]=0.2mol·L-1(不考虑水解),如果加入3 mol·L-1的盐酸15mL,恰好完全反应,可产生标准状况下的CO2672mL,通过计算确定该白色固体可能有哪些化合物及其物质的量是多少?
1、有烧碱、小苏打及不与酸、碱反应也不溶于水的杂质组成的混合物30g,将其平均分为两等份做以下实验:
(1)将第一份置于密闭容器中加热至2500C,充分反应后,将密闭容器中的气体导入过量的澄清石灰水中,得到白色沉淀5g
(2)将第二份溶于水配成100mL溶液,(除杂质外全部溶解),取10mL该溶液能跟1mol·L-1的盐酸20mL恰好反应.求混合物中杂质的质量分数.
10、取3.40只含g羟基不含其它管能团的液态饱和多元醇,置于5.0L氧气中,经点燃,醇完全燃烧,反应后气体体积减少0.560L,将气体经CaO吸收,体积又减少2.80L(所有气体体积均在标况下测定)
(1)3.40g醇中C、H、O物质的量分别为C mol,H mol O mol, 该醇中C、H、O的原子数之比为 .
(2)由以上比值能否确定该醇的化学式? 其原因是
(3)如果多元醇的任意一个羟基,换成一个卤原子,所得到的卤代物都只有一种,试写出该饱和多元醇的结构简式
9、含有H2、Cl2混合气100mL(标况),其中一种为45mL,另一种为55mL,光照使其充分反应,恢复至标准状况,气体体积为 mL,为证明反应后气体中H2或Cl2有剩余,使气体通过100mL水,若
(1)剩余气体为 mL,证明 有剩余.
(2)溶液有 性质,证明有 剩余.
(3)由于气态HCl易溶于水,有人认为测定溶液的PH值并和计算值核对,即可知H2和
Cl2谁剩余,你同意这个观点吗?请说明理由 .
8、一定条件下,可逆反应A2(g)+B2(g) 2C(g)达到化学平衡状态,测得平衡状态时[A2]=0.5mol·L-1,[B2]=0.1omol·L-1,[C]=1.6mol·L-1,其中A2、B2、C的起始浓度分别为a mol·L-1、b mol·L-1、c mol·L-1,请回答:
a、b应满足的关系是 a的取值范围是 说明你的结论的由来 .
7、将一定量的氨氧化成硝酸,并全部溶解在反应所生成的水中,则这种硝酸的质量分数为
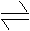 .
.
6、在铁与铜的混合物中加入一定量的稀HNO3,充分反应后剩余金属m1g,再向其中加入一定量的稀H2SO4,充分振荡后剩余金属m2g,则m1与m2之间的大小关系是 原因是
.
5、把河沙(主要成分为SiO2)跟镁粉按一定质量比(略大于15:24)混合均匀,装入试管中加热大约1min后,发生剧烈反应,生成一种白色固体化合物和一种硅化合物,待生成的混合物冷却后入盛有稀H2SO4的烧杯中,立即产生气泡并伴有轻微的爆炸声,这是因为产生的气体是一种能在空气中自燃的气态氢化物.
(1)写出河沙与镁粉在加热条件下发生反应的化学方程式 ,该反应是 反应(填“吸热”或“放热”)
(2)生成的混合物放入稀H2SO4中产生的气体是 (填化学式)
(3)写出产生“爆炸”时的反应方程式 .
4、称取mg纯Na2CO3固体恰好和20mL盐酸作用,反应生成CO2、H2O及NaCl,则这种盐酸的物质的量浓度为 .
(1)如果上述mg Na2CO3中实际混有少量的NaCl,那么这种盐酸的实际浓度比上面的数值要 .
(2)如果上述mg Na2CO3中实际混有少量K2CO3,那么这种盐酸的实际浓度比上面的值要 .
(3)如果上述mg Na2CO3中实际混有少量NaOH时,那么这种盐酸的实际浓度比上面的数值要 .
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com