
题目列表(包括答案和解析)
21、(9分)常温下,将a molFe投入含b molHNO3的浓硝酸中,经一段时间反应停止后溶液中Fe3+和Fe2+的物质的量相等,HNO3的还原产物为NO和NO2,且不考虑NO2转化为N2O4。反应中可产生气体c L,将该气体溶于水,充分反应后,气体体积减少到d L,(气体体积均为标准状态下体积)。
(1)硝酸是否完全反应?为什么?
(2)若a=0.6,求出b的取值范围,求出d的值(写出计算过程)
20.(11分)下图①-⑩分别代表有关反应中的一种物质,请填写以下空白:
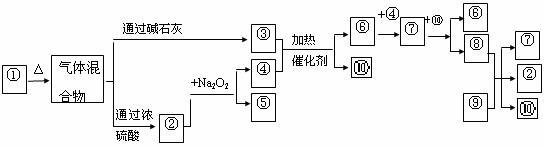
⑴、写出②③的化学式分别为 、 。
⑵、①分解的化学方程式
③和④反应的化学方程式
⑶、⑧与⑨反应的化学方程式 。
19、(16分)某课外活动小组用如图所示的实验装置探究氯气与氨气之间的反应。其中A、F为氨气和氯气的发生装置,C为纯净、干燥的氯气与氨气反应的装置。

请回答下列问题:
(1)装置F中发生反应的离子方程式是 。
(2)装置A中的烧瓶内固体可选用 (选填以下选项的代号)。
A.碱石灰 B.浓硫酸 C.生石灰 D.五氧化二磷 E.烧碱
(3)虚线框内应添加必要的除杂装置,请从右图的备选装置中选择,并将编号填入下列空格。B 、D 、E 。
(4)氯气和氨气在常温下混合就能发生反应生成氯化铵和氮气,该反应的化学方程式为: ;装置C内出现浓厚的白烟并在容器内壁凝结,请设计一个实验方案鉴定该固体就是氯化铵: 。
(5)若从装置C的G处逸出的尾气中含有N2和少量C12,应如何处理?
。
18、(12分)向2L密闭容器中通入amol 气体 A和bmol气体B,在一定条件下发生反应;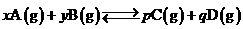 已知:平均反应速率
已知:平均反应速率 ;反应2min 时,A的浓度减少了
;反应2min 时,A的浓度减少了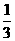 ,B的物质的量减少了
,B的物质的量减少了 mol,有a mol D生成。
mol,有a mol D生成。
回答下列问题:
(1)反应2min内,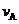 =
,
=
,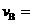 ;
;
(2)化学方程式中,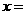 、
、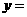 、
、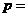 、
、 ;
;
(3)反应平衡时,D为2a mol,则B的转化率为 ;
(4)欲提高该反应的反应速率,下列措施可行的是 。(填字母)
A.恒容时向装置中再充入N2 B.将容器的容积变为1L
C.使用合适的催化剂 D.升高温度
(5)如果其他条件不变,恒容时向装置中再充入A气体,进行同样的实验,则与上述反应比较:反应速率 (填“增大”、“减小”或“不变”),理由是 ;
17、(12分)向盛有KI溶液的试管中加入少许CCl4后滴加氯水,CCl4层变成紫色。如果继续向试管中滴加氯水,振荡,CCl4层会逐渐变浅,最后变成无色。完成下列填空:
(1)写出并配平CCl4层由紫色变成无色的化学反应方程式(如果系数是1,不用填写):

(2)在整个的反应过程中的还原剂是 。
(3)把KI换成KBr,则CCl4层变为_ _色:继续滴加氯水,CCl4层的颜色没有变化。Cl2、HIO3、HBrO3氧化性由强到弱的顺序是 。
(4)加碘盐中含碘量为12.7mg-50mg/kg。制取加碘盐(含KIO3的食盐)1000kg,若庄Kl与Cl2反应制KIO3,至少需要消耗Cl2 L。
16、 可逆反应:2NO2 2NO + O2在体积不变密闭容器中进行,达到平衡状态的标志是
可逆反应:2NO2 2NO + O2在体积不变密闭容器中进行,达到平衡状态的标志是
(1)单位时间内生成n mol O2的同时生成2n mol NO2
(2)单位时间内生成n mol O2的同时,生成2n mol NO
(3)用NO2、NO、O2物质的量浓度变化表示的反应速率的比为2:2:1的状态
(4)混合气体的颜色不再改变的状态 (5)混合气体的密度不再改变的状态
(6)混合气体的平均相对分子质量不再改变的状态
A. (1)(4)(6) B. (2)(3)(5)
C. (1)(3)(4) D. (1)(3)(4)(6)
第Ⅱ卷(非选择题 共60分)
15、关于合成氨的反应N2+3H2 2NH3,下列有关说法不正确的是( )
2NH3,下列有关说法不正确的是( )
A.选择工业反应条件时,要综合考虑反应的快慢和反应进行的程度
B.升高温度与加催化剂都能增大反应物活化分子百分率
C.为了加快化学反应速率,工业上选择高温高压合成氨
D.若3v(H2)正 = 2v(NH3)逆,则反应达平衡
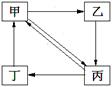
14、下表所列各组物质中,物质之间通过一步反应就能实现如图所示转化的是
|
物质 编号 |
甲 |
乙 |
丙 |
丁 |
物质转化关系 |
|
A |
Cu |
CuCl2 |
CuO |
Cu(NO3)2 |
 [ [ |
|
B |
Na2CO3 |
NaOH |
NaHCO3 |
CO2 |
|
|
C |
Fe |
Fe Cl3 |
Fe(OH)3 |
Fe2O3 |
|
|
D |
N2 |
NO |
HNO3 |
NH3 |
13、1L稀硝酸和稀硫酸的混合液,其物质的量浓度分别为0.1mol/L和0.4mol/L。若向该混合液中加入足量的铜粉,则最多能溶解铜粉的质量为
A 2.4g B 3.2g
C 6.4g D 9.6g
12、如图在同温同压下,两个等体积的干燥圆底烧瓶中分别充 满:①NH3 ②NO2进行喷泉实验。经充分反应后,瓶内溶液的物质的量浓度的比较关系为( )
A.①>②
B.①=②
C.①<②
D.不能确定
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com