
题目列表(包括答案和解析)
1.(2003年春季高考理综题)家用炒菜铁锅用水清洗放置后,出现红棕色的锈斑,在此变化过程中不发生的化学反应是
A.4Fe(OH)2+2H2O+O2===4Fe(OH)3↓
B.2Fe+2H2O+O2===2Fe(OH)2↓
C.2H2O+O2+4e-===4OH-
D.Fe-3e-===Fe3+
26.解析:先求平均相对分子质量M:M=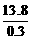 =46
=46
设式量较小的一种醇为CnH2n+2O,式量为14n+18,14n+18<46,14n<28,n<2。所以必有一种是甲醇,另一种碳原子大于2而小于5的可能是丙醇,也可能是丁醇。
设平均“化学式”为CmH2m+2O,有
CmH2m+2O+3m/2O2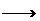 mCO2+ (m+1)H2O
mCO2+ (m+1)H2O
1 3m/2 m m+1
前后物质的量之差为m/2,由已知条件得1∶m/2= 0.4∶0.4,m=2。
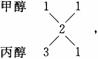
当混合物为甲醇与丙醇时,计算平均碳: n(甲醇)∶n(丙醇)=1∶1。

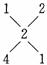
当混合物为甲醇与丁醇时,有 ,n(甲醇)∶n(丁醇)=2∶1。

根据溶液质量守恒可得
1.8x+5x×1=500×1.2 x=88.2 mL
1∶5
H2SO4溶液的质量分数为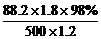 ×100%=25.9%
×100%=25.9%
1∶5
H2SO4溶液的物质的量的浓度为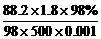 =3.18 mol·L-1
=3.18 mol·L-1
答案:应取质量分数为98%的浓H2SO4 88.2 mL;1∶5 H2SO4溶液的质量分数为25.9%,物质的量的浓度为3.18 mol·L-1。
(2)①乳酸为一元酸②乳酸分子中除含一个羧基外,还含一个羟基③乳酸分子中的羟基在羧基相邻的碳原子上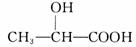
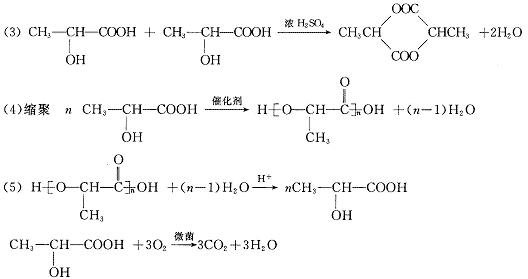
24.解析:本题关键从题意中提供“柯达尔”高聚物的有机结构信息不难推出它的两种单体是
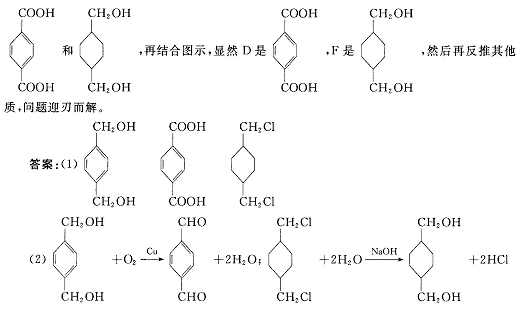
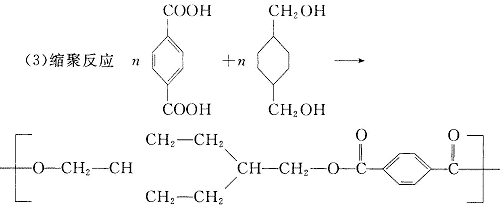
答案:(1)逆压强增大2.5倍,而D浓度增大2.3倍,压强增大倍数大于D浓度增大倍数
(2)正压强增大2倍,而D浓度增大2.2倍,压强增大倍数小于D浓度增大倍数,故平衡向正反应方向移动。这是由于加压后E被液化使平衡正移
22.解析:A盐固体受热分解为三种物质,且为非氧化还原反应。由此很容易想到可能是(NH4)2CO3或NH4HCO3。又因为电解Z盐溶液生成三种物质,其中两种物质(X和Y)为单质,且X与F化合生成D,结合这两点,X应为H2,F为N2,D为NH3。这样Z盐应似NaCl或KCl,则Y为Cl2,W为NaOH或KOH,A盐确实为(NH4)2CO3或NH4HCO3,B为CO2,G为Na2CO3或NaHCO3,C为水,E为HCl或NH4Cl(NH3过量时)。
答案:(1)(NH4)2CO3或NH4HCO3 N2 H2 Cl2
(2)CO2+2NaOH====Na2CO3+H2O或CO2+NaOH====NaHCO3
|
(3)N2+3H2 2NH3
2NH3
答案:实验步骤如下:
(1)取少量明矾固体,放入一支干燥的试管中,用酒精灯给试管中的固体加热,观察试管内壁上的现象。(应有水珠出现)
(2)取少量明矾放入烧杯中,加蒸馏水搅拌配成稀溶液。向三支试管中分别加入明矾溶液。
(3)向第一支试管中滴入NaOH,观察沉淀的生成量与NaOH的量的关系。(证明有Al3+)
(4)向第二支试管中滴加BaCl2溶液和稀盐酸,观察产生的现象(证明有SO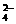 )。
)。
(5)用一根洁净的铂丝蘸取第三支试管中的溶液,在酒精灯火焰上灼烧,透过蓝色钴玻璃观察火焰的颜色(证明含有K+)。
20.(1)棉花球变蓝;B中石灰水变浑浊;开始时A中有气泡产生;小试管内有液滴出现
(2)防止倒吸
(3)NaHCO3的热稳定性比Na2CO3的差,NaHCO3分解有CO2和H2O生成
(4)B C(E)或ABC(E)
(5)将圆底烧瓶倒置,向试管中分别加入所选试剂,迅速将试管的上口伸至烧瓶的底部,过一会将湿润的红色石蕊试纸置于烧瓶口处,若试纸变蓝,则说明NH3已集满
(6)NH3·H2O====NH3+H2O(或同时有:NH4Cl+NaOH====NH3↑+NaCl+H2O)
(7)简化实验操作,提高实验效果,节约药品
18.C根据题意可知对苯二酚具有还原性,能被Ag+氧化,则应能被O2氧化,故C项不正确,应选C。
17.D aX(g)+bY(g)
 cZ(g)+dW(g),达到平衡后加压,容器容积缩小一半,W的浓度应增大2倍,而实际只增大1.8倍,说明平衡向逆反应方向移动:(a+b)<(c+d);Z的体积分数降低,X的转化率变小,所以D选项正确。
cZ(g)+dW(g),达到平衡后加压,容器容积缩小一半,W的浓度应增大2倍,而实际只增大1.8倍,说明平衡向逆反应方向移动:(a+b)<(c+d);Z的体积分数降低,X的转化率变小,所以D选项正确。
16.D A.从结构可看出C原子为12,O原子为4,其中结构中有二个双键,二个环,所以H原子数为:12×2+2-4×2=18,分子式为C12H18O4;B.该化合物结构中不含有官能团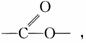 所以不属于有机酯;C.该化合物结构中在仲碳原子上连有羟基,所以能发生消去反应,但催化氧化时应生成酮;D显然正确。
所以不属于有机酯;C.该化合物结构中在仲碳原子上连有羟基,所以能发生消去反应,但催化氧化时应生成酮;D显然正确。
15.D A项BaSO4不溶于水,SO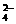 与Ba2+不能共存。B项H+、NH
与Ba2+不能共存。B项H+、NH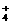 、Al3+、SO
、Al3+、SO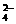 可共存,加入大量氨水,则生成沉淀,Al3++3NH3·H2O====Al(OH)3↓+3NH
可共存,加入大量氨水,则生成沉淀,Al3++3NH3·H2O====Al(OH)3↓+3NH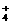 。C项,H+与CH3COO―不能大量共存。D项,可以共存,加氨水后也不变化。
。C项,H+与CH3COO―不能大量共存。D项,可以共存,加氨水后也不变化。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com