
题目列表(包括答案和解析)
1.假若是你在将来发现了186号元素Uoh,如果其中一同位素是 ,那么该元素原子的中子数与核外电子数之差为( )
A、186 B、375 C、3 D、189
2. 对于3BrF3 + 5 H2O = HBrO3 + Br 2 + 9 HF + O2反应,若有5mol水充当还原剂,则被水还原的BrF3的物质的量为( )mol.
A、2/3 B、10/3 C、2 D、4/3
26.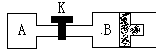 (9分)如图所示,当关闭K时,向A中充入1molX、1molY,向B中充入2molX,2molY,起始时,V(A) = V(B) = aL。在相同温度和有催化剂存在的条件下,两容器中各自发生下列反应:2X(g) + 2Y(g)=Z(g) + 2W(g);
(9分)如图所示,当关闭K时,向A中充入1molX、1molY,向B中充入2molX,2molY,起始时,V(A) = V(B) = aL。在相同温度和有催化剂存在的条件下,两容器中各自发生下列反应:2X(g) + 2Y(g)=Z(g) + 2W(g);
△H<0,达到平衡(Ⅰ)时,V(B) = 0.8aL。请回答:
⑴B中X的转化率α(Y)B为___________________
⑵A中W和B中Z的物质的量比较:n(Z)B __________ n(W)A (填大于、小于、等于);
⑶打开K,过一段时间重新达平衡(Ⅱ)时,A和B的总体积为_______________(用a的代数式表示,连通管中气体体积不计。)
25.(11分)A为烃,B为烃的含氧衍生物,由等物质的量的A和B组成的混合物0.05mol在0.125molO2中恰好完全燃烧生成0.1molCO2和0.1molH2O,通过计算回答:
(1)从分子组成的角度分析,该混合物的组合可能有几种?
(2)另取一定量的A和B的混合物完全燃烧,将其以任意比混合且物质的量之一和一定。
①若耗氧量一定,则A和B的分子式分别的 、 。
②若生成的CO2和H2O的物质的量一定,则A和B的分子式分别是 、 。
24.(10分)已知:R表示烃基,R’表示烃基或氢原子,X表示卤原子
①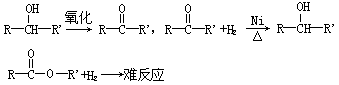
②R-X 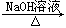 ROH
ROH
链烃A能发生如下图所示的一系列变化
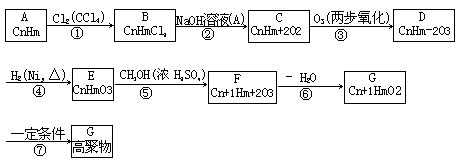
在上述转化中,已知2个E分子间可脱去水分子缩合生成环状化合物C6H8O4。试填写下列空白:
(1)C6H8O4的结构简式为 。
(2)链烃A的结构简式为 。
(3)在反应①-⑦中属于取代反应的 。
(4)写出反应④、⑦的化学方程式:
④
⑦
23.(8分)A、B都是芳香族化合物,1molA水解得到1molB和1mol乙酸。A、B的相对分子质量都不超过200,完全燃烧都只生成CO2和H2O。且B分子中碳和氢元素总的质量百分含量为65.2%,(即质量分数为0.652)。A溶液具有酸性,不能使FeCl3溶液显色。
(1)A、B两化合物的相对分子质量之差为 。
(2)1个B分子中应该有 个氧原子。
(3)A的分子式是 。
(4)B可能的三种结构简式: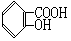
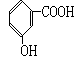 和
。
和
。
22.(10分)已知单质铁溶于一定浓度的硝酸溶液中反应的离子方程式为: a Fe + b NO3- + c H+ = d Fe2+ + f Fe3+ + g NO↑ + h N2O↑ + k H2O(化学计量数a~k均为正整数)。回答下列问题:(1)根据反应中氮、氢、氧三种元素的原子个数守恒,可得c、g、h的关系式是(用一个代数式表示。下同) 。
(2)根据反应中离子的电荷守恒,可得b、c、d、f的关系式是 。
(3)根据反应中电子转移的总数相等,可得d、f、g、h的关系式是 。
(4)若a=12,且铁和稀硝酸恰好完全反应,则b的取值范围是 ;c的取值范围是 。
21.(12分)A、B、C、D为四种单质,常温时,A、B是气体,C、D是固体。E、F、G、H、I为五种化合物,F不溶水,E为气体且极易溶于水成为无色溶液,G溶于水得黄棕色溶液。这九种物质间反应的转化关系如图所示
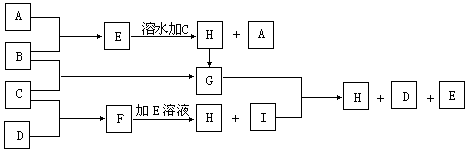
(1)写出四种单质的化学式
A B C D
(2)写出E+F-→H+I的离子方程式
(3)写出G+I-→H+D+E的离子方程式
20.(12分)铜是生命必需的元素,也是人类最早使用的金属之一,铜的生产和使用对国计民生各个方面产生了深远的影响。(在化学反应中,铜元素通常可表现为0、+1、+2价)。
⑴在西汉古籍中曾有记载:曾青得铁则化为铜[即:曾青(CuSO4)跟铁反应就生成铜]。试写出该反应的离子方程式: 。
⑵铜器表面有时会生成铜绿[Cu2(OH)2CO3],这层铜绿可用化学方法除去。试写出除去铜绿而不损伤器物的反应的化学方程式: 。
⑶某种碱式碳酸铜的组成可表示为Cu2(OH)2CO3·xH2O,在加热条件下,发生分解的化学方程式为:Cu2(OH)2CO3·xH2O===2CuO+CO2↑+(x+1)H2O。现取该碱式碳酸铜样品,进行测量该样品(粉末)组成中碳的质量分数和结晶水x的值的实验。
现有下面几种仪器(必要的铁架台、铁夹、酒精灯、橡皮管等,均在图中略去)
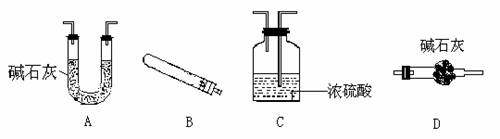
用上述仪器进行组装并做实验时,按气流方向从左到右连接顺序是(用字母填写,下同)( )→( )→( )→(D)
⑷新制的Cu(OH)2悬浊液与葡萄糖反应会生成红色沉淀,因此该试剂可用于检验糖尿病人尿液中葡萄糖的含量。葡萄糖的结构简式如下:
CH2OH-CHOH-CHOH-CHOH-CHOH-CHO(简写为GCHO)
试写出GCHO与新制Cu(OH)2反应的化学方程式: 。
19.(6分)下列有关实验的叙述,正确的是(填序号)
A. 制备Fe(OH)2时,盛NaOHaq的滴管不能伸入到试管中
B. 用渗析法分离淀粉中混有的NaCl杂质
C. 无法用分液漏斗将甘油和水的混合液体分离
D. 用酸式滴定管量取20.00mL高锰酸钾溶液
E. 为了测定某溶液的pH,将未经湿润的pH试纸浸入到待测溶液,过一会取出,与标准比色卡进行对比
F. 用浓氨水洗涤做过银镜反应的试管
G. 配制银氨溶液时,将稀氨水慢慢滴加到硝酸银溶液中,产生沉淀后继续滴加到沉淀刚好溶解为止
18.物质的量浓度相同(0.1mol/L)的弱酸HX和NaX溶液等体积混合后,溶液中微粒浓度关系错误的是
A.c(Na+)+ c(H+)= c(X-)+ c(OH-)
B.c(HX )+ c(X-)= c(Na+)
C.若溶液呈酸性,则c(X-)>c(Na+)>c(HX)>c(H+)>c(OH-)
D.若溶液呈碱性,则c(Na+)>c(HX)> c(X-)>c(OH-)>c(H+)
第II卷(非选择题 共78分)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com