
题目列表(包括答案和解析)
30、用下列仪器、药品验证由铜和适量浓硝酸反应产生的气体中含NO(仪器可选择使用,N2和O2的用量可自由控制)。
已知:①NO+NO2+2OH-→2NO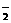 +H2O②气体液化温度:NO2 21℃ NO -152℃
+H2O②气体液化温度:NO2 21℃ NO -152℃
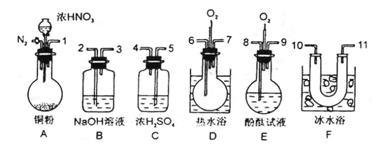
试回答:(1)仪器的连接顺序(按左→右连接,填各接口的编号)为
(2)反应前先通入N2目的是 (3)确认气体中含NO的现象是 (4)装置F的作用是
(5)如果O2过量,则装置B中发生反应的化学方程式为:
29、高炉炼铁中发生的基本反应之一如下:FeO(固)+CO(气)≒Fe(固)+CO2(气)-Q ,其平衡常数可表达为 K=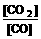 ,已知1100℃时,K=0.263 。
,已知1100℃时,K=0.263 。
(1)温度升高,化学平衡移动后达到新的平衡,高炉内CO2和CO和体积比值
平衡常数K值 (本小题空格均备选:增大、减小或不变)
(2)1100℃时测得高炉中[CO2]=0.025mol/L [CO]=0.1mol/L,在这种情况下,该反应是否处于化学平衡状态 (选填是或否),此时,化学反应速度是V正 V逆(选填大于、小于或等于),其原因是
28、汽车尾气(含有烃类、CO、SO2与NO等物质)是城市空气的污染源。治理的方法之一是在汽车的排气管上装一个“催化转换器”(用铂、钯合金作催化剂)。它的特点是使CO与NO反应,生成可参与大气生态环境循环的无毒气体,并促使烃类充分燃烧及SO2的转化。
(1)写出一氧化碳与一氧化氮反应的化学方程式
(2)“催化转换器”的缺点是在一定程度上提高空气的酸度,其原因是
(3)控制城市空气污染源的方法可以有 (多选扣分)
a 开发氢能源 b 使用电动车 c 植树造林 d 戴上呼吸面具
27、a、b、c、d、e、f、g为七种由短周期元素构成的微粒,它们都有10个电子,其结构特点如下:
|
微粒代码 |
a |
b |
c |
d |
e |
f |
g |
|
原子核数 |
单核 |
单核 |
双核 |
多核 |
单核 |
多核 |
多核 |
|
带电荷数 (单位电荷) |
0 |
1+ |
1- |
0 |
2+ |
1+ |
0 |
其中b的离子半径大于e的离子半径;d是由极性键构成的四原子极性分子;c与f可形成两个共价型g分子。
试写出:(1)a微粒的核外电子排布式
(2)b与e相应元素的最高价氧化物对应水化物的碱性强弱比较为 > (用化学式表示) (3)d溶于水的电离方程式
(4)g微粒所构成的晶体类型属 (5)c微粒是 ,f微粒是
(用化学式表示)
26、智利硝石矿层中含有碘酸钠,可用亚硫酸氢钠与其反应来制备单质碘。
(1)试配平该反应的化学方程式,并用短线标出电子转移方向及总数
NaIO3 + NaHSO3→ NaHSO4+ Na2SO4+ I2+ H2O
(2)已知含氧酸盐的氧化作用随溶液酸性的加强而增强,在制备试验时,定时取样,并用酸化的氯化钡来检测SO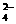 离子生成的量,发现开始阶段反应速度呈递增的趋势,试简述这变化趋势发生的原因:
离子生成的量,发现开始阶段反应速度呈递增的趋势,试简述这变化趋势发生的原因:
25、第二主族元素R的单质及其相应氧化物的混合物12g,加足量水经完全反应后蒸干,得固体16g,试推测该元素可能为
A Mg B Ca C Sr D Ba
第Ⅱ卷
24、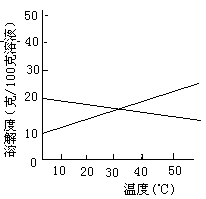 联合制碱法中关键的一步是把NH4Cl从几乎饱和的NaHCO3溶液中分离出来,为此根据NaCl和NH4Cl溶解度的差异,向混合溶液中通入某种气体,同时加入磨细的食盐,可析出不夹带NaHCO3的NH4Cl.NaCl和NH4Cl共同存在时的溶解度曲线如图所示,以下操作正确的是
联合制碱法中关键的一步是把NH4Cl从几乎饱和的NaHCO3溶液中分离出来,为此根据NaCl和NH4Cl溶解度的差异,向混合溶液中通入某种气体,同时加入磨细的食盐,可析出不夹带NaHCO3的NH4Cl.NaCl和NH4Cl共同存在时的溶解度曲线如图所示,以下操作正确的是
|
|
通入气体 |
温度控制 |
|
(A) (B) (C) (D) |
CO2 CO2 NH3 NH3 |
30~40℃ 0~10 ℃ 30~40 ℃ 0~10℃ |
23、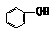
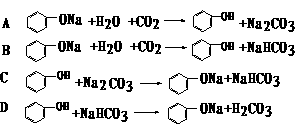 已知酸性强弱顺序为H2CO3> >HCO
已知酸性强弱顺序为H2CO3> >HCO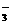 ,下列化学方程式正确的是
,下列化学方程式正确的是
22、下列离子方程式书写正确的是
A 过量氯气通入溴化亚铁溶液中 3Cl2+2Fe2++4Br-→6Cl-+2Fe3++2Br2
B 过量二氧化碳通入偏铝酸钠溶液中 CO2+2H2O+AlO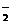 →Al(OH)3↓+HCO
→Al(OH)3↓+HCO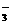
C 在溶液中亚硫酸氢铵与等物质的量氢氧化钠混合 NH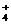 +HSO
+HSO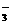 +2OH-→SO
+2OH-→SO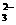 +NH3↑+2H2O
+NH3↑+2H2O
D 碳酸氢镁溶液中加入过量石灰水 Mg2++2HCO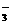 +Ca2++2OH-→CaCO3↓+2H2O+MgCO3↓
+Ca2++2OH-→CaCO3↓+2H2O+MgCO3↓
21、己知维生素A的结构简式可写为
式中以线示键,线的交点与端点处代表碳原子,并用氢原子数补足四价,但C、H原子未标记出来,关于它的叙述正确的是
A 维生素A的分子式为C20H30O B 维生素A 是一种易溶于水的醇
C 维生素A分子中有异戊二烯的碳链结构 D 1mol维生素A 在催化剂作用下最多可
与7molH2发生加成反应
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com