
题目列表(包括答案和解析)
23.(10分)如图,B为常见金属或非金属单质,有下列转化关系:
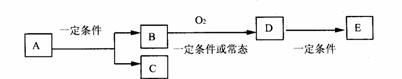
请回答以下问题:
①若C是可用作自来水消毒的气体,D、E是氧化物,D转化为E时,增加氧的质量约
是D物质总质量的25.8%,则A是_________。
②若E是酸酐,且为易挥发的晶体,则A是________;D转化为E的一定条件是________。
③若C是水,B是有机化合物,且是同系物中相对分子质量最小的物质,E能使紫色石
蕊试液变红色。则A是_______;A、B、D、E中易溶于C的物质是_______(填字母)。
21.(7分)物质A-H有下图所示转化关系(部分反应物、生成物没有列出)。其中,B的
浓溶液与单质X在加热时才能发生反应①,B的稀溶液与足量X发生反应②,向C溶
液中滴入KSCN溶液呈红色。
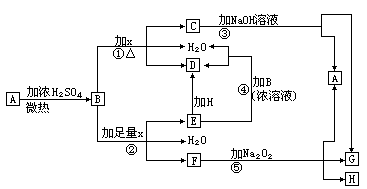
试填写下列空白:
(1)晶体A是(化学式)______________________ __。
(2)反应②的离子方程式:________ ______________。
(3)根据图示信息判断,足量B的浓溶液与单质X共热时能否产生E,说明理由(写出
化学方程式回答):_________________________________。
(4)在反应⑤中,若生成物G与H的物质的量之比为4∶1,写出F溶液与Na2O2反应
的化学方程式:______________________________________。
20.(11分)石油资源紧张曾是制约中国发展轿车事业,尤其是制约轿车进入家庭的重要因
素。为此,2001年5月,中国宣布将推广“车用乙醇汽油”。所谓乙醇汽油就是在汽油
里加入适量乙醇混合而成的一种燃料。
(1)下列叙述错误的是 ( )
A.乙醇汽油是一种新型的化合物
B.汽车使用乙醇汽油能减小有害气体的排放
C.工业常用裂化的方法提高汽油的产量
D.用玉米、高梁发酵可以制得乙醇
(2)乙醇燃烧不完全时,有CO生成。用下图装置确证乙醇燃烧产物有CO、CO2和H2O,
应将乙醇燃烧产物依次通过_________________。(按气流从左至右顺序填装置编号)
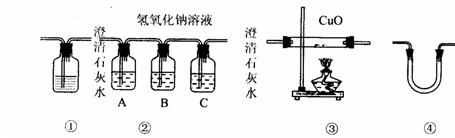
(3)实验时可观察到装置②中A瓶的石灰水变浑浊。A瓶溶液的作用是________ __;
B瓶溶液的作用是____ _______;C瓶溶液的作用是_____________。
(4)装置③的作用是____ _______。装置①中所盛的是________ __ ___溶液,
作用是 。
(5)装置④中所盛的固体药品是____________,可以确证的产物是____________。
(6)尾气应如何处理?_____________________________________________________。
19.(8分)回答下列问题:
(1)实验室利用铜丝和浓H2SO4反应的原理,制取少量二氧化硫气体,通常需要哪些
仪器?
(2)将SO2气体通入红棕色的溴水中,可以使溴水褪色。甲同学分析说褪色是由SO2的
还原性造成的;乙同学分析说褪色是SO2的漂白性造成的。请你根据SO2漂白性的
特点设计一个简单的实验,证明甲、乙两同学到底谁的分析正确?
1.62mol/L,则在该温度下各物质的平衡浓度中,不正确的是 ( )
A.c(N2O5)(平)= 1.44 mol/L B.c(N2O5) (平)= 0.94 mol/L
C.c(N2O)(平)= 0.44 mol/L D.c(N2O) (平)= 1.44 mol/L
第Ⅱ卷(非选择题 共78分)
18.加热N2O5时发生以下2个分解反应N2O5
 N2O3+O2 N2O3
N2O3+O2 N2O3 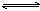 N2O+O2在
N2O+O2在
1L密闭容器中,加热4 mol N2O5,达到化学平衡时,c(O2)为4.50 mol/L,c (N2O3)为
17.目前,人们正在研究开发一种高能电池--钠硫电池。它以熔融的钠、硫为两极,以
 Na+导电的β′-Al2O3陶瓷作固体电解质,反应式如下:
Na+导电的β′-Al2O3陶瓷作固体电解质,反应式如下:
2Na+xS Na2Sx,以下说法正确的是 ( )
A.放电时,Na作正极,S极发生还原反应
B.若用此电池电解AgNO3溶液,当阳极产生标准状况下气体1.12升时,消耗金属钠2.3g
C.充电时,钠极与外电源的正极相连
D.充电时,阳极发生的反应为:Sx2--2e= xS
16.将NaHCO3溶液加水稀释时,下列各量中数值变大的是①c(CO32-)②c(H2CO3)③c(H+)
④c (OH-)⑤c(Na+) ( )
A.只有①②③ B.只有④⑤ C.只有③ D.只有②④
15.已知相同条件下,乙溶液的pH为x,甲溶液的pH为乙溶液pH的2倍,则甲溶液中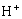
的物质的量浓度是乙溶液中H+物质的量浓度的多少倍 ( )
A.10x B.10-x C. 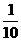 D.
D.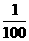
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com