
题目列表(包括答案和解析)
17.经测定某溶液中只含NH4+、C1- 、H+、OH-四种离子,下列说法错误的是 ( )
A.溶液中四种粒子之间不可能满足:c(C1-)>c(H+)>c(NH4+)>c(OH-)
B.若溶液中粒子间满足:c(NH4+)>c(C1-)>c(OH-)>c(H+)则溶液中溶质一定为:NH4Cl和NH3·H20
C.若溶液中粒子间满足:c(C1-)>c(NH4+)>c(H+)>c(OH-)溶液中溶质一定只有NH4Cl
D.若溶液中c(NH4+)=c(Cl-),则该溶液一定显中性
16.硝酸铜是制备Cu-Zn-AI系催化剂的重要原料,制取硝酸铜现有三种设计方案可供选用
①Cu与稀硝酸反应制取,3Cu+8HN03=3Cu(NO)Q+2NO↑+4H20
②Cu与浓硝酸反应制取,Cu+4HN03=Cu(NO3)2+2N02↑+2H20
③通氧气于铜屑与稀硝酸的体系中制取,2Cu+4HN03+02=2Cu(N03)2+2H2O
下列说法不正确的是 ( )
A.制取相同量的硝酸铜需硝酸的量③最少
B.制取相同量的硝酸铜①产生的有毒气体比②少
C.三种方案中硝酸的利用率③>②>①
D.三种方案的反应都可以在铁制容器中进行
15.以NA表示阿伏加德罗常数,下列说法正确的是 ( )
A.0.1molH3O+中含有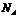 个电子
个电子
B.标准状况下,11.2L臭氧中含有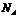 个氧原子
个氧原子
C.2g重氧水(H218O)、含有 个中子
个中子
D.84gNaHC03晶体中含有 个CO32-
个CO32-
14.X和Y两元素的阳离子具有相同的电子层结构。K元素的阳离子半径大于Y元素的阳离子半径。Z和Y两元素的核外电子层数相同,Z元素的原子半径小于Y元素的原子半径。则X、Y、Z三种元素原子序数的关系是 ( )
A.X>Y>Z B.Y>X>2 C.Z>X>Y D.Z>Y>X
13. 固体氧化物燃料电池是由美国西屋(Westinghouse)公司研制开发的。它以固体氧化锆一氧化钇为电解质,这种固体电解质在高温下允许氧离子(O2- )在其间通过。该电池的工作原理如图所示,其中多孔电极a、b均不参与电极反应。下列判断正确的是 ( )
固体氧化物燃料电池是由美国西屋(Westinghouse)公司研制开发的。它以固体氧化锆一氧化钇为电解质,这种固体电解质在高温下允许氧离子(O2- )在其间通过。该电池的工作原理如图所示,其中多孔电极a、b均不参与电极反应。下列判断正确的是 ( )
A.有O2参加反应的a极为电池的负极
B.有H:参加反应的b极为电池的正极
C.a极对应的电极反应式为O2+2H20-4e=40H-
D.该电池的总反应方程式为:2H2+02=2H2O
12.下列离子反应方程式正确的是 ( )
A.氯气与水反应:Cl2 +H2O =Cl-+2H++ClO-
B.氨气通入醋酸溶液中NH3+H+=NH4+
C.氯化铁溶液显弱酸性:Fe3++3H2O  Fe(OH)3 +3H+,
Fe(OH)3 +3H+,
D.碳酸氢钠溶液中加入过量石灰水HCO3-+OH-=CO32-+H2O
11.25℃时,将pH=x的H2S04溶液与pH=y的NaOH溶液等体积混合,反应后所得溶液pH=7。若x=1/6y,则x值为 ( )
A.2 B.3 C.4 D.5
10.某温度下,在一容积可变的容器中,反应2A(S)十B  2C(g);△H>0,达到平衡
2C(g);△H>0,达到平衡
时,A、B、C的物质的量分别为4mol、2mol、4mol,当采取下列措施能使平衡向正反应方向移动的是 ( )
A.升高温度 B.加入催化效果更好的催化剂
C.A、B、C均增加1mol D.A、B、C的量均减半
9.维生素E在国外美称之“生命奇迹丸”,是一种脂溶性维生素,对抗衰老等有特殊作用,
经研究发现维生素E有α、β、γ、δ四种类型,其结构简式如下: ( )
上述互为同分异构体的是
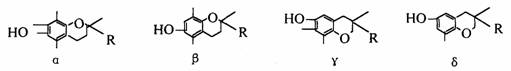
其中R为-CH2CH2CH2[CH(CH3)CH2CH2]2CH(CH3)2即:

A.α β B.β γ C.γδ D.α δ
8.过氧乙酸(CH3COOOH)是一种高效消毒剂,具有很强的氧化性和腐蚀性,他可由冰醋酸
与过氧化氢在一定条件下制得;他可以迅速杀灭多种微生物,包括多种病毒(如:SARS
病毒)、细菌、真菌及芽孢,有关过氧乙酸的叙述正确的是 ( )
A.过氧乙酸与羟基乙酸(HOCH2COOH)互为同分异构体
B.过氧乙酸可与苯酚混合使用
C.由过氧化氢与醋酸制取过氧乙酸的反应属于氧化还原反应
D.浓过氧乙酸中加入少许紫色石蕊试液,振荡后试液一定呈红色
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com