
题目列表(包括答案和解析)
2.人的血液总是维持在PH=7.37-7.45范围内,这是由于 ( )
A.人体中有大量水分(占体重70%)
B.血液中氯化钠保持一定浓度
C.排出的二氧化碳溶解在血液中
D.血液中HC03-和H2C03的浓度稳定在一定范围内
1.环境问题关系到人类的生存和发展,保护环境就是保护人类自己。从保护环境的角度出
发,目前最有发展前景的二次性餐具是 ( )
A.塑料餐具 B.不锈钢餐具 C.瓷器餐具 D.纸质餐具
28、(8分)将1molH2S和a molO2置于一个容积可变的容器内进行反应,维持容器内气体的压强(101kPa)不变,在120℃下测得反应前后容器中气体的密度分别为d1和d2。若a的取值范围不同,则H2S的氧化产物可能有如下三种情况:
(1)全部是SO2,此时a的取值范围是 ;
(2)全部是S,此时a的取值范围是 ,且d1 d2(填>、<、=)
(3)部分是S,部分是SO2时,此时a的取值范围是 。反应所
生成的SO2的物质的量为 mol,容器内气体物质的量之和为
mol(用a的代数式表示)
班级 姓名 座号
请将选择题答案填入下表
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
11 |
12 |
13 |
14 |
15 |
16 |
17 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
27、(6分)在标准状况下,在635mL水中需充入多少LHCl气体才能得到密度为1.18g/cm3,物质的量浓度为11.8mol/L的盐酸?
26、(18分)有一包含有AlCl3、MgCl2、NaBr三种物质的混合物粉末,按下列实验测定各成分的质量分数(已知氯化物在HCl气流中灼烧不会水解)
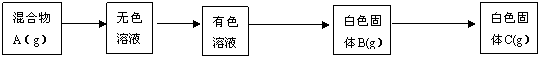 蒸馏水
通入足
蒸干后在HCl气
加蒸馏水溶解
蒸馏水
通入足
蒸干后在HCl气
加蒸馏水溶解
量X气体 流中灼烧冷却 加足量Y液过滤
(1)气体X是 ,溶液Y中的溶质是 ,最后的纯净物C是 。(6分)
(2)加入足量Y溶液的目的是
;过滤后,沉淀C必须用蒸馏水冲洗干净,其目的是 。(2分)
(3)写出B→C过程中的所有离子方程式:
。(4分)
(4)B→C过滤中滤液合格的标准是 ;若不合格,则必须进行的操作是 。(2分)
(5)原混合物中氯化铝的质量为 ;(2分)
(6)原混合物中溴化钠的质量分数为 。(2分)
25、(6分)某无色溶液可能含有下列钠盐中的几种:A-NaCl ;B-Na2S;C-Na2SO3 ;D-Na2S2O3;E-Na2SO4;F-Na2CO3,向此溶液中加入适量稀硫酸,有浅黄色沉淀析出,同时有气体产生。此气体有臭鸡蛋气味,可使澄清石灰水变混浊,不能使品红溶液褪色。则:
(1)不能使品红溶液褪色,说明该气体中不含 (填化学式);(2分)
(2)此无色溶液中至少存在哪几种钠盐?请写出全部的可能情况。(填序号4分)
① ② ③ ④ (不一定填满也可补充)
24、(8分)根据下图变化关系,回答问题:
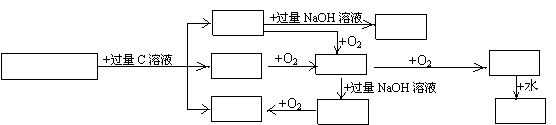
气体D A溶液
A、B混合溶液 沉淀E 气体X 气体Y
滤液F B溶液 C溶液
(1)气体D的分子式是 ,气体X的分子式是 ;(4分)
(2)A、B的混合溶液中,溶质A和B的物质的量n(A)和n(B)必须满足的条件是 ;(2分)
(3)生成沉淀E的离子方程式是 。
23、(6分)已知NaBiO3是黄色微溶于水的固体,Bi3+为无色,其硫酸盐易溶于水,将NaBiO3固体加入MnSO4和H2SO4的混合溶液中,加热,得紫色混合溶液,则:
(1)写出该反应的离子方程式 ;
(2)如将MnSO4改用MnCl2或将硫酸改用盐酸,则下列说法中可能的是
A、必定有黄绿色气体产生; B、必定无黄绿色气体产生;
C、溶液必定变成紫色; D、溶液可能不会变成紫色 (每空3分)
22、(8分)(1)在V LAl2(SO4)3溶液中,测得含Al3+的质量为a g,则Al2(SO4)3溶液的物质的量浓度为 ,SO42-的物质的量浓度为 。
(2)Wg碳酸钠晶体(Na2CO3·10H2O),溶于VmL水中,测得所得溶液的密度为d g/mL,则此溶液中溶质的质量分数为 ,溶液中溶质的物质的量浓度为 。 (每空2分,共8分)
21、工业制硫酸中沸腾炉中的反应方程式为 ,其中氧化产物是 ,若反应中共转移2.2mol电子,则被硫元素还原的O2为 g。 (每空2分,共6分)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com