
题目列表(包括答案和解析)
1、下列说法正确的是 ……………………………………………………………………………( )
A.强电解质一定是离子化合物
B.强电解质、弱电解质的电离都是吸热过程
C.强电解质的饱和溶液一定是浓溶液
D.强电解质在水中一定能全部溶解
2、NaHCO3溶解度比Na2CO3小
CO2溶解度比NH3小得多
1、200、230.8、10
1、B 2、BD 3、B 4、A、D 5、C
一定温度下在135gCuSO4溶液中取出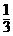 ,加入5g无水CuSO4恰好达到饱和.在剩下的
,加入5g无水CuSO4恰好达到饱和.在剩下的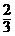 的CuSO4溶液中,加入过量的铁粉,待反应完全后,测得溶液的质量为89.5g.
的CuSO4溶液中,加入过量的铁粉,待反应完全后,测得溶液的质量为89.5g.
⑴求原135gCuSO4溶液是由多少克CuSO4·5H2O晶体和多少克水配制而成的.
⑵该温度下CuSO4的溶解度.
[能力训练答案]
2、在饱和Na2CO3溶液通入足量CO2,会有晶体析出,此晶体是________,析出此晶体的原因是因为_____________________.
在饱和食盐水中先通入足量的氨气,再通入足量CO2,会有NaHCO3晶体析出;若在饱和食盐水中先通入足量CO2,再通入氨气,往往没有晶体析出,原因是_____________________.
1、有一包含SiO2杂质的KNO3样品,将其加入到一定量的水中,充分搅拌.在10℃时,剩余固体
189g;在40℃时剩余固体103g;在75℃时,剩余固体10g,硝酸钾溶解度有关数据如下表:
|
温度(℃) |
10 |
40 |
50 |
75 |
80 |
|
溶解度(g) |
20.9 |
63.9 |
85.5 |
150 |
169 |
由此推断:加入水为________g,原样品质量为________g,含SiO2_______g.
5、浓度为30%的KNO3溶液冷却到下列何温度范围内,便有晶体开始析出( )
A、0-10℃ B、10℃-20℃ C、20℃-30℃ D、30℃-40℃
KNO3溶解度
|
温度(℃) |
0 |
10 |
20 |
30 |
40 |
|
溶解度(g) |
13.3 |
20.9 |
31.6 |
45.8 |
63.9 |
4、有xg浓度为10%的KNO3溶液,将其浓度变为20%,可采用的方法是( )
A、蒸发掉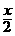 g水 B、蒸发掉溶剂质量的
g水 B、蒸发掉溶剂质量的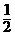
C、加入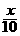 gKNO3晶体 D、加入
gKNO3晶体 D、加入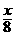 gKNO3晶体
gKNO3晶体
3、t1℃时KNO3的溶解度为S1g,t2℃时KNO3溶解度为S2g,将Ag t2℃时的KNO3饱和溶液降温至t1℃时,KNO3溶液的质量将变为(g)( )
A、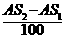 B、
B、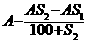 C、
C、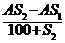 D、
D、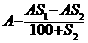
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com