
题目列表(包括答案和解析)
24、(7分)已知有机化合物A为具有香味的液体,从A出发有下列变化。同时经有关实验证实:1 mol A在完全燃烧后产生8 mol 二氧化碳;D为最简单的芳香烃;F可发生银镜反应。
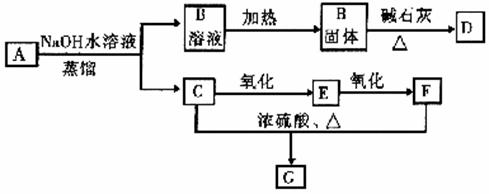
请回答下列问题:
(1) A、B物质的名称分别是 、 ;E物质的水溶液通常叫做 ;
(2) 写出下列变化过程的化学方程式:
 ①C+F G
;
①C+F G
;
 ②B D
。
②B D
。
23、已知与外加电源正极相连的电极为电解池的阳极,与外加电源负极相连的电极为电解池的阴极,在以石墨为电极电解时,电解质溶液中的阴离子在阳极发生氧化反应,电解质溶液中的阳离子在阴极发生还原反应,又知阳离子得电子的能力与其对应金属的金属活动性顺序相反(注意:Fe3+>Cu2+>Fe2+ ),阴离子失电子的能力为S2– > I– > Br– > Cl– > OH–> 含氧酸根离子> F–。如图所示:以石墨为电极电解A的水溶液,并做下面一系列实验,试根据实验现象完成下列问题。电解质A的水溶液焰色反应呈浅紫色。(1+1+2+2+1+1=8分)

(1)写出A的化学式为 ,E的名称为 ;
(2)I与F作用的离子方程式是 ;
(3)G加入L后产生的白色沉淀到生成红褐色沉淀H的化学方程式:
;
(4)用两个最直接的离子方程式来证明Fe3+、Cu2+、Fe2+的氧化性强弱顺序是Fe3+>Cu2+>Fe2+
① ;② 。
22、下图中每一个方格表示一种反应物或生成物(反应中的水以及部分反应中生成的常温下呈气态的物质均已略去)。已知D是一种盐,焰色反应是浅紫色,且B生成A的反应的另一种气体产物是空气的主要成分之一。
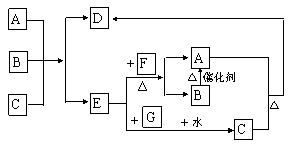
⑴ A是 ,B是 ,G是 (用化学式表示);
|
 ⑵ E+G+水 C的化学反应方程式
;
⑵ E+G+水 C的化学反应方程式
;
 ⑶ E+F
A+B的离子反应方程式
;
⑶ E+F
A+B的离子反应方程式
;
⑷ A、B、C三种物质反应的物质的量之比为 。(1x3+2x3=9分)
21、草酸晶体的组成可表示为H2C2O4·xH2O,为测定x值,进行下述实验:① 称取w g 草酸晶体配成100.00 mL水溶液;② 取25.00 mL所配的草酸溶液置于锥形瓶中,加适量稀H2SO4后,用浓度为a mol/L的KMnO4溶液滴定,所发生的反应为:
2 KMnO4 + 5 H2C2O4 + 3 H2SO4 === K2SO4 + 10 CO2 + 2 MnSO4 + 8 H2O
反应生成的MnSO4在水溶液中基本无色。试回答下列问题:
(1)实验滴定时,KMnO4溶液应装在 式滴定管中;
(2)在滴定过程中,达到滴定终点的标志是 ;
(3)若滴定过程中,用少量蒸馏水洗锥形瓶内壁,再继续滴定,则所测得的x值 (填“偏大”、“偏小”或“无影响”下同);记录测定结果时,滴定前平视刻度线,滴定到达终点时,又俯视刻度线,将导致滴定结果 ;若在滴定终点后,因操作错误多加1滴KMnO4溶液则应采取何措施 。若滴定过程中,液体飞溅出来,则应采取何措施 。
(4)若滴定过程中,共用去a mol/L KMnO4溶液 V ml,由此可计算出草酸晶体结晶水的x值为 。(1x6+2=8分)
20、实验:(每空2分,共16分,每空只有全对才得分,否则不得分)
有一瓶澄清的溶液,其中可能含有NH4+、K+、Na+、Mg2+、Ba2+、Al3+、Fe3+、Cl–、I–、NO3–、CO32-、S2–、SO42–、AlO2–、SO32–、MnO4– , 取该溶液进行以下实验:
(1) 取PH试纸检验,溶液呈强酸性,可以排除 离子的存在。
(2) 取出部分溶液,加入少量CCl4及数滴新制氯水,经振荡后CCl4层呈紫红色,可以排
除 离子的存在。
(3) 另取出部分溶液逐渐加入NaOH溶液,使溶液从酸性逐渐变为碱性,在滴加过程中和滴加完毕后,溶液均无沉淀产生,则又可以排除 离子的存在。
(4) 取出部分上述碱性溶液加Na2CO3溶液后,有白色沉淀生成,证明 离子存在,又可排除 离子的存在。
(5) 将(3)得到的碱性溶液加热,有气体放出,该气体能使湿润的红色石蕊试纸变蓝。
根据上述实验事实确定:该溶液中肯定存在的离子是 ;肯定不存在的离子是 ;还不能确定是否存在的离子是 。
19、KClO3和浓盐酸在一定温度条件下反应会生成黄绿色的易爆物ClO2,其变化可表示为:






 KClO3+ HCl(浓)-- KCl+ ClO2↑+ Cl2↑+
KClO3+ HCl(浓)-- KCl+ ClO2↑+ Cl2↑+
⑴ 请完成该化学方程式并配平(未知物化学式和系数填入框内);
⑵ 浓盐酸在反应中显示出来的性质是 (填写序号);
①只有还原性 ②还原性和酸性 ③只有氧化性 ④氧化性和酸性
⑶ 产生0.1 molCl2,则转移的电子的物质的量为 mol;
⑷ ClO2具有很强的氧化性,因此常被用作消毒剂,其消毒的效率(以单位质量得到的电子
数表示)是Cl2的 倍。 (2x4=8分 )
18、有一可逆反应,2A(g)
+ 3B(g) 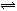 xC(g) +4D(g);若将按下列两种配比的物质:
xC(g) +4D(g);若将按下列两种配比的物质:
(1) 0.8 mol A,1.2 mol B,1.2 mol C,2.4 mol D;(2)1.4 mol A,2.1 mol B,0.6 mol C,1.2 mol D
放入一容积不变的密闭容器中,保持温度不变,达平衡后,两种情况C的百分含量相等,则方程式中的x值为:
A、1 B、2 C、3 D、4
第Ⅱ卷(非选择题部分,共78分)
17、有一铁的氧化物样品,用5 mol/L盐酸100 mL恰好完全溶解,所得溶液还能吸收标况下的氯气1.12 L,Fe2+全部被氧化为Fe3+,则该氧化物的化学式可表示为:
A、Fe2O3 B、Fe3O4 C、Fe4O5 D、Fe2O7
16、现代的防晒霜中含有能吸收紫外线的防晒剂,例如:对氨基苯甲酸丁酯,它能吸收到达皮肤上99%的紫外线,具有十分理想的防晒效果。下列关于对氨基苯甲酸丁酯的说法正确的是:
A、从有机物分类角度看,它属于氨基酸类、酯类、芳香烃类
B、它能与NaOH溶液反应,也能与盐酸反应
C、甲酸丁酯基(-COOC4H9)有3种不同结构
D、它的分子式为C11H15NO2
15、将SO2通入BaCl2溶液至饱和,未见沉淀生成,继续通入另一气体则有沉淀。则通入的气体可能是: A、CO2 B、NH3 C、NO2 D、CH4
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com