
题目列表(包括答案和解析)
8.工业上电解食盐水的阴极区产物是( )
(A)氯气 (B)氢气和氯气 (C) 氢气和氢氧化钠 (D) 氯气和氢氧化钠
7.电解氧化铝和冰晶石的熔融体时。若电路中有50 mol电子通过,可以得到金属铝的质量是( )
(A) 0.45 kg (B) 2.7 kg (C) 0.9 kg (D) 5.4 kg
6.用惰性材料作电极分别电解1 mol·L-1的下列溶液,电解过程中,溶液浓度逐渐减小的是( )
(A) 稀硫酸
(B) 氢氧化钠溶液
(C) 硝酸钾溶液
(D) 氯化铜溶液
5.电解下列溶液,pH明显下降的是( )
(A) 硝酸银溶液
(B) 稀硫酸
(C) 硝酸钾溶液
(D) 氯化钠溶液
4.电解水时在水中加入少量硫酸的目的是( )
(A) 增加溶液中c(H+)和c(OH-)的浓度
(B) 增大水的离子积常数
(C) 增大水的电离度
(D) 增强水的导电性,加快电解速度
3.下列关于铜电极的叙述正确的是( )
(A) 铜锌原电池中铜是正极
(B) 用电解法精炼粗铜时粗铜作阴极
(C) 在镀件上电镀铜时可用金属铜作阳极
(D) 电解稀硫酸制氢气、氧气时用作阳极
2.下列那种工业生产的过程不必使用电解的方法( )
(A) 由光卤石制镁
(B) 由黄铁矿制硫酸
(C) 由铝土矿制铝
(D) 用海水制氢氧化钠
1.电镀银时,下列物质可作阳极的是( )
(A)Ag (B) Cu (C) Pt (D) C(石墨)
15.有两只密闭容器A和B,A容器有一个移动的活塞,能使容器内保持恒压,B容器保持恒容。起始时向这两只容器中分别充入等量的体积比为2∶1的SO2和O2的混合气体,并使A和B容积相等(见图)。
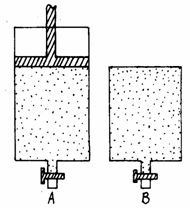 在保持400℃条件下使之发生反应:
在保持400℃条件下使之发生反应:
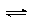 2SO2 + O2 2SO3
2SO2 + O2 2SO3
填写下列空格:
(1)达到平衡时所需的时间A容器比B容器 ,A容器中SO2的转化率比B容器 中SO2的转化率 。
(2)达到(1)所述平衡后,若向两容器中通入数量不多的等量氩气,A容器中化学平衡
移动,B容器中化学平衡 移动。
(3)达到(1)所述平衡后,若向两容器中通入等量的原反应气体,再达到平衡时,A容 器中SO3的百分含量 (增大、减少、不变);B容器中SO3的百分含量 (增大、减小、不变)。
14.常温常压下,A、B、C、D均为气态。A与B可发生可逆反应:A + B?C + n D。若将2 mol A和2 mol B混合充入体积可变的密闭容器中,在不同条件下达平衡时C的浓度如下:
|
温度 |
压强(Pa) |
C平衡浓度(mol/L) |
|
25 ℃ |
1×105 |
1.0 |
|
25 ℃ |
2×105 |
1.8 |
|
25 ℃ |
4×105 |
3.2 |
|
25 ℃ |
5×105 |
6.0 |
(1)可逆反应中系数n取值范围为___________________,理由___________________
_____________________________________________________________________。
(2)在5×105 Pa时,D的状态为____________________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com