
题目列表(包括答案和解析)
1、分子组成和结构:甲烷的分子组成确定是经典确定分子式的方法,其步骤是:先测定标准状况甲烷的密度根据其密度。求出分子量M=e×22.4=16,通过对甲烷进行的定量测定: 碳的百分含量75%, 氢的百分含量25%,从而得出: C: , 其化学式为CH4,而现在很多涉及有关分子式的计算均由这个经典求法衍变而来,现举二例:
, 其化学式为CH4,而现在很多涉及有关分子式的计算均由这个经典求法衍变而来,现举二例:
例1:吗啡和海洛因都是严格查禁的毒品,吗啡分子含C: 71.58%, H: 6.67%, N: 4.91%, 其余为O, 已知其分子量不超过300,试求:
(1)吗啡的分子量;(2)吗啡的分子式
(3)已知海洛因是吗啡的二乙酸酯,试求海洛因的分子量和分子式
解析:本题从表面看与求甲烷分子组成不相同,因为分子量未知.显然,不知道分子量,仅知道各元素及其百分含量可以求出分子式即先确定最简式,然后,根据分子量不超过300,可以确定分子量和分子式.姑且不谈这种求法,只能先得出分子式,再得出分子量与题目要求的顺序相反,更主要的是这种求法很繁,很难得出准确的最简式.这时需要逆向思维:根据分子量和元素含量可确定原子个数,反之,可否根据原子个数和元素含量确定分子量?因为有机物中N原子数一般比较少,假设吗啡中只含一个N原子则分子量M=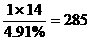 <300,则假设成立, C:
<300,则假设成立, C: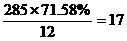 , H:
, H:  , O:
, O: ,C17H19NO3
,C17H19NO3
海洛因是吗啡的二乙酸酯,即吗啡+2CH3COOH→海洛因+2H2O
分子量=285+2×60-2×18=369 分子式:吗啡中所有原子+2CH3COOH-2H2O→C21H23NO5
例2:A、B都是芳香族化合物,1mol A水解得到1mol B和1mol醋酸,A、B的式量都不超过200,完全燃烧都只生成CO2和H2O,且B分子中碳和氢元素总的质量分数为0.652, A溶液具有酸性,不能使FeCl3溶液显色.
(1)A、B式量之差为________________(2)1个B分子中应该有______个氧原子.
(3)A的化学式是___________________(4)B可能的结构简式是______________.
解析:本题将经典求化学式的方法与有机物的化学性质有机的结合,并运用推理的方法来确定化学式,这是考查同学们综合运用知识能力的好题.
具体解法如下:由于A能水解且生成B和CH3COOH,说明A可能是酯,显然:
A+H2O→B+CH3COOH 根据质量守恒定律: MA+18=MB+60
MA-MB=60-18=42 得出式量之差为42, 同时得到MB≤200-42=158(因为A、B式量均不超过200,而B的式量又比A小42),.又知A属于酯,但有酸性.但不使FeCl3显色说明又属于羧酸(不是酚),那么A水解后的B至少应含有3个氧原子(A本身至少含一个-CCOH, 水解后B相当于醇,又含至少一个-OH),且B中O元素的质量分数为1-0.652=0.348. 若B中只含3个氧原子MB= <158合理.所以B中只含3个氧原子.如何得出A、B的分子式?根A、B均为芳香族化合物且B中有5个不饱和度,B的分子式为CnH2n-8O3,即14n-8+48=138,n=7 A+H2O→C7H6O3+CH3COOH A的分子式C9H8O4(原子守恒法)
<158合理.所以B中只含3个氧原子.如何得出A、B的分子式?根A、B均为芳香族化合物且B中有5个不饱和度,B的分子式为CnH2n-8O3,即14n-8+48=138,n=7 A+H2O→C7H6O3+CH3COOH A的分子式C9H8O4(原子守恒法)





 OH OH OH
OH OH OH


 B可能的结构简式为 -COOH、
B可能的结构简式为 -COOH、
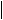 -COOH
-COOH
COOH
甲烷的分子结构:正四面体结构,由此得出多碳原子的烷烃C原子不可能在一条直线上。
5、有机反应多数速率慢,需催化剂,副反应多,反应复杂。
有机物具有以上共同特点的原因:以共价键结合,形成分子晶体。有机物与无机物性质上的差异是相对
 的。如:NaHCO3与Na2CO3的溶解性与有机酸盐的溶解性一致,即酸式盐溶解度小于正盐。且有机物与无机物可相互转化。如:NH4CNO △ CO(NH2)2
的。如:NaHCO3与Na2CO3的溶解性与有机酸盐的溶解性一致,即酸式盐溶解度小于正盐。且有机物与无机物可相互转化。如:NH4CNO △ CO(NH2)2
4、绝大多数热稳定性差,易燃烧(CCl4例外)
3、易溶于有机溶剂,难溶于水。
有机物特点:1、种类繁多:接近一千万种,原因是①碳原子有四个价电子,通过共价键结合其它原子②碳与碳之间形成C-C共价键的长链③普遍存在同分异构现象。
2、绝大多数属于非电解质(CH3COOH等除外)
5.把淀粉溶液溶于沸水中,制成淀粉胶体。
(1)鉴别水溶液和胶体可以利用的方法是
。
(2)60 ℃左右时,在淀粉胶体中加入淀粉酶,充分反应。然后把反应后的全部液体装入半透膜袋里,系紧袋口,并把它悬挂在盛有蒸馏水的烧杯里。从半透膜袋里析出的物质是
,该操作的名称是 。
4.铁酸钠(Na2FeO4)是水处理过程中的一种新型净水剂,它的氧化性比高锰酸钾更强,本身在反应中被还原为Fe3+离子达到净水的目的。它是由硝酸铁、氢氧化钠和氯气在一定条件下制得的,同时还有硝酸钠、氯化钠等生成,写出其反应的化学方程式_______________________________________________________制铁酸钠的反应中________元素被氧化,转移电子总数是__________,铁酸钠之所以有净水作用,除了杀菌外,另一个原因是_______________________________________________________________________
__________________________________________________
3.分别设计化学实验,用最佳的方法证明明矾溶于水时发生的下面变化:供选用的仪器和药品:明矾溶液、甲基橙试液、石蕊试液、酚酞试液、pH试纸、氢氧化钠溶液、酒精灯、半透膜、电泳仪、聚光束仪。
①证明明矾发生了水解反应_________________________________________
②证明其水解反应是一个吸热反应___________________________________
③证明生成了胶体溶液_____________________________________________
2. 选择适宜的提纯或分离的方法,将操作名称填入下列空白中
⑴除去硝酸钾晶体中少量的氯化钠________________
⑵除去粗铜中混有少量锌_________________
⑶除去二氧化碳中混有少量氯化氢_____________
⑷除去氯化钾中混有少量的二氧化锰_____________
⑸除去氢氧化铁溶胶中的氯离子_____________
1. 一般说来,金属氢氧化物、金属氧化物的胶体微粒带_____电荷,在电场作用下向___________极运动,而非金属氧化物、金属硫化物的胶体微粒带_______电荷,在电场作用下向_____极运动。若将氢氧化铁溶胶和碘化银溶胶混合,将会发生_________________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com