
题目列表(包括答案和解析)
3、拟(类)卤素--这些虽然不含卤素原子,但其性质与卤素相似.如
(CN)2、(SCN)2、(SeCN)2、(OCN)2等。请写出下列化学方程式
(CN)2+H2O-- Fe+(SCN)2--
 MnO2+HSCN △ (CN)2+CH2=CH2
MnO2+HSCN △ (CN)2+CH2=CH2
2、卤素互化物--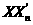 (n=1,3,5,7)其化学性质与卤素单质相似,具有强氧化性.
(n=1,3,5,7)其化学性质与卤素单质相似,具有强氧化性.
例:已知BrFn与水按3:5物质的量比反应,生成HF、HBrO3、O2和Br2,且O2和Br2物质的量相等.请回答:
(1)n= (2)氧化产物是 (3)1mol水可还原 mol BrFn?
解析:(1)根据题意:反应式为3BrFn+5H2O=3nHF+aHBrO3+bBr2 +bo2
由于O2与Br2物质的量相等,且反应物只含3mol Br元素,则a=b=1根据H原子守恒3n+1=5×2 n=3.
(2)元素化合价升高后的产物是氧化产物,显然为HBrO3和O2.
(3)还原1mol BrF3必提供3mol电子,而1mol水只能提供2mol电子则可还原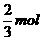 BrF3.
BrF3.
1、 化学性质--Cl原子最外层有7个电子,表现强氧化性.
(1)与金属反应--Cl2与绝大多数金属能反应(除极少数不活泼金属),且变价金属(如Fe)一般能氧化到最高价.
2Na+Cl2=2NaCl(白烟)
 2Fe+3Cl2
△ 2FeCl3(棕褐色)
2Fe+3Cl2
△ 2FeCl3(棕褐色)
思考:常温Fe能否与干燥Cl2反应?你能举出实例吗?
(不能,除非潮湿Cl2.液氯用钢瓶盛装运输)
 Cu+Cl2 点燃 CuCl2(棕黄色的烟)
Cu+Cl2 点燃 CuCl2(棕黄色的烟)
注意:由Cu在Cl2中燃烧的现象说明无水CuCl2为棕黄色固体,只有溶于水其颜色由于浓度不同显绿色或蓝色.
 思考:[CuCl4]2-+4H2O [Cu(H2O)4]2++4Cl-
思考:[CuCl4]2-+4H2O [Cu(H2O)4]2++4Cl-
(绿色) (蓝色)
在此平衡体系中,改变下列条件:①加入适量NaCl ②加入适量AgNO3 溶液 ③加入适量水,溶液颜色将如何改变?
(①绿色加深 ②蓝色变深 ③变蓝色)
CuCl2固体与AlCl3相似,亦为共价化合物,且形成的是多聚体(CuCl2)n
(2)与非金属的反应
氯气除与H2反应外,还能与P、S、Si等非金属反应
 2P+3Cl2 点燃 2PCl3 PCl3+Cl2=PCl5
2P+3Cl2 点燃 2PCl3 PCl3+Cl2=PCl5
反应现象:有白色烟雾生成--中学化学中唯一的烟、雾同时生成的一个反应.
其中PCl3具有重要用途--生产农药敌百虫.
PCl3、PCl5均能水解 PCl3+3H2O=H3PO3+3HCl PCl5+4H2O=H3PO4+5HCl
 Si+2Cl2 高温 SiCl4--工业制单晶硅(高纯硅)的重要反应.
Si+2Cl2 高温 SiCl4--工业制单晶硅(高纯硅)的重要反应.
(3)与化合物的反应
 ①水 Cl2+H2O HCl+HClO(歧化反应)--非常重要的平衡,混合液称氯水,氯水存在的微粒
①水 Cl2+H2O HCl+HClO(歧化反应)--非常重要的平衡,混合液称氯水,氯水存在的微粒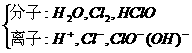
思考:a、如何证明氯水中存在Cl2、H+、Cl-、HClO?
b、0.224L(标况)Cl2溶于2L水中,Cl2、Cl-、HClO物质的量之和 0.01mol?(填大于、小于或等于)
②碱 Cl2+2NaOH=NaCl+NaClO+H2O--主要用来吸收多余Cl2
思考:标准状况aL H2与Cl2混合气体光照爆炸后的产物恰好使bmol NaOH完全转化为盐,则b与a的关系可以是
(0<b≤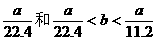 )
)
2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O--工业用来制取漂白粉.
思考:a、工业上为什么用Cl2来制取漂白粉?
b、漂白粉的主要成分是什么?有效成分是什么?其漂白原理是什么?
c、自来水净化过程可用液氯和绿矾来净化消毒,也可用氯胺(NH2Cl)来杀菌消毒、请用化学方程式表示净化消毒过程.
(a、形成比次氯酸更稳定的比次氯酸盐,便于运输、保存.
b、CaCl2和Ca(ClO)2,Ca(ClO)2, Ca(ClO)2+H2O+CO2=CaCO3+2HClO
 c、Cl2+2Fe2+=2Fe3++2Cl-, Fe3++3H2O Fe(OH)3(胶体)+3H+--净化
c、Cl2+2Fe2+=2Fe3++2Cl-, Fe3++3H2O Fe(OH)3(胶体)+3H+--净化
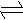
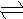 Cl2+H2O HClO+HCl--杀菌 NH2Cl+H2O NH3+HClO)
Cl2+H2O HClO+HCl--杀菌 NH2Cl+H2O NH3+HClO)
③其它还原性化合物
S2-(H2S)+Cl2-- Br-+Cl2-- Fe2++Cl2--
SO32-(SO2)+Cl2+H2O-- I-+Cl2--
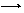 取代反应CH4+Cl2 光 CH3Cl+HCl
取代反应CH4+Cl2 光 CH3Cl+HCl
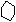
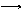
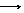 ④有机物
o +Cl2 Fe o-Cl+HCl
④有机物
o +Cl2 Fe o-Cl+HCl
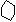
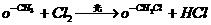
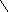 加成反应 CH2=CH2+Cl2 CH2-CH2
加成反应 CH2=CH2+Cl2 CH2-CH2
Cl Cl
21(14分)经测定,葡萄糖的分子式为C6H12O6,分子内含有5个羟基和1个醛基,每次用1mol葡萄糖溶液进行下列实验:
(1)用葡萄糖做银镜反应时,需要[Ag(NH3)2]OH mol,反应后葡萄糖转变为
(填物质名称)
(2)和醋酸反应生成酯,理论上完全酯化需醋酸 g
(3)一定条件下,与金属钠完全反应,能产生标准状况下 L气体
(4)用它发酵制取酒精的化学方程式为:
(5)用它发酵制取乳酸的化学方程式为:
(6)与新制的Cu(OH)2碱性悬浊液共热,反应的化学方程式为:
22 (6分)使用某些有机物材料给环境所造成的“白色污染”后果十分严重。最近研究的一些分解塑料,如:
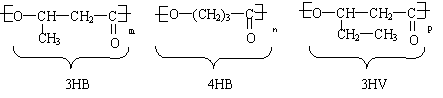
有良好的生物适应性和分解性,能自然腐烂分解。已知3HB的单体的单体叫3-羟基丁酸,则4HB的单体叫 ,当两分子4HB的单体脱水时,生成的环酯
的结构简式为 ,3HV单体的结构简式为
23 (4分)怎样用简单的实验操作鉴别聚乙烯、聚氯乙烯、聚苯乙烯和酚醛树脂四种塑料,写出简要步骤。
24 (11分)今有一个“多肽”,其分子式是C55H70N10O19,已知将它彻底水解只得到下列4种氨基酸
则(1)该多肽是 (填汉字)肽。(2)该多肽水解后,有 个谷氨酸。
(3)该多肽水解后,有 个苯丙氨酸。
25 (5分)就生活中常见的现象,填写有机物发生反应的反应类型:
(1)变质的油脂有难闻的哈喇味,这是因为油脂发生了
(2)手不小心沾上浓硝酸,皮肤变黄色
(3)吃饭时多咀嚼米饭,感觉有甜味
(4)葡萄糖用于制热水瓶胆
(5)烹调鱼时,往往既放醋又放料酒
26 (10分)三位同学在验证蔗糖的部分性质时,分别进行了如下实验:
甲同学:取表面已潮湿的冰糖晶体配成溶液,加入新制的Cu(OH)2悬浊液后加热,结果产生红色沉淀。结论:蔗糖是还原性糖。
乙同学:取表面已潮湿的冰糖晶体,用蒸馏水冲洗2-3次,再配成溶液,加入新制的Cu(OH)2悬浊液后加热,结果无红色沉淀产生。结论:蔗糖不是还原性糖。
丙同学:取表面已潮湿的冰糖晶体,用蒸馏水冲洗2-3次,再配成溶液,滴入一定量硫酸,水浴加热后,冷却。取水解液,加入新制的Cu(OH)2悬浊液后加热,结果无红色沉淀产生。结论:蔗糖的水解产物中没有还原性糖。
请分析这三位同学的实验,你认为 同学的结论错误。你认为错误的理由是
三 计算题(共10分)
27 由人尿分离出来的结晶化合物A的熔点为1870C-1880C。对A做下列实验:
(1) 测得A的蒸气密度为8.0g/L(已折算成标准状况),取17.92gA完全燃烧,生成的
气体通过浓硫酸,浓硫酸增重8.10g。剩余气体通过碱石灰,气体质量减轻39.6g。另取17.92gA完全分解,可得标准状况下氮气1.12L,试通过计算确定A的分子式。
(2) 又知A和足量6mol/L盐酸混合加热可以完全水解,1mol A水解生成1mol B和
1mol C。已知A、B、C三物质中都含有一个羧基,B物质仍由碳、氢、氧元素组成,其物质的量之比为7∶6∶2,C是最简单的氨基酸,试写出A、B、C的结构简式。
作者:上虞章镇中学 董斌开
预备题:
1、用一种隔膜(只有水分子能自由通过,而直径比水分子大的溶质分子不能通过)把水槽隔成完全相同的甲、乙两室,相同温度下,甲室装入1%的尿素溶液,乙室装入等体积a%的葡萄糖溶液,若两溶液密度近似为1g/cm3,且水分子的扩散速率也相同,则a%的近似值是(已知这种扩散速率语单位体积内溶质的微粒数成反比,而与液体的压强成正比)( B )
A 4% B 3% C 2% D 1%

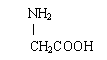
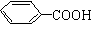
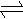
3、当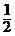 ≤x<1为烷烃,当x=1为烯烃,当1<x≤2为炔烃
≤x<1为烷烃,当x=1为烯烃,当1<x≤2为炔烃
2、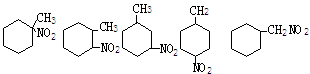 (1) C10H8、C9H20、C8H16O、C7H12O2、C6H8O3
(1) C10H8、C9H20、C8H16O、C7H12O2、C6H8O3
(2)
1、27种,烯酚或环酚类。
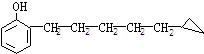
和
3、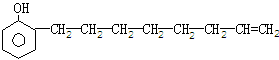 某链烃[CnHm]属烷、烯或炔烃中的一种,使若干克该烃在足量O2中完全燃烧,生成xLCO2和1L水蒸气(120℃ 1.03×105Pa)试根据x的不同取值范围来确定该烃所属类型及其分子内所含碳原子n值。
某链烃[CnHm]属烷、烯或炔烃中的一种,使若干克该烃在足量O2中完全燃烧,生成xLCO2和1L水蒸气(120℃ 1.03×105Pa)试根据x的不同取值范围来确定该烃所属类型及其分子内所含碳原子n值。
[能力训练答案]
2、有机物A的分子量为128,燃烧只生成CO2和H2O。
(1)写出A的可能分子式5种________、________、_________、_________、_________。
(2)若A能与纯碱溶液反应,分子结构有含一个六元碳环,环上的一个H原子被-NH2取代所得产物为B的同分异构体甚多,其中含有一个六元碳环和一个-NO2的同分异构有(写结构简式)_________________________________________
1、化合物A[ ]的同分异构体B中无甲基,但有酚羟基符合此条件的B的同分异构体有_______种,从结构上看,这些同分异构体可属于________类,写出每类同分异构体中的一种同分异构体的结构简式_________________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com