
题目列表(包括答案和解析)
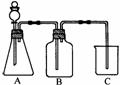
20.为了证明铜与稀硝酸反应产生一氧化氮,某校学生实验小组设计了一个实验,其装置如下图所示(加热装置和固定装置均已略去),B为一个用金属丝固定的干燥管,内装块状碳酸钙固体;E为一个空的蒸馏烧瓶;F是用于鼓入空气的双连打气球。

(1)实验时,先将B装置下移,使碳酸钙与稀硝酸接触产生气体,当C处产生白色沉淀时,立刻将B装置上提,使之与稀硝酸分离。该组学生设计此步操作的目的为_______.
(2)将A中铜丝放入稀硝酸中,给装置A微微加热,在装置A中产生无色气体,其反应的化学方程式为_______________________________________________;
装置E中开始时出现浅红棕色气体,用F向E中鼓入空气后,可观察到烧并E内气体颜色加深,产生上述现象的原因是___________________________。
一段时间后,C中白色沉淀溶解,其原因是______________________;
(3)装置D的作用是________________________________________ 。
(4)若将E瓶用冰盐水冷却,得到微黄色液体,其成分是 ,理由是
。
19.(1)为确认CH3COOH、H2CO3和H4SiO4的酸性强弱,有人设计用如右图装置,一次实验即可达到目的(不必再选用其它酸性溶液)。请依据此实验填空:
①锥形瓶内装某可溶性正盐固体,分液漏斗中所盛试剂是 。
②装置B所盛的试剂是 ;装置B所盛试剂的作用是 。
③装置C中所盛的试剂是 ;出现的现象是 。
(2)Ca3(PO4)2 、CaHPO4 均为难溶于水的白色固体。某同学向Na2HPO4 溶液中滴加CaCl2 溶液至恰好反应,生成白色沉淀。试设计一个简单的实验方案,来证明所生成的白色沉淀是Ca3(PO4)2 还是CaHPO4
实验原理: 。
实验用品及试剂:烧杯、玻璃棒、试管;石蕊试液、酚酞、PH试纸
实验步骤、现象、结论(可不填满):
A.___________________________________________________________
B.__________________________________________________________
C.__________________________________________________________
D.__________________________________________________________
17.实验室常以纯净的无水Na2CO3作基准物,用未知浓度的盐酸滴定之,通过此法测定盐酸的准确浓度。下列判断正确的是
A.若所取Na2CO3在空气中受过潮,则被测盐酸浓度偏高
B.若所取Na2CO3中混有NaOH,则所测盐酸浓度偏高
C.若用酚酞作为滴定指示剂,则被测盐酸浓度偏低
D.滴定前盛放盐酸的滴定管玻璃活塞下端有气泡,滴定过程中气泡被液流冲出,则被测盐酸的浓度偏低
18 将18g某混合气体通过足量的Na2O2固体充分反应后固体增重2g,则该混合气体不可能是
A.H2O(g), N2 B.H2O(g), CO2 C.CO2,O2 D.CO2 ,H2O(g), O2
 第Ⅱ卷(非选择题
共78分)
第Ⅱ卷(非选择题
共78分)
15.乙烯在硫酸催化作用下的水化合成乙醇经过下列步骤;首先在较低温度下乙烯被浓H2SO4吸收: CH2=CH2十H2SO4(浓)→CH3CH2OSO3H (I) 然后生成物(I)再进一步吸收乙烯,产生生成物(II): CH3CH2OSO3H + CH2=CH2→( CH3CH2O)2SO2 (II)
加水时,生成物(I)和(II)都与水反应生成乙醇:
CH3CH2OSO3H +H2O→CH3CH2OH+H2SO4 (CH3CH2O)2SO2 + 2H2O→2CH3CH2OH+H2SO4
下列叙述中正确的是:
(1)化合物I、II都属于酯类;
(2)上述生成I、II化合物的反应都属于酯化反应(酸和醇起作用生成酯和水的反应叫做酯化反应);
(3)上述生成I、II化合物的反应都属于加成反应;
(4)上述生成醇的反应都属于取代反应
A.只有(1) B.只有(1)(3) C.只有(1)(3)(4) D.(1)(2)(3)(4)
16.蒽与苯炔反应生成化合物X:

X中一个氢原子被甲基取代的所有异构体数为
A.5种 B.4种 C.3种 D.2种
13.下列离子方程式书写正确的是
A FeCl2溶液中通入Cl2:Fe2++Cl2===Fe3++2Cl-
B 澄清石灰水与少量小苏打溶液混合:Ca2+十OH-+HCO3-===CaCO3↓+H2O
C FeS固体放人稀硝酸溶液中:FeS+2H+====Fe2++H2S↑
D AlCl3溶液中加入过量氨水:Al3++4OH-===AlO2-+2H2O
14.在一恒定容积的容器中充入2mol的A和1mol的B发生反应:2A(g)+B(g) XC(g)。达到化学平衡后,C的体积分数为a。若在恒温恒容下,按0.6mol的A、0.3mol的B、1.4 mol的C为起始物质,达到化学平衡后,C的体积分数仍为a,则X的值可能为
XC(g)。达到化学平衡后,C的体积分数为a。若在恒温恒容下,按0.6mol的A、0.3mol的B、1.4 mol的C为起始物质,达到化学平衡后,C的体积分数仍为a,则X的值可能为
A.2 B.3 C.4 D.无法确定
12.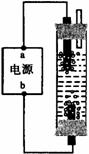 某学生想制作一种家用环保型消毒液发生器,用石墨作电极电解饱和氯化钠溶液,通电时,为使Cl2被完全吸收,制得有较强杀菌能力的消毒液,设计了如图的装置,则对电源电极名称和消毒液的主要成分判断正确的是
某学生想制作一种家用环保型消毒液发生器,用石墨作电极电解饱和氯化钠溶液,通电时,为使Cl2被完全吸收,制得有较强杀菌能力的消毒液,设计了如图的装置,则对电源电极名称和消毒液的主要成分判断正确的是
A a为正极,b为负极;NaClO和NaCl
B a为负极,b为正极;NaClO和NaCl
C a为阳极,b为阴极;HClO和NaCl
D a为阴极,b为阳极;HClO和NaCl
11.下列说法中错误的是
A.原子及其离子的核外电子层数等于该元素所在的周期数
B.元素周期表中从IIIB族到IIB族 10个纵行的元素都是金属元素
C.除氦外的稀有气体原子的最外层电子数都是8
D.同一元素的各种同位素的物理性质、化学性质均相同
10.在常温下10mL pH=10的KOH溶液中,加人pH=4的一元酸HA溶液至pH刚好等于7(假设反应前后溶液体积具有加和性),则对反应后溶液的叙述正确的是
A c(A-)=c(K+) B c(H+)=c(OH-)<c(K+)<c(A-)
C V总≥20mL D V总≤20mL
9.在 100mL 0.10 mol·L-1的 AgNO3溶液中加入100mL溶有2.08g BaCl2的溶液,再加入100 mL溶有0.010 mol CuSO4·5H2O的溶液,充分反应。下列说法中正确的是
A.最终得到白色沉淀和无色溶液
B.最终得到的白色沉淀是等物质的量的两种化合物的混合物
C.在最终得到的溶液中,Cl- 的物质的最为0.02 mol
D.在最终得到的溶液中,Cu2+的物质的量浓度为0.01 mol·L-1
8.一定温度下,向质量分数为a的乙腈(CH3CN)溶液中加入等体积的水,所得溶液中乙腈的质量分数为0.4a,若乙腈的密度为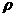 1,水的密度为
1,水的密度为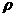 2,则下列说法正确的是
2,则下列说法正确的是
A.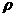 1<
1<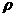 2
B.
2
B.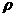 1>
1>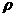 2 C.
2 C.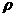 1=
1=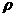 2
D.无法确定
2
D.无法确定
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com