
题目列表(包括答案和解析)
5.下列所述情况可能引起水污染的是:①城市生活污水的任意排放;②农业生产中农药、化肥使用不当;③海上油轮石油泄漏;④工业生活中废液、废渣、废气的排放
(A)只有①③ (B)只有①④ (C)只有②④ (D)①②③④
选项符合题意.若正确答案只包括一个选项,多选时,该小题0分;若正确答案包括两个选项,只选一个且正确的给1分,选两个且都正确的给3分.但只要选错一个,该小题就为0分.)
4.在炼铁、制玻璃和制水泥三种工业生产中,都需要的原料是
(A)生石灰 (B)石灰石 (C)石英 (D)纯碱
3.既有离子键又有共价键和配位键的化合物是
(A)NH4NO3 (B)NaOH (C)H2SO4 (D)H2O
1.下列物质中属于纯净化合物的是
(A)福尔马林 (B)干冰 (C)凡士林 (D)石墨
(A)Fe(OH)3溶液与硅酸胶混和将产生凝聚现象
(B)Fe(OH)3胶体粒子在电场影响下将向阳极运动
(C)Fe(OH)3胶体微粒不停地作布朗运动
(D)光线通过Fe(OH)3溶胶时会发生丁达尔现象
26.将等物质的量的两种氧化物溶于100 mL硫酸,而后逐滴加入l.00 mol/L的 NaOH溶液。当加入的NaOH的体积V1=50 mL时,开始有沉淀析出,且沉淀量随NaOH 加入量逐渐增加。当NaOH的体积V2=650 mL时,沉淀量达最大值,继续滴加NaOH时,沉淀量逐渐减小。当V3=750 mL时,沉淀量不再改变。
(1)最初加入的50 mL NaOH溶液的作用是
(2)硫酸的浓度是 mol/L
(3)两种氧化物分别是 ,其物质的量分别是 。
高三第一学期期末考试
25.0.1mol某种烯烃或两种烯烃的混合物(碳原子数均不超过5)充分燃烧后,生成的二氧化碳完全被300mL2mol/L的NaOH溶液吸收,所得溶液中含有两种物质的量相等的溶质。
(1) 若为纯净物,试推断可能的烯烃分子式:
① ;② ;③ (可以不填满,也可以补充)
(2)若为两种烯烃的混合物,试推断可能的组成及体积比(可以不填满,也可以补充)
|
序号 |
组成 |
体积比 |
|
1 |
|
|
|
2 |
|
|
|
3 |
|
|
24. 2002年度国家科学技术奖的颁奖大会,于2003年2月28日在人民大会堂隆重举行,连续四年空缺的国家自然科学一等奖由中科院上海有机化学研究所获得。他们完成的有机分子簇集和自由基化学研究项目,荣获2002年度国家自然科学唯一个一等奖。
(1)上海有机化学研究所在我国氟化学理论研究和氟产品以及核化学工业方面等作出过重大贡献,如F46,就是用四氟乙烯与全氟丙烯(分子式C3F6)共聚得到的。写出这两种单体按物质的量之比为1:1聚合所得高分子化合物的结构简式 。
(2)已知三氟苯乙烯(三个氟均连在苯环上)的分子式为C8H5F3,则它的异构体除
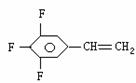
外,还有 种,试写出其中任意两种的结构简式
。
(3)有机反应中很多是自由基反应,最简单的自由基是碳烯(:CH2),它可以由重氮甲烷(CH2N2)受热或光照时分解得到,同时有氮气生成
①碳烯的电子式为 。
②碳烯很容易以它的一对未成对电子与不饱和烯、炔发生加成,生成三元环状化合物,它与丙烯反应后所得产物的结构简式为 。
③碳烯还可以插入C-H之间,使碳链加长。它插入丙烷分子C-H之间,碳链增长形成C4H10,该化合物结构简式可能为 。
④重氮甲烷和CCl4混合后用紫外光照射时发生反应,生成一种相对分子质量为210的有机物和N2,写出该反应的化学方程式(有机物用结构简式表示):
。
23.如图所示,甲、乙、丙是三种常见单质,X、Y、Z是常见化合物。它们之间有如下转化关系:
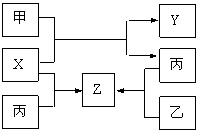 (1)若甲是短周期金属单质,乙、丙是短周期非金属单质。X、Y、Z中只有一种是离子晶体,试推断:
(1)若甲是短周期金属单质,乙、丙是短周期非金属单质。X、Y、Z中只有一种是离子晶体,试推断:
①含有丙元素的化合物是 (填X、Y、Z)
②工业上有些气体中也含有一定量的Z成分,试 列举 工业上含Z成分的气体 。
③X与甲反应的化学方程式 。
(2)若甲是具有氧化性的黄绿色气体单质,丙通常是深红棕色液体,Y和Z具有相同的阳离子,X与Z含有相同的阴离子,试推断:
①写出甲、乙、丙三种物质的化学式 、 、 。
②写出X与足量的甲在溶液中完全反应的离子方程式 。
22. 设计出燃料电池使汽油氧化直接产生电流是对世纪最富有挑战性的课题之一。最近有人制造了一种燃料电池,一个电极通入空气,另一电极通入汽油蒸气,电池的电解质是掺杂了Y2O3的ZrO2晶体,它在高温下能传导O2-离子。回答如下问题:
(1) 以丁烷代表汽油,这个电池放电时发生的化学反应的化学方程式是:
(2) 这个电池的正极发生的反应是:
固体电解质里的O2-的移动方向是:
向外电路释放电子的电极是:
(3)汽油燃料电池最大的障碍是氧化反应不完全产生 堵塞电极的气体通道,有人估计,完全避免这种副反应至少还需10年时间,正是新一代化学家的历史使命。
21.在100℃时,将0.100mol的四氧化二氮气体充入1 L抽空的密闭容器中,隔一定的时间对该容器内的物质进行分析,得到如下表格:
|
浓度 |
时间 |
0 |
20 |
40 |
60 |
80 |
100 |
|
C(N2O4)moL·L-1 |
0.100 |
C1 |
0.050 |
C3 |
a |
b |
|
|
C(NO2)moL·L-1 |
0.000 |
0.060 |
C2 |
0.120 |
0.120 |
0.120 |
试填空:
(1)该反应的化学方程式为 。达到平衡时四氧化二氮的转化率为 %。表中C2 C3、a b(填 > < =)。
(2)20s时四氧化二氮浓度C1= moL·L-1。
0s~20s四氧化二氮的平均反应速率为 moL·L-1·s-1。
(3)若在相同情况下最初向该容器充入的是二氧化氮气体,要达到上述同样的平衡状态,二氧化氮的起始浓度是 moL·L-1。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com