
题目列表(包括答案和解析)
4、已知氢化锂(LiH)属于离子晶体,LiH跟水反应可以放出氢气,下列叙述中正确的是
A LiH的水溶液呈中性 B LiH是一种强氧化剂
C LiH中的氢离子可以被还原成氢气 D LiH中氢离子与锂离子的核外电子排布相同
3、CH3COOH分别跟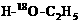 和
和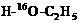 起酯化反应后,两者生成的水中所含
起酯化反应后,两者生成的水中所含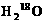 的质量分数
的质量分数
2、某强酸和某强碱溶液等体积混合后,所得溶液的pH值为7。原酸溶液和原碱溶液的物质的量浓度
下列1~3小题中都隐含着2个数字,请比较前后这两个数字的大小,A用表示“大于”,B表示“小于”,C表示“等于”,D表示“不能确定”。把答案的序号填写在“答题卷”上。
1、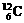 和
和 原子的中了数
原子的中了数
2.本题第4个采分点共4分,可分段给分如下:计算盐酸的总物质的量,应扣除的NaOH的物质的量、CaCO3消耗的盐酸物质的量各给1分,答案[0.0268(摩)]给1分.
1.第1个采分点共2分,若开始时没有作出判定,但在解题过程中表明样品中含有CaCO3和Ca(OH)2,该采分点同样给分.
x=4.27(摩) (2分)
37.(12分)判定CaO样品中可能含有Ca(OH)2和CaCO3(各1分,共2分)
设0.80克中含x克CaO,含(0.80-x)克Ca(OH)2,
[说明]
35.(8分)CH3CH2CH2CH2COOCH2CH2CH2CH2CH3、
(CH3)2CHCH2COOCH2CH2CH(CH3)2、
(每空2分,共8分)
33.(4分)
(每空2分,共4分)
注:不写HBr,而是写HCl,HX,1,4-二溴丁烷写成二氯,二X丁烷都是对的.但是从第1个错误答案起,后面均不给分.
31.(4分)
A4 4AH3=A4+6H2 (每空2分,共4分)
(若答案中将A写成P或As,都可当作A,同样给分)
透明溶液,也会出现此方案的现象 (2分)
(2分)
此方案的现象 (2分)
(每个方案分析2分,其中判断1分,理由1分.其它合理的分析也给分).
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com