
题目列表(包括答案和解析)
4.下列实验中,能验证乙二酸比乙酸酸性强的是 ( )
A、分别将未知浓度的两种酸滴在Na2CO3粉末上
B、同温时取等物质的量的浓度的两种酸分别滴定0.1mol·L-1的NaOH溶液
C、相同温度时取等物质的量的浓度的两种酸分别滴在pH试纸上
D、分别将乙二酸晶体和冰醋酸置于pH试纸上
3.在实验中手不慎被玻璃划破,可用FeCl3溶液紧急止血,其主要原因是 ( )
A、FeCl3溶液能使血凝聚 B、FeCl3溶液具有杀菌消毒作用
C、FeCl3溶液能产生Fe(OH)3沉淀堵住伤口 D、FeCl3溶液能使血液发生化学变化
2.下列事实中,能证明氯化氢是共价化合物的是 ( )
A、氯化氢易溶于水 B、氯化氢的水溶液能导电
C、液态氯化氢不导电 D、氯化氢不易分解
1.制备1,2-二溴乙烷的合理反应是 ( )
A、乙烷光照下与Br2反应 B、乙烯加成HBr
C、乙炔与过量Br2反应 D、乙烯加成Br2
4、实验室用Zn粒和盐酸反应制H2,其中含酸雾、水气、硫化氢及少量氧气等杂质气体,某同学设计了以下几种装置,按一定顺序连接,气体通过时,达到每一装置除去一种气体的目的。
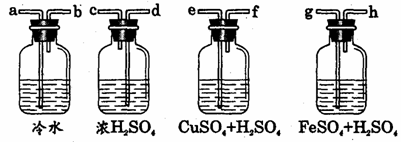 (1)它们连接的顺序为
;
(1)它们连接的顺序为
;
(2)除去H2S的离子方程式为 ;
(3)除去O2观察到的现象为 。
3、欲制无水氯化铝并保存备用。现有仪器如下图所示,并有食盐晶体、水、固体烧碱、铝粉、二氧化锰、浓硫酸等六种试剂。
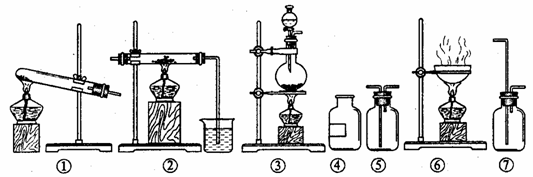 设计的制取过程是:制氯气 → 加净化和干燥氯气 → 制氯化铝
设计的制取过程是:制氯气 → 加净化和干燥氯气 → 制氯化铝
请回答下列问题:
(1)从上列仪器中选取必须的几种,连接成一个制无水氯化铝的连续装置,按前后顺序填写图的编号(不一定填满),并写出各仪器里放入的试剂的化学式。
仪器编号 、 、 、 、 ;
放入试剂 、 、 、 、 。
(2)写出实验过程中有关反应的化学方程式。
2、实验室利用乙醇脱水制备乙烯的步骤如下;
①在一蒸馏烧瓶中加人95%的乙醇和浓硫酸(体积比为l:3),再加入少量干净的河沙;
②瓶口插上带塞的温度计;
③加热并迅速使反应温度上升到170℃;
④气体通过稀NaOH溶液进行洗气后,用酸性KMnO4溶液检验乙烯的还原性。
据此回答下列问题:
(1)步骤①中混合乙醇和浓硫酸时应注意的问题是 。
(2)在反应液中加入河沙的原因是 。
(3)步骤②中温度计水银球的正确位置是 。
(4)加热时,使反应液温度迅速升高到I7O℃的原因是 。
(5)步骤④中.用稀NaOH溶液洗涤气体,能除去可能伴随乙烯生成的气体是 。
1、实验室有一包 KCl和 AlCl3的固体混合物,通过以下实验可确定 KCl和 AlCl3的质量之比,试根据实验方法和主要步骤,回答有关问题:
(1)调整托盘天平的零点时,若指针偏向右边,应将右边的螺丝向旋动。
(2)某学生用已知质量为 y g的表面皿准确称取 W g样品,他在托盘天平的右盘上放上(W+y)g的砝码,在左盘的表面皿中放入样品,此时指针稍偏右边,该学生应怎样操作 ;
 (3)将样品置于烧杯中加适量水溶解,滴入过量的A溶液,烧坏中有沉淀物,则A溶液的名称是
;
(3)将样品置于烧杯中加适量水溶解,滴入过量的A溶液,烧坏中有沉淀物,则A溶液的名称是
;
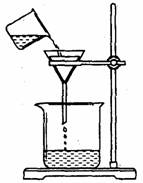
(4)过滤,某学生欲用右图装置操作,错误之处应怎样纠正?
答: ;
(5)甲学生用水多次洗涤过滤所得沉淀物,然后使其干燥,得到固体纯净物C,质量为W2g,C的名称是 ;
(6)乙学生将过滤所得滤液跟甲学生洗涤沉淀所得液体混合,然后蒸干溶剂,再充分加热,最后得到纯净KCl固体W1g,则原混合物中KCl与AlCl3的质量之比的计算式为 。
2、写出有关的化学方程式:
A与B ;C与D ;
E与无水硫酸铜 ;F与Mg ;
F与Mg的反应产物与水 。
知识过关
2、训练发散思维以增强实验设计能力,提高信息迁移水平
实验方案的设计往往有许多途径。为了适应中学生的知识能力水平,中学课本中的某些实验可能不是最优的方案。所以在实验复习中要根据实验原理来设计实验步骤和装置,掌握一些装置和仪器药品的替代方法,力求使设计的实验仪器简单、操作便捷、节省试剂、现象明显、安全防污等,培养和增强实验设计能力和创造性思维能力。近年来,实验题中新情境试题不断增多,这类试题的特点是将基本的实验操作设计置于新的情境中(主要是中学课本没有的新反应或新装置或是能使中学生理解的最新科技知识、简化的改进的装置等),结合学生原有的知识和能力,来进行仪器组装、现象描述、数据分析、考虑安全和防污等,用来考查考生自学能力、思维能力、分析综合及评价的能力。由于这类实验试题情境新颖、设问巧妙、铺垫得当、知识新、思维量大、所以区分度很好,能确实将一些基础扎实、自学能力强、思维敏捷、心理素质好的考生选拨出来。所以,新情境实验试题将是今后实验试题的命题方向。
典型例题
例1、某学生根据高中课本中硝酸钾受热分解的实验操作来判断硝酸铅的分解产物之一是氧气;将试管中的硝酸铅加热到熔融,把带有火星的细木条伸进试管口,检验放出的气体,当发现木条复燃时该学生即断言,硝酸铅受热分解有氧气放出。请你对上述实验及结论的合理性作出评价。如有必要,可提出改进的实验方案。
例2、研究某一化学反应的实验装置如下图所示:
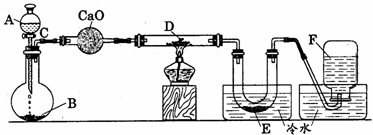 A-F属于下列物质中的六种物质:浓硫酸、浓盐酸、浓氨水、稀硫酸、稀盐酸、稀氟水、水、锌粒、铜片、食盐、高锰酸钾、氯化钙、氧化钙、四氧化三铁、氧化铁、氧化铜、氢气、二氧化碳、二氧化氮、一氧化碳、氯气、氯化氢、氨气、氮气、氧气。
A-F属于下列物质中的六种物质:浓硫酸、浓盐酸、浓氨水、稀硫酸、稀盐酸、稀氟水、水、锌粒、铜片、食盐、高锰酸钾、氯化钙、氧化钙、四氧化三铁、氧化铁、氧化铜、氢气、二氧化碳、二氧化氮、一氧化碳、氯气、氯化氢、氨气、氮气、氧气。
实验现象;
(1)D物质由黑色变为红色
(2)无水硫酸铜粉末放入无色透明的E中得到蓝色溶液
(3)点燃的镁条伸入无色无味的F中.镁条表面生成一种灰黄色固体物质。将该发黄色物质放入水中,有气体放出,该气体具有刺激性气味。并能使润湿的红色石蕊试纸变蓝。通过分析回答:
l、写出A-F的物质名称:
A ,B ,C ,D ,E ,F 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com