
题目列表(包括答案和解析)
14.已知化合物甲和乙都不溶于水,甲可溶于质量分数大于或等于98%的硫酸,而乙不溶。现有一份甲和乙的混合物样品,通过实验进行分离,可得到固体甲。(实验中使用的过滤器是用于过滤强酸性液体的耐酸过滤器。)
请填写表中空格,完成由上述混合物得到固体甲的实验设计。
|
序号 |
实验步骤 |
简述实验操作(不必叙述如何组装实验装置) |
|
① |
溶解 |
将混合物放入烧杯中,加入98% H2SO4,充分搅拌直到固体不再溶解。 |
|
② |
|
|
|
③ |
|
|
|
④ |
|
|
|
⑤ |
洗涤沉淀 |
|
|
⑥ |
检验沉淀
是否洗净 |
|
13.现有右图所示装置,为实现下列实验目的,其中y端适合于作入口的是
(A)瓶内盛液体干燥剂,用以干燥气体
 (B)瓶内盛液体洗涤剂,用以除去某气体中的杂质
(B)瓶内盛液体洗涤剂,用以除去某气体中的杂质
(C)瓶内盛水,用以测量某难溶于水的气体的体积
(D)瓶内贮存气体,加水时气体可被排出
(E)收集密度比空气大的气体
(F)收集密度比空气小的气体
12.下列事故中,处理不当的是 ( )
A、皮肤上沾有苯酚时,立即用酒精洗涤
B、误食重金属盐,立即喝生牛奶或蛋清
C、不慎将水银温度计打碎,立即用硫磺覆盖水银
D、不小心将装浓硫酸的试剂瓶撞翻,立即用自来水冲洗
11.Cu+在酸性溶液中可发生自身氧化还原反应,生成Cu2+和单质。若要检验用氢气还原CuO后所得的红色固体产物中是否含有Cu2O,应选用的试剂和相应的实验现象正确的是 ( )
A、浓H2SO4;是否有无色气体生成 B、稀HNO3;是否生成蓝色溶液
C、稀H2SO4;固体物质是否溶解 D、稀HCl;是否生成蓝色溶液
10. 某学生想制作一种家用环保型消毒液发生器,用石墨作电极电解饱和氯化钠溶液,通电时,为使Cl2被完全吸收,制得有较强杀菌能力的消毒液,设计了如图的装置,则对电源电极名称和消毒液的主要成分判断正确的是
( )
某学生想制作一种家用环保型消毒液发生器,用石墨作电极电解饱和氯化钠溶液,通电时,为使Cl2被完全吸收,制得有较强杀菌能力的消毒液,设计了如图的装置,则对电源电极名称和消毒液的主要成分判断正确的是
( )
A、 a为正极,b为负极;NaClO和NaCl
B、 a为负极,b为正极;NaClO和NaCl
C、 a为阳极,b为阴极;HClO和NaCl
D、 a为阴极,b为阳极;HClO和NaCl
9.下列各组物质,只用一种试剂就能鉴别的是(允许加热) ( )
 ①Al2(SO4)3、FeCl2、Mg(NO3)2、NH4NO3四种溶液
①Al2(SO4)3、FeCl2、Mg(NO3)2、NH4NO3四种溶液
② 、 、 、 四种液体
③CuO、FeS、FeO、C四种黑色粉末
④KNO3、Al2(SO4)3、Ba(OH)2、HCl四种溶液
A、只有①③ B、只有①③④ C、只有②③④ D、全部
8.某有机物x溶解于烧碱液(滴有酚酞)中,开始溶液呈红色,煮沸5分钟后,溶液褪色;加入盐酸至酸性时,沉淀出白色的晶体,该晶体溶于水,加入FeCl3溶液呈现紫色。该有机物x是 ( )
 O
O
A、 HO- -NH2 B、HO- -C-O-CH3
O
C、 HO-CH2- -C-OCH3 D、HO- -COOH
7.向某一溶液里加入过量氨水,得到白色沉淀和无色溶液,将沉淀过滤并使其与过量烧碱作用,沉淀全部溶解,则原液里可能含有的离子是 ( )
A、Fe3+ B、Mg2+ C、Al3+ D、Ag+
6.现有一种未知液,若加入过量盐酸,生成白色沉淀。过滤后向滤液加入过量的氨水使溶液呈碱性,又产生白色沉淀。再向滤液中加入小苏打液,还产生白色沉淀。根据以上事实,原溶液中可能存在的离子是 ( )
A、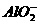 、Ba2+、Mg2+
B、Ag+、Ca2+、Mg2+
、Ba2+、Mg2+
B、Ag+、Ca2+、Mg2+
C、Ag+、Mg2+、Na+ D、Ag+、Al3+、Ba2+
5. 验证乙酸乙酯密度,溶解性和水解三项性质的合理实验是 ( )
A、将其滴入水中,随即滴加碱液并迅速加热至沸腾
B、将其滴入沸腾的碱液中观察
C、将其滴入水中观察片刻,再滴加含有酚酞的碱液并缓缓加热
D、将其滴入沸腾的水中观察
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com