
题目列表(包括答案和解析)
7.( )由CO2、H2和CO组成的混合气体在同温同压下与氮气的密度相同。则该混合气体中CO2、H2和CO的体积比为
A.29:8:13 B.22:1:14 C.13:8:29 D.26:16:57
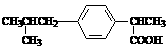
6.( )具有解热镇痛及抗生素作用的药物“芬必得”,其主要成分的结构式如图,它属于
 A.芳香族化合物
A.芳香族化合物
B.苯甲酸的同系物
C.易溶于水的有机物
D.易升华的物质
5.( )已知2H2S+SO2=3S+2H2O,现将等物质的量的SO2和H2S常温下在定容的密闭容器中反应,待充分反应后恢复至常温。容器内的压强是原压强的
A.1/2 B.1/4 C.<1/4 D.>1/4
4.( )向100mL的FeBr2溶液中通入标准状况下的Cl23.36L时,Cl2全部被还原,测得此时溶液中c(Br-)=c(Cl-),则原FeBr2溶液的物质的量浓度是
A.0.75mol• L-1 B.1.5mol• L-1 C.2mol• L-1 D.3mol• L-1
3.( )室温下,在pH=12的某溶液中,由水电离的c(OH-)为
①1.0×10-7mol• L-1 ②1.0×10-6mol• L-1
③1.0×10-2mol• L-1 ④1.0×10-12mol• L-1
A.① B.①③ C.④ D.③④
2.( )生物体中细胞膜内的葡萄糖.细胞膜外的富氧液体及细胞膜之间可构成微型的生物原电池,下列有关判断正确的是
①正极的电极反应可能是:O2+4e-+2H2O=4OH-
②负极的电极反应可能是:O2+4e-+2H2O=4OH-
③负极的反应主要是C6H12O6(葡萄糖)生成CO2或HCO3-
④正极的反应主要是C6H12O6(葡萄糖)生成CO2或HCO3-
A.①② B.①③ C.②③ D.②④
1.( )近年来,我国许多城市禁止汽车使用含铅汽油,其主要原因是
A、提高汽油燃烧效率 B、降低汽油成本
C、避免铅污染大气 D、铅资源短缺
25.某CuO粉末与适量的硫酸(d=1.7g·cm-3)在微热下充分反应,冷却后恰好全部形成CuSO4·5H2O(设反应过程中无水分损失)。求此硫酸溶液的物质的量浓度。
26在密闭容器中,加入一定量的N2O4,在一定温度下反应达到平衡:N2O4(气)=2NO2(气)(正反应为吸热)试求:
⑴该温度下该反应的化学平衡常数的表达式K= ,若使该反应的温度降低,则达新平衡时K值 (用“增大”“减小”“不变”填空)。⑵若有3 4 的N2O4未发生分解,则平衡时混合气体的平均相对分子质量为 .
⑶若平衡混合气体的平均相对分子质量为69则N2O4的分解率为 .⑷保持容器容积不变,N2O4未分解时容器内压强为1×105Pa,则当压强增至1.35×105Pa时,N2O4的分解率为
24.利用下图装置,选用适当试剂,可完成实验A、B,并得出相应的实验结论。实验所用试剂和所得结论列于下表中。⑴请将表中①、②应填写的内容填在下面空格内
|
实验 |
所用试剂 |
实验结论 |
||
|
甲 |
乙 |
丙 |
||
|
A |
浓盐酸 |
高锰酸钾 |
① |
氧化性 KMnO4>Cl2>Br2 |
|
B |
盐酸 |
石灰石 |
苯酚钠 |
② |
① 。 甲


 ②
。
②
。
 丙
丙
乙
⑵请利用上面的装置另设计一个有机化学实验,制备某熟悉有机物并检验其化学性质。
①写出制备该有机物的化学方程式 。
②丙中试剂是 观察到的现象是 ,由此现象得出的结论是 。
23. 现有四种无色溶液a、b、c、d,分别是Na2CO3、Na2SO4、H2SO4、Ba(NO3)2中的一种,为确定每种溶液,做如下实验
①a + b→沉淀+溶液e ②b +d→沉淀f+ 溶液 ③e +f→溶液+气体
请根据上述实验推断
a是 b是 c是 d是 .
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com