
题目列表(包括答案和解析)
13.电子工业中常用FeCl3溶液腐蚀印刷电路板上的部分铜皮。要从腐蚀后的废液中回收铜
和制得纯净的FeCl3溶液,需要用到下列试剂中的( )
①蒸馏水; ②铁粉; ③浓硫酸; ④浓盐酸; ⑤烧碱; ⑥浓氨水 ⑦氯气。
A、①②④⑦ B、①③④⑥ C、②④⑥⑦ D、①④⑥⑦
12.下列离子方程式正确的是 ( )
A、将少量SO2气体通入NaClO溶液中
SO2 +2ClO-+H2O==SO32-+2HClO
B、在硫酸氢钾溶液中加入Ba(OH)2溶液至pH=7
2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O
C、碳酸氢钙溶液中加入少量氢氧化钠溶液
OH―+ Ca2++ HCO3-==CaCO3↓+H2O
D、用铂电极电解硫酸铜饱和溶液
Cu2+ +2H2O Cu +O2↑+4H+
Cu +O2↑+4H+
11.在容积相同的两密闭容器A和B中,保持温度为423K,同时向A、B中分别加入amol
及bmol碘化氢(a>b),待反应 2HI(g)  I2(g)+H2(g) 达到平衡后,下列说法肯定正确的是( )
I2(g)+H2(g) 达到平衡后,下列说法肯定正确的是( )
A、从反应开始到建立平衡A容器中所需的时间短
B、平衡时A、B两容器中I2蒸气的浓度相同
C、平衡时I2蒸气在混合气体中的百分含量,A容器大于B容器
D、平衡时HI的分解率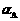 等于
等于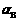
10.近年来用红外激光技术研究液氢时,发现分子间作用力也可引起粒子间的反应。在液氢中有氢分子和质子形成的H3+离子,其构型是等边三角形;H3+还可进一步形成Hn+。下列判断正确的是( )
A、H3+可在液氢中开成H5+、H7+、H9+
B、每个H3+粒子中含有2个质子
C、H3+可在液氢中形成H4+、H5+、H6+
D、H3+可广泛存在于固态、液态和气态氢中
9.以NA表示阿伏加德罗常数,下列说法正确的是( )
A、1L0.1mol·L-1的醋酸溶液中含离子和分子总数是0.1NA
B、22.4L氖气中所含原子数为NA
C、1.6gNH2-离子中所含电子数为NA
D、2gD2O所含中子数为NA
8.通常状况下,下列各选项中的两个量,前者一定大于后者的是( )
A、物质的量浓度相等的次氯酸钠溶液和醋酸钠溶液的pH
B、25℃的纯水和100℃的纯水中的c(H+)
C、硫酸铵溶液和氯化铵溶液中c(NH4+)
D、读取量筒中一定体积的液体时,仰视的读数和俯视的读数
7.2002年12月31日,世界上第一条商业磁悬浮铁路在上海投入运营,磁悬浮的核心技术是利用超导体的反磁性。以Y2O3、BaCO3和CuO为原料,经研磨烧结可合成一种高温超导物质YBa2Cu3Oⅹ。现欲合成0.5mol此高温超导物质理论上需要Y2O3、BaCO3和CuO的物质的量(mol)分别是( )
A、0.50、 0.50、 0.50 B、0.50、 1.0、 1.5
C、0.25、 1.0、 1.5 D、1.0、 0.25、 0.17
6.根据所学知识,下列说法正确的是( )
①把1mL饱和的FeCl3溶液逐滴加入20mL沸水中,边加边振荡,即可制得Fe(OH)3胶体;②医学上利用胶态磁流体(将磁性物质制成胶体离子作为药物的载体,在磁场作用下送到病灶,达到治疗目的)可以治癌病; ③化工生产上可以利用电泳将油漆、乳胶、橡胶等粒子均匀地沉积在镀件上,这样的操作叫电泳电镀;④KNO3溶于水则形成溶液,如果溶解在酒精中则可形成胶体。
A、只有①正确 B、只有①②③正确
C、只有①③④正确 D、全部正确
5.2003年由于“非碘”的影响,市场上的消毒液被抢售一空,因而“家用消毒液发生器”
也进入了百姓家庭。该“家用消毒液发生器”是以食盐和自来水为原料,通电时发生器内的
电极板上产生大量气泡(同时使产生的气体充分与电解液接触),所制得的混合液具有强烈
的杀菌能力,且不致对人体造成伤害。该发生器配制消毒液所涉及到的化学反应(反应条件
均略去)有( )
①2NaCl +2H2O = 2NaOH +H2↑+Cl2↑
②Cl2 + 2NaOH = NaCl +NaClO +H2O
③H2 +Cl2 = 2HCl
④Cl2 +H2O =HCl+HClO
⑤2HClO =2HCl + O2↑
A、①④⑤ B、①② C、③④⑤ D、②③④
4.蓄电池在放电时起原电池作用,在充电时起电解池作用,下列是爱迪生蓄电池分别在充电和放电时的反应:Fe +NiO2+2H2O放电充电Fe(OH)2+ Ni(OH)2,下列有关爱迪生蓄电池的推断中不正确的是 ( )
A、放电时Fe作负极,NiO2作正极
B、放电时溶液中的阳离子向正极移动
C、充电时的阳极反应是Fe(OH)2 +2e- == Fe + 2OH-
D、该蓄电池既可用KOH溶液又可用稀H2SO4作电解质溶液
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com