
题目列表(包括答案和解析)
23.(8分)荣获2001年诺贝尔化学奖的科学家科研的成果,不仅具有巨大的理论意义,并且已经成功地运用于生产实际,取得了良好的经济效益。例如,美国科学家的成果被应用于工业合成重要的治疗帕金森症(震颤麻痹症)的药物左旋多巴(C)。下面是它们的结构式以及美国科学家发明的合成路线。

(1)在上述反应中,关于(I)、(II)两步的反应类型,全部正确的是( )
A、化合反应,分解反应 B、加成反应,水解反应
C、还原反应,分解反应 D、氧化反应,水解反应
(2)在上述化合物中,多巴、甘氨酸都是氨基酸,它们的共同点是具有两性,即:既有酸性,也有碱性。因此,它们只是与下列物质中的( )不进行反应。
A、金属钠 B、氢氧化钠 C、氯化钠 D、盐酸
22.(10分)
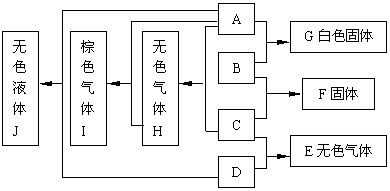
上图中每一个方框内的字母代表一种物质,常温常压下,A、B、C和D均为单质,且B为金属,其它三种为双原子分子的气体,它们在一定条件下,发生图中所示的化合反应,得到化合物E、F、G、H、I和J,这些化合物在常温常压下的状态及颜色已在图中注明,有关反应的化学计量关系为:
(1)A与B按物质的量之比n(A)︰n(B)=1︰2完全反应生成G
(2)B与C按物质的量之比n(B)︰n(C)=3︰1完全反应生成F
(3)C与D按物质的量之比n(C)︰n(D)=1︰3完全反应生成E
请填空:
(1)物质B是 ,物质C是 。
(2)B与C反应生成F的化学方程式为: 。
(3)A与H反应生成I的化学方程式为: 。
(4)E与A能反应吗? ,若能则化学方程式为: 。
21.(8分)有元素X、Y、Z,已知X元素的-2价离子、Y元素的+1价离子的核外电子排布均与氖原子相同;Z元素最高价氧化物分子组成为Z2O3,4.5gZ元素所形成的单质与盐酸反应,在标准状况下生成5.6L氢气,Z原子核中质子数比中子数少一个。(1)X原子的结构示意图_______;Y元素位于周期表中第_______周期、第------族。(2)用电子式表示X与Y在高温下形成稳定的化合物的过程__________________________________(3)X、Z两种元素所形成的化合物,是工业上____________的主要原料,该反应的化学方程式为_______________________________________。
20.(15分)实验室可以用下图所示仪器连接起来制备纯净的二氧化碳并测定其式量。

现用含有少量硫化亚铁的大理石和盐酸反应制备二氧化碳气体, 实验步骤如下:
(1)将橡皮塞B塞在A烧瓶口, 并用橡皮筋套在烧瓶的瓶颈处以标记橡皮塞所塞入瓶颈的深度, 准确称其质量为m1g。
(2)连接制备和净化气体的装置, 其接口连接顺序是: 接 , 接 , 接 , 接 。
(3)将导管G插入烧瓶A中用向 (填“上”或“下”)排空气法收集二氧化碳气体; 检验二氧化碳气体已经充满烧瓶的方法是 。
若经检验, 二氧化碳气体已经充满烧瓶, 迅速用橡皮塞塞好烧瓶口, 并称其质量为m2g。
(4)将烧瓶口橡皮塞取下, 向烧瓶内注水至标记线, 再将水小心地倒入量筒, 测量出水的体积为V1mL; 将该体积换算成标准状况时的体积为V2mL。
请写出二氧化碳式量的计算式 。
若不将气体净化和干燥, 所测定的二氧化碳式量的数值将会 (填“偏高”或“偏低”), 其理由是 。
19. (7分)
(7分)
如图A、B、C均为制气装置,盛放药品前都需检验气密性。回答下列问题:
(1)三次检验气密性方法的共同之处是:
________________________________________________________
________________________________________________________;
(2)三次检验气密性方法中的不同之处是:
_______________________________________________________
_______________________________________________________。
18.将0.2mol KMnO4在一定温度下加热后生成a molO2;将剩余固体与过量浓盐酸混合加
热又生成b mol Cl2,此时锰元素全部以Mn2+形式存在。若a+b=m,则m的值可能为( )
A、0.35 B、0.45 C、0.55 D、0.60
第二卷(非选择题,共78分)
17.1L1.00mol·L-1的纯碱溶液逐滴加入到1L1.25mol·L-1的盐酸中;再做相反操作:将1L1.25mol·L-1的盐酸逐滴加入到1L1.00mol·L-1的纯碱溶液中,两次操作在同温同压下产生气体的体积比是( )
A、2:5 B、1:1 C、2:1 D、5:2
16.将下列各组括号内的少量杂质除去的操作正确的是( )
A、福尔马林(甲酸):加Na2CO3 蒸馏
B、乙醇(水):加浓H2SO4 蒸馏
C、O2(H2 、H2O):通过浓硫酸洗气,再通过灼热的CuO 粉末
D、FeCl2溶液(FeCl3):加足量的铁粉,振荡、过滤
15.在铁与铜的混合物中,加入不足量的稀硝酸,反应后剩余金属m1g;再向其中加入一定
量稀硫酸,充分振荡后,剩余金属m2g。则m1与m2之间的关系是( )
A、m1一定大于m2 B、m1可能等于m2
C、m1一定等于m2 D、m1可能大于m2
14.安息香酸(C6H5 -COOH)和山梨酸(CH3CH==CH-CH==CH-COOH)都是常用的
食品防腐剂。下列有关这两种酸的叙述正确的是( )
A、都能与溴水反应,使溴水褪色
B、1mol酸分别与足量氢气加成,消耗氢气的量相等
C、在一定条件下都能与乙醇发生酯化反应
D、都能与氢氧化钠发生中和反应
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com