
题目列表(包括答案和解析)
7.美国Lawtcce Lirermre国家实验室(LLNL)的V·Lota·C·S·Yoo和H·Cynn成功地在高压下将CO2转化为具有类似SiO2结构的原子晶体,下列关于CO2原子晶体的说法正确的是
A.CO2的原子晶体和分子晶体互为同素异形体
B.在一定条件下,CO2原子晶体转化为分子晶体是物理变化
C.CO2的原子晶体和CO2分子晶体具有相同的物理性质
D.在CO2的原子晶体中,每一个碳原子周围结合4个氧原子,每一个氧原子跟两个碳原子相结合
6.以 NA 表示阿佛加德罗常数,下列说法正确的是
A.10.6gNa2CO3 固体中,含 0.1NA个CO 32 -
B.1摩尔甲基中含有7 NA个电子
C.31g 白磷中含有 NA 个 P - P 键
D.2g 重氢中含有2 NA个质子
5.在常温下10mL pH=10的KOH溶液中,加人pH=4的一元酸HA溶液至pH刚好等于7(假设反应前后体积不变),则对反应后溶液的叙述
① c(A-)=c(K+) ② c(H+)=c(OH-)<c(K+)<c(A-)
③ V总≥20mL ④ V总≤20mL 其中正确的是
A.①③ B.②④ C.①④ D.②③
4.周期表中16号元素和4号元素的原子相比较,前者的下列数据是后者的4倍的是 ①电子数 ②最外层电子数 ③电子层数 ④次外层电子数 其中正确的是
A ①② B ②③ C ③④ D ①④
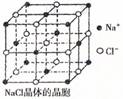
3.纳米材料的表面微粒占总微粒数的比例极大,这是纳米材料
具有许多特殊性质的原因,假设某氯化钠纳米颗粒的大小和
形状恰好与氯化钠晶胞的大小和形状(如图所示)相同,
则这种纳米颗粒的表面微粒数占总微粒数的百分数为
A.87.5% B.92.9%
C.96.3% D.100%
2.X和Y属短周期元素,X原子的最外层电子数是次外层电子数的一半,Y位于X的前一周期,且最外层只有一个电子,则X和Y形成的化合物的化学式可表示为
 A.XY B.XY2 C.XY3 D.X2Y3
A.XY B.XY2 C.XY3 D.X2Y3
1.有下列物质:①白磷 ②金刚石 ③石墨 ④二氧化硅 ⑤甲烷 ⑥四氯化碳 ⑦单晶硅 ⑧铵根离子,其分子结构或晶体结构单元中存在正四面体的是
A.除③外 B.只有①②⑤⑥ C.除③⑧外 D.除③④⑦⑧外
26.(8分)现有等物质的量的NaHCO3、KHCO3的混合物a g与100mL盐酸反应。题中涉及的气体体积均以标准状况计,填空时可以用带字母的公式表示。
(1)该混合物中NaHCO3与KHCO3的质量比为 。
(2)如碳酸氢盐与盐酸恰好完全反应,则盐酸的物质的量浓度为 mol·L-1。
(3)如果盐酸过量,生成CO2的体积为 L。
(4)如果反应后碳酸氢盐有剩余,盐酸不足量,要计算生成CO2的体积,还需要知道
。
25. (12分)在一定温度下,把2体积
(12分)在一定温度下,把2体积
N2和6体积H2通入一个带有活塞的容积
可变的容器中,活塞的一端与大气相通,
发生反应N2(g)+3H2(g)
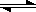 2NH3 (g) ;
2NH3 (g) ;
ΔH<0达到平衡,测得混合气体为7体积。
(1)保持上述反应温度不变,设a、b、c分别代表初始加入的N2、H2、NH3体积,若反应达到平衡后,混合气体中各物质的百分含量仍与上述平衡完全相同,那么:
①若a=1, c=2则b=_____,在此情况下,反应起始时将向_____方向进行。
②若规定起始时反应向逆方向进行,则C的取值范围是______________
(2)在上述装置中,若起始时的a、b、c值均与(1)相同,但需控制平衡后混合气体为6.5体积,则可采取措施是______,其原因是__ ____。
24.(10分)药用有机化合物A为一种无色液体。从A出发可发生如下图所示的一系列反。
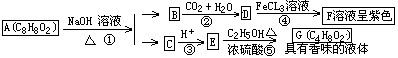
试回答:
(1) 写出化合物A、B、C的结构简式: A _________________;B__________________;
C_______________。
(2)化学方程式表示如下反应:
①___________________________;⑤_______________________________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com