
题目列表(包括答案和解析)
13.表示0.1mol·L-1NaHCO3溶液有关微粒浓度的关系正确的是
A.c(Na+)+c(H+)=c(HCO3-)+c(CO32-)+c(OH-)
B.c(Na+)=c(HCO3-)+c(CO32-)+c(H2CO3)
C.c(Na+)>c(HCO3-)>c(CO32-)>c(H+)>c(OH-)
D.c(OH-)=c(H+)+c(H2CO3)+c(HCO3-)
12.在恒温恒压下,向容积可变的密闭容器中充入3LA和2LB发生如下反应:3A(g)+2B(g)
 xC(g)+yD(g)达到平衡时,混合气体中D的体积分数为W%,若维持温度、压强不变,将1.2LA, 0.8LB,3LC, 0.6LD作为起始物质充入密闭容器中,达到平衡时混合气体中D的体积分数仍为W%,则x, y的值分别为
xC(g)+yD(g)达到平衡时,混合气体中D的体积分数为W%,若维持温度、压强不变,将1.2LA, 0.8LB,3LC, 0.6LD作为起始物质充入密闭容器中,达到平衡时混合气体中D的体积分数仍为W%,则x, y的值分别为
A.x=3, y=1 B.x=2, y=3 C.x=4, y=1 D.x=5, y=1
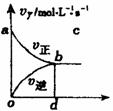
11.在容积固定的2L密闭容器中,充入X、Y气体各2mol发生反应X(g)+2Y(g)=2Z(g),并达平衡,以Y的浓度改变表示的反应速率v(正)、v(逆)与时间的关系如图所示,则Y平衡浓度表达式正确的是(式中S指对应区域的面积)
A.2-Saob B.1-Saob
C.2-Sabdo D.1-Sbod
10.在反应X+2Y
R+2M中,已知R和M的摩尔质量之比为22:9,1.6gX与Y恰好反应后,生成4.4gR,则此反应中Y和M的质量之比为
 A.16:9 B.23:9 C.32:9 D.46:9
A.16:9 B.23:9 C.32:9 D.46:9
9.热化学方程式:S(g)+O2(g)=SO2(g);△H=-297.3kJ/mol,分析下列说法中正确的是
A.反应S(g)+O2(g)=SO2(l)为吸热反应
B.S(g)+O2(g)=SO2(l); |△H|<297. 3kJ/mol
C.1mol SO2的键能总和大于1mol S和1mol O2键能之和
D.1mol SO2的键能总和小于1mol S和1mol O2键能之和
8.有主族元素形成的三种离子:Xn+、Ym-、Zm+,已知m>n,Xn+ 与Zm+多1个电子层,Z与Y同周期,三种原子的M层电子数均为偶数,则Y元素为
A.硅 B.氧 C.硫 D.碳
7.电解KOH溶液时,若阴、阳两极分别为碳和铁,当生成0.1mol Fe(OH)3沉淀时,共消耗amol H2O,产生bLH2(标准状况).则a和b分别为
A.a=0.25,b=2.24; B.a=0.05,b=2.24;
C.a=0.25,b=4.48; D.a=0.3,b=3.36.
6.已知钍原子(23290Th)可发生放射性变化:23290Th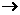 22888X+42He,其中X是生成的一种新元素,对X的判断正确的是
22888X+42He,其中X是生成的一种新元素,对X的判断正确的是
A.X位于第六周期;
B.X的单质能与冷水剧烈反应;
C.X的最高正价为+3价;
D.X的氢氧化物具有两性.
5.最近有人用一种称为“超酸”的化合物H(CB11H6Cl6)和C60反应,使C60获得一个质子,得到一种新型离子化合物[HC60]+[CB11H6Cl6]-。该反应看起来很陌生,但反应类型上可以跟中学化学里某个熟悉的化学反应相比拟。该化学反应是
A.Zn+2HCl=ZnCl2+H2↑ B.NH3+HCl
|
C.NaOH+ HCl=NaCl+H2O D.H2O+CH3COOH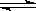 H3O++CH3COO-
H3O++CH3COO-
4.由短周期元素形成化合物A2B3,A3+比B2-少一个电子层,且A3+具有与Ne相同的核外电子层结构,B2-具有与Ar相同的核外电子层结构,则下列说法正确的是
A.A2B3是三氧化二铝 B.A3+和B2-最外层上的电子数不相等
C.A是第2周期第Ⅲ族的元素 D.B是第3周期ⅥA族的元素
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com