
题目列表(包括答案和解析)
23.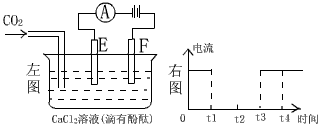 (6分)如图为持续电解含一定CaCl2水溶液的装置(以铂为电极),A为电流表。电解一段时间t1后,将CO2连续通入到电解液中。
(6分)如图为持续电解含一定CaCl2水溶液的装置(以铂为电极),A为电流表。电解一段时间t1后,将CO2连续通入到电解液中。
(1)请在右图中完成左图实验中电流对时间的变化关系图。
(2)电解时,F极的电极反应式为_____________________,
电解总反应式为______________________。
(3)电解池中产生的现象:
①________________________________ ②___________________________________________________
③____________________________________________________
22.(6分)用滴管将新制的饱和氯水慢慢滴入含酚酞的氢氧化钠稀溶液(样品 )中,当滴到最后一滴时红色突然褪去,产生该现象的原因可能有两个:
(1)是由于
(简要文字说明)
(2)是由于
(简要文字说明)
(3)简述怎样用实验证明红色褪去的原因是(1)或者是(2)。
。
21.(11分)已知X、Y、Z、W是短周期中的四种非金属元素,它们的原子序数依次增大。X元素原子形成的离子就是一个质子,Z、W在元素周期表中处于相邻的位置,它们的单质在常温下均为无色气体,Y原子的最外层电子数是内层电子数的2倍。
(1)请写出元素符号:X________;Y________;Z________;W________。
(2)X单质和Z单质在一定条件下反应生成化合物E,该反应的化学方程式为(请注明反应条件)________;E分子的空间构型为________,电子式为________;E在催化剂存在的条件下,可用于还原汽车尾气中的________,以减少对大气的污染。
(3)仅由X、Z、W三种元素组成的某种盐是一种速交肥料,但长期施用会使土壤酸化,有关的离子方程式为 。
(4)这四种元素可组成原子个数比为5∶1∶1∶3的化合物(按X、Y、Z、W的顺序),该化合物的水溶液与足量NaOH溶液反应的离子方程式为________。
(5)将9gY单质在足量W单质中燃烧,所得气体通入1L1mol/L的NaOH溶液中,完全吸收后,溶液中的离子浓度由大到小的顺序是 。
20. (4分)将1molI2(g)和2molH2置于某2L密闭容器中,在一定温度下发生反应:
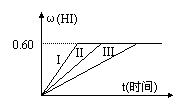
I2(g)+H2(g)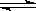 2HI(g);△H<0,并达平衡,HI的体积分数ω(HI)随时间变化如图曲线(II)所示:
2HI(g);△H<0,并达平衡,HI的体积分数ω(HI)随时间变化如图曲线(II)所示:
 ⑴达平衡时,I2(g)的物质的量浓度为 。
⑴达平衡时,I2(g)的物质的量浓度为 。
⑵若改变反应条件下,在甲条件下ω(HI)的变化如图曲线(I)所示,在乙条件下ω(HI)的变化如图曲线(III)所示。则甲条件可能是 (填入下列条件的序号。下同),乙条件可能是 ____________。
①恒容条件下,升高温度 ②恒容条件下,降低温度 ③恒温条件下,缩小反应容器体积 ④恒温条件下,扩大反应容器体积 ⑤恒温恒容条件下,加入适当催化剂
⑶若保持温度不变,在另一相同的2L密闭容器中加入a mol I2(g)、b mol H2和c mol HI(a、b、c均大于0),发生反应,达平衡时,HI的体积分数仍为0.60,则a、b、c的关系是 。
19.(12分)磷在空气中充分燃烧后生成X的分子结构如图所示。图中的圆圈表示原子,实线表示化学键。
(1)图中共有 个磷原子,请将其涂黑。写出该化合物的化学式 。
(2)X分子内磷原子排成 形,每个磷原子处于 的中心。
(3)X分子中共含P-O-P键 个。X极易与水作用,其作用过程是P-O-P键断裂过程,每断裂一个P-O-P键就可以结合 个H2O分子。
(4)1molX与4molH2O作用的化学方程式为 ;若每个X与6个H2O作用,则生成物的分子式为 。
(5)磷在不充足的氯气中燃烧的化学方程式 ,用磷酸钙制取磷酸的化学方程式 。
(6)磷在空气中燃烧生成的氧化物通常可用作强干燥剂。制备100 g这种干燥剂所消耗的空气的体积约为 L(在标准状况下)。
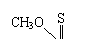
|
 (7)有机磷农药“乐果”的结构简式是: P-SCH2OCONHCH3其中所含的双键
(7)有机磷农药“乐果”的结构简式是: P-SCH2OCONHCH3其中所含的双键
有? 个。
18.目前人们正在研究开发一种高能电池-钠硫电池。它是以熔融的钠硫为两 极,以Na+导电,以β-Al2O3陶瓷作固体电解质,反应如下:2Na+xS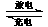 Na2Sx,以下说法正确的是
Na2Sx,以下说法正确的是
A.放电时,钠作正极,硫作负极 B.放电时,硫发生氧化反应
C.充电时,钠极与外电源的正极相连 D.充电时,阳极发生反应:Sx2―-2e-=xS
17.羟磷灰石[Ca3(PO4)2·Ca(OH)2]是牙齿表面的一层坚硬物质,它可保护牙齿,它在唾液存在如下平衡:Ca3(PO4)2·Ca(OH)2 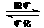 4Ca2++2PO43-+2OH-进食后,细菌和酶作用于食物产生有机酸,这时牙齿就会受到腐蚀。当使用含氟牙膏刷牙时形成氟磷石灰石
4Ca2++2PO43-+2OH-进食后,细菌和酶作用于食物产生有机酸,这时牙齿就会受到腐蚀。当使用含氟牙膏刷牙时形成氟磷石灰石
[Ca3(PO4)2·CaF2],能防止龋齿。下列说法正确的是
A.牙齿受到腐蚀的原因是有机酸可以溶解羟磷灰石,使之矿化
B.说明氟磷石灰石比羟磷灰石溶解度大
C.多食用碱性食物可以防止龋齿,有利于人体健康
D.使用含氟牙膏时,能发生如下反应:4Ca2++2PO43-+2F-
Ca3(PO4)2·CaF2
16.在容积相同的两密闭容器A和B中,保持温度为423K,同时向A、B中分别加入amol
及bmol碘化氢(a>b),待反应 2HI(g)  I2(g)+H2(g) 达到平衡后,下列说法肯定正确的是
I2(g)+H2(g) 达到平衡后,下列说法肯定正确的是
A.从反应开始到建立平衡A容器中所需的时间短
B.平衡时A、B两容器中I2蒸气的浓度相同
C.平衡时I2蒸气在混合气体中的百分含量,A容器大于B容器
D.平衡时HI的分解率aΑ小于aB
15.石墨晶体为层状结构,层内每个碳原子以三个共价单链与其它碳原子连结合组成正六边形平面网状结构,则每层碳原子个数与碳碳单链数之比为
A.1:1 B.1:3 C.2:3 D.3:2
14.在-50℃时液氨中存在着下列平衡:2NH3(l) NH+4+NH-2,两种离子的平衡浓度均为1.0×10-15mol·L-1。以下有关-50℃时液氨的叙述中正确的是
NH+4+NH-2,两种离子的平衡浓度均为1.0×10-15mol·L-1。以下有关-50℃时液氨的叙述中正确的是
A.离子积为1.0×10-15
B.向液氨中加入金属钠,平衡不移动
C.向液氨中加入氨基钠(NaNH2),液氨的离子积不变
D.向液氨中加入NH4Cl,c(NH+4)增大,离子积的数值也随之增大
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com