
题目列表(包括答案和解析)
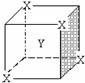
7.某离子晶体晶胞结构如右图所示,X位于立方体的顶点, Y位于立方体的中心,晶体中距离最近的两个X与一个Y形成的夹角∠XYX的角度为
A.90° B.60° C.120° D.109°28′
6.A、B为短周期元素,A原子所具有的电子层数是最外层电子数的1/2,B原子次外层电子数是最外层电子数的1/3,A与B能形成多种原子团,其中一定不存在的是
 A.AB32- B.A2B32- C.AB42- D.AB4-
A.AB32- B.A2B32- C.AB42- D.AB4-
5.已知同周期的X. Y. Z三种元素的最高价氧化物的水化物的酸性由强到弱的顺序是:
HZO4>H2YO4>H3XO4,下列判断正确的是
A.单质的氧化性按X、Y、Z的顺序减弱
B.原子半径按X、Y、Z的顺序增大
C.水溶液的PH值Na3XO4>Na2YO4>NaXO4
D.阴离子的还原性按X3-、Y2-、Z-顺序减弱
4.1999年度诺贝尔化学奖授予了开创“飞秒(10-15s)化学”新领域的科学家,使运用激光光谱技术观测化学反应时分子中原子运动成为可能。你认为该技术不能观察到的是
A.原子中原子核的内部结构 B.化学反应中原子的运动
C.化学反应中生成物分子的形成 D.化学反应中反应物分子的分解
3.HNO2的下列性质中,可以证明它是弱电解质的是
A.0.1mol·L-1HNO2溶液pH值约为2
B.用HNO2溶液作导电性实验,灯泡很暗
C.HNO2与NaCI溶液不反应
D.含0.1molHNO2和0.1molNaOH的两溶液恰好反应
2.常温下,在10mL、0.2mol/L氨水中,滴入0.2mol/L的稀盐酸,使溶液pH=7。则下列说法正确的是
A.加入盐酸的体积大于10mL B.c(NH4+)=c(Cl-)
C.加入盐酸的体积等于10mL D.c(NH4+)<c(Cl-)
1.下列变化过程中,无化学键断裂或生成的是
A.石墨转化为金刚石 B.NaCl晶体溶于水
C.干冰升华 D.HCl溶于水
5.00mL,再吸入水若干,当B注射器内气体恰好全部溶入水中时,形成的氯水约为
多少体积(20℃时,氯气的溶解度0.7293g/100g水,假设该氯水的密度为1g/cm3)?
(2)漂粉精是NaClO和NaCl的混合物,其物质的量之比为1∶1,在制漂粉精时,难免有极少量的烧碱多余,你能否计算出这种漂粉精中除NaClO和NaCl之外的杂质含
量
 为多少?
为多少?
(3)将二滴氯水蓝色石蕊试纸上,试纸的颜色有什么变化?反映了氯水具有什么性质?
(4)将该氯水放置一段时间,B注射器内会出现气体,且将注射器剧烈振荡也不能使气体消失,相反地,气体数量还略有增加,这是为什么?
(5)若将该氯水长时期放置你估计B注射器内出现气体的体积约是多少?你可用怎样的化学方法确定这种气体是什么?具体的操作步骤怎样?
(6)你还可以利用A注射器内的氯气做哪些氯气性质的试验?当实验结束时,A注射器内多余的氯气应如何处理?
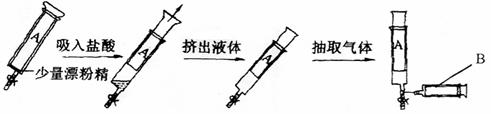
25.(9分)现取用一个容量为200mL的大注射器(A),在注射器的套筒内预先盛放0.2414g漂粉精,然后吸入足量的盐酸,反应充分后,将注射器内的液体小心地推出,这时注射器内的黄绿色的气体折合为标准状况下的体积是40.32mL。
(1)然后用B注射器在A注射器的橡皮管上抽取折合为标准状况下的黄绿色气体
24.(6分)在390℃、3×106Pa下,以CO和H2为原料合成甲醇,其反应式为:CO+2H2
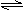 CH3OH(g),当原料气中H2和CO比例不同时,对CO的转化率及平衡混合物中甲醇的质量分数都有影响。
CH3OH(g),当原料气中H2和CO比例不同时,对CO的转化率及平衡混合物中甲醇的质量分数都有影响。
(1)以m表示H2和CO的物质的量之比(即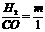 ),a 为CO的转化率,Y为平衡混合物中CH3OH的体积百分含量,试导出与m,a的关系式:
;
),a 为CO的转化率,Y为平衡混合物中CH3OH的体积百分含量,试导出与m,a的关系式:
;
(2)下表列出m=1,2,3,4时的一部分实验数据,试计算出空格中转化率a和平衡时CH3OH的含量Y?
|
m |
1 |
2 |
3 |
4 |
|
a |
25% |
45% |
③ |
④ |
|
x |
① |
② |
19.35% |
16.35% |
① ② ③ ④
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com