
题目列表(包括答案和解析)
18.在容积相同的甲、乙两个密闭容器中均分别加入2molSO2和1mol O2,同时发生下列反应:2SO2(g)+O2(g)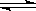 2SO3(g),在相同温度下达到平衡。若甲容器保持体积不变,乙容器保持压强不变,测得甲容器中SO2的转化率为25%,则下列说法中正确的是
2SO3(g),在相同温度下达到平衡。若甲容器保持体积不变,乙容器保持压强不变,测得甲容器中SO2的转化率为25%,则下列说法中正确的是
A.反应过程中的某时刻,甲容器中的反应速率比乙中的大
B.达到平衡时,甲容器反应所需时间比乙容器少
C.乙容器中SO2的转化率大于25%
D.平衡时,乙容器中SO2,O2,SO3的浓度之比一定为2:1:2
17.某温度下,反应N2O4(g)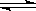 2NO2(g)-Q在密闭容器达到平衡,平衡时改变外界条件,使反应再次平衡,新平衡时,c(NO2)/c(N2O4)与原平衡相比变小了,则改变的条件可能是
2NO2(g)-Q在密闭容器达到平衡,平衡时改变外界条件,使反应再次平衡,新平衡时,c(NO2)/c(N2O4)与原平衡相比变小了,则改变的条件可能是
①保持容器容积和温度不变,向容器内补充了NO2 ②保持容器容积和温度不变,向容器内补充了N2O4 ③保持温度压强不变,向容器内补充了N2 ④保持容器的容积不变,升高了温度
A.只有② B.只有③ C.①② D.①②③
16.等体积等物质的量浓度的强碱MOH溶液和弱酸H2A溶液混合后,混合液中有关离子的浓度关系不正确的是
A.c(M+) +c(H+) = c(HA-)+2c(A2-)+c(OH-) B.c(M+) =c(HA-) + c(A2-) + c(H2A)
C.c(H2A) + c(H+) =c(A2-) +c(OH-) D.c(M+) >c(A2-) >c(HA-) >c(H+) >c(OH-)
15.R为短周期元素,其原子所具有的电子层数为最外层电子数的1/2。它可能形成的含氧酸根离子有:①R2O42-、②RO42-、③R2O32-、④RO32-。则下列判断正确的是
A.当它形成①时,不可能形成④ B.当它形成②时,不可能形成③、④
C.当它形成①时,不可能形成②、③ D.当它形成②时,可以形成①
14.把6 mol气体A和5 mol气体B混合后充入4 L密闭容器中在一定条件下反应:3A
(g) + B (g) 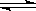 x C (g) + 2 D (g),在5 min时达到平衡,此时生成2 mol D,并测得C的平均速率为0.1 mol /(L•min),则下列结论错误的是
x C (g) + 2 D (g),在5 min时达到平衡,此时生成2 mol D,并测得C的平均速率为0.1 mol /(L•min),则下列结论错误的是
A.x的值为1 B.B的平衡浓度为1.0 mol /L
C.B的转化率为20% D.A的平均速度为0.15 mol / (L•min)
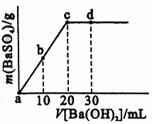
13.常温下,向0.1mol·L-1的硫酸溶液中逐滴加入物
质的量浓度相同的氢氧化钡溶液,生成沉淀的量与
加入氢氧化钡溶液的体积关系如图所示。a、b、c、
d分别表示实验时不同阶段的溶液,下列有关说法中
不正确的是
A.c、d溶液呈碱性 B.溶液的导电能力:a>b>d>c
C.a、b溶液呈酸性 D.溶液的pH:a<b<c<d
12.恒温下,将两个铂电极插入一定量的Na2SO4饱和溶液里进行电解,经过一段时间后,在两极共产生 气体,同时从溶液中析出m g Na2SO4·10H2O晶体,则原Na2SO4
气体,同时从溶液中析出m g Na2SO4·10H2O晶体,则原Na2SO4
饱和溶液的质量分数为
 A.71m/161(m+18n) B.71m/161(m+12n)
A.71m/161(m+18n) B.71m/161(m+12n)
C.71/161(m+36n) D.m/161(m+12n)
11.X、Y为短周期元素,X原子各电子层的电子数之比为1 :4 :1,它比Y原子多3个电子,下列叙述正确的是
A.X离子半径大于Y离子半径 B.X、Y两元素位于同一周期
C.X单质在空气中燃烧可生成两种化合物 D.X、Y形成的化合物是共价化合物
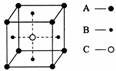
10.某物质的晶体中含有A、B、C三种元素,其排列方式如图所示(其中前后两面面心中的B元素的原子未能画出)。晶体中A、B、C的原子个数比为
A.1∶3∶1 B.2∶3∶1 C.2∶2∶1 D.1∶3∶3
9.下列离子方程式中正确的是
A.氨水中加入明矾溶液:3OH-+Al3+===Al(OH)3↓
B.硫酸铜溶液中加入氢氧化钡溶液:SO42-+Ba2+===BaSO4↓
C.碳酸氢铵溶液中加入足量的氢氧化钠溶液:
NH4++HCO3-+2OH-===NH3·H2O+CO32-+H2O
D.向漂白粉溶液中通入SO2气体:
 Ca2++2ClO-+SO2+H2O===CaSO3↓+2HClO
Ca2++2ClO-+SO2+H2O===CaSO3↓+2HClO
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com