
题目列表(包括答案和解析)
4.血液中有一种含铜呈蓝色的蛋白质分子,其相对分子质量约为151000,已知该分子中铜的质量分数为0.34%,则平均每个含铜蛋白质分子中的铜原子数为( )
A.8 B.6
C.4 D.2
3.在一定条件下,将X和Y两种物质按不同的比例放入密闭容器中反应,平衡后测得X,Y的转化率与起始时两物质的物质的量之比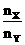 的关系如图所示,则X,Y的反应方程式可表示为( )
的关系如图所示,则X,Y的反应方程式可表示为( )
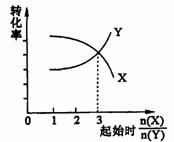
A.2X+Y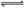 3Z B.3X+2Y
3Z B.3X+2Y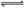 2Z
2Z
C.X+3Y Z D.3X+Y
Z D.3X+Y Z
Z
A.使用燃油机 B.绿化城市
C.出门戴口罩 D.开发使用太阳能
2.钋( )原子核内的中子数与核外电子数之差是( )
)原子核内的中子数与核外电子数之差是( )
A.40 B.168
C.126 D.42
22.燃料电池是一种新型的无污染、无噪音、高效率的发电设备,是一种很有发展潜力的新能源,它主要由燃料、氧化剂、电极和电解质组成,燃料电池的结构和传统电池一样具有正负电极,正负电极被电解质分隔,它以还原剂(用氢作燃料)为负极反应物,以氧化剂(如空气中的氧气等)为正极交换物,在燃料电池中,氢气等燃料在通常条件下就能在电极上进行电极反应(一般用多孔镍、铂等作电极材料).电池中的电解质为有机高分子高聚物,它可以交换质子.
(1)燃料电池的电极在常温条件下就能持续发生电极反应,写出氢氧燃料电池中的电极反应式:负极______________;正极______________.
(2)氢氧燃料电池可作为载人航天器的首选电池,一个重要原因是它在产生持续电流的过程中生成的产物是水,这正好解决航天员的饮水问题,航天员饮用这些合成水通过消化系统,大部分在被___________吸收.
21.(8分)2001年诺贝尔化学奖被美国的诺尔斯、沙普雷斯和日本的野依良治获得,以表彰他们发现某些被称为手征性的分子可以用来加速并控制化学反应的创造性工作.在有机物分子中,若某碳原子连接四个不同的原子或基团,则这种碳原子称为“手征性碳原子”.例如: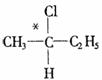 中*C就是“手征性碳原子”.含“手征性碳原子”的物质通常具有不同的光学特征(称为光学活性).
中*C就是“手征性碳原子”.含“手征性碳原子”的物质通常具有不同的光学特征(称为光学活性).
(1)据报道最新合成的有机物A为: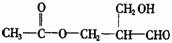 具有光学活性,若要使A失去光学活性,可采用的方法有(最少列举三种方法):
具有光学活性,若要使A失去光学活性,可采用的方法有(最少列举三种方法):
(2)某链烃B的分子式为 ,在B的各种结构(不考虑
,在B的各种结构(不考虑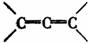 结构)中,含有“手征性碳原子”,且与足量
结构)中,含有“手征性碳原子”,且与足量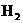 加成反应后仍具有光学活性的有机物有五种,已知其中三种的结构简式为:
加成反应后仍具有光学活性的有机物有五种,已知其中三种的结构简式为:
① 
② 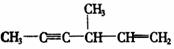
③ 
则另两种的结构简式为:
④______________________________________,
⑤______________________________________.
20.(8分)现有化合物甲: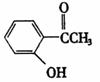 乙:
乙:
丙: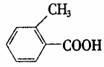
(1)请写出丙中含氧官能团的名称:________,________.
(2)请判别上述哪些化合物互为同分异构体:
(3)请分别写出鉴别甲、乙、丙化合物的方法(指明所选试剂及主要现象即可).
(4)请按酸性由强到弱排列甲、乙、丙的顺序:________、________、________.
19.(8分)利用示踪原子可以研究化学反应.比如乙酸乙酯与水反应,生成醋酸和乙醇,反应方程式为:
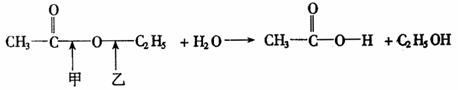
乙酸乙酯 水 醋酸 乙醇
那么,水解过程是从甲处断开还是从乙处断开呢?试分析说明如何通过示踪原子的方法来确定化学反应的过程.
18.(10分)在冶金工业中,常用焦炭来冶炼铁,其原理是(用化学方程式表示):______________________________.实验室中可用CO还原CuO和 ,在加热CuO或
,在加热CuO或 前应________,直到无________现象时才能点燃酒精灯加热,否则可能发生________现象,未反应完全的CO________(填“能”、“不能”)排放到大气中,应________,处理.
前应________,直到无________现象时才能点燃酒精灯加热,否则可能发生________现象,未反应完全的CO________(填“能”、“不能”)排放到大气中,应________,处理.
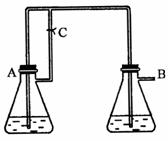
17、(10分) 由于在空气中易被氧化,制取时很难观察到白色沉淀现象,只能看到灰绿色,采用图装置使用
由于在空气中易被氧化,制取时很难观察到白色沉淀现象,只能看到灰绿色,采用图装置使用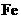 ,
,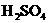 (稀),NaOH溶液可在还原性气氛中制取
(稀),NaOH溶液可在还原性气氛中制取 白色沉淀,且较长时间内不变色,其中C为弹簧夹,则锥形瓶A中应加入的药品为________,锥形瓶B中应加入的药品为________.容器A中的反应开始后,请设计后续操作步骤完成的制备,并说明每步操作理由和现象.
白色沉淀,且较长时间内不变色,其中C为弹簧夹,则锥形瓶A中应加入的药品为________,锥形瓶B中应加入的药品为________.容器A中的反应开始后,请设计后续操作步骤完成的制备,并说明每步操作理由和现象.
16.根据中学化学教材所附元素周期表判断,下列叙述不正确的是( )
A.K层电子为奇数的所有元素所在族的序数与该元素原子的K层电子数相等
B.L层电子为奇数的所有元素所在族的序数与该元素原子的L层电子数相等
C.L层电子为偶数的所有主族元素所在族的序数与该元素原子的L层电子数相等
D.M层电子为奇数的所有主族元素所在族的序数与该元素原子的M层电子数相等
第Ⅱ卷(非选择题,共56分)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com