
题目列表(包括答案和解析)
21.(12分)有A、B、C、D、E、F六种短周期的主族元素、原子序数依次增大,其中A、
D元素的原子最外电子层均只有一个电子,且A和D可形成离子化合物;C、F同主族,
B元素位于元素周期表中第二周期,且原子最外层电子数占核外电子总数的3/4,F元
素原子最外电子层比同周期的E元素原子的最外电子层多4个电子,请回答:
(1)写出AD元素组成化合物的电子式_________ _______
(2)写出BDE元素组成化合物的名称___________ _______
(3)工业生产E的方法是___ ____________
(4)D、F两元素最高价氧化物的水化物之间发生反应的化学方程式______________
(5)D的氢氧化物和C的氢化物在水溶液中反应的离子方程式为________________
(6)若以上(4)、(5)两个反应物间恰好完全反应,且得到等体积,等物质的量浓度的
溶液,则(4)、(5)反应所得溶液中的离子个数是(4)_____________(5)(空格内选填“大
于”,“小于” 或“等于”)
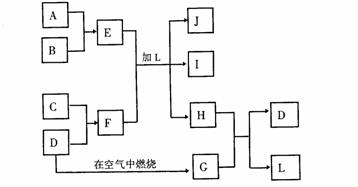 22.(8分)图中方框中的字母表示一种反应物或生成物
22.(8分)图中方框中的字母表示一种反应物或生成物
产物J是含A金属元素的胶状白色沉淀,I为NaCl溶液,D是淡黄色固体单质。试填写下列空白:
(1)L的化学式为________________ ___
(2)F的化学式为______________ ______
(3)写出J受热分解反应的化学方程式__________ __________________
(4)H和G之间反应的化学方程式为______________ _______________。
20.(10分)实验室可以用下图所示仪器连接起来制备纯净的二氧化碳并测定其式量。
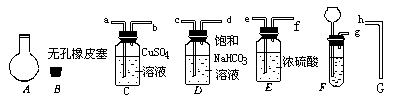
现用含有少量硫化亚铁的大理石和盐酸反应制备二氧化碳气体,实验步骤如下:
(1)将橡皮塞B塞在A烧瓶口,并用橡皮筋套在烧瓶的瓶颈处以标记橡皮塞所塞入瓶颈
的深度,准确称其质量为m1g。
(2)连接制备和净化气体的装置,其连接顺序是:
_ _接 __,_ _接_ _,_ _接_ _,_ _接_ _。
(3)将导管G插入烧瓶A中用向___ _(填“上”或“下” )排空气法收集
二氧化碳气体;检验二氧化碳气体已经充满烧瓶的方法是___ _ __。若经
检验,二氧化碳气体已经充满烧瓶,迅速用橡皮塞塞好烧瓶瓶口,并称其质量为m2g。
(4)将烧瓶口橡皮塞取下,向烧瓶内注水至标记线,再将水小心地倒入量筒测量出水的
体积为V1 mL;将该体积换算成标准状况时的体积为V2 mL。
请写出二氧化碳式量的计算式__ _____。
若不将气体净化和干燥,所测定的二氧化碳式量的数值将会____ _(填“偏高”或
“偏低” ),其理由是:___ ________________________
_ ________________________________________________________________________。
19.(9分)下图为常用玻璃仪器组成的七种实验装置,根据需要可在其中加入适量液体或固
体试剂。请选择适宜装置的序号填于空白处(多选、漏选或错选均扣分)
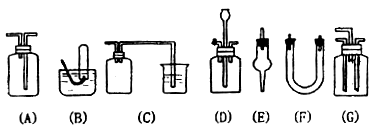
(1)既能用于收集Cl2又能用于收集NO的装置是________________________________。
(2)能用作干燥CO2气流的装置是________________________________________。
(3)能用于实验室制取Cl2并检验Cl2性质的连续实验中,除去Cl2中的HCl杂质的最佳
装置是________________________。
(4)合成NH3,可用于干燥、混合H2和N2的装置是________________________。
(5)接在气体的连续实验中间,用于达到控制气流使其平稳目的的装置是__________。
(6)用于尾气吸收并能防止液体倒吸到其它装置中的是________________________。
18.某学生想制作一种家用环保型消毒液发生器,用石墨作电极电解饱和氯化钠溶液,通电
时,为使Cl2被完全吸收,制得有较强杀菌能力的消毒液,设计了如图的装置,则对电
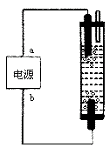 源电极名称和消毒液的主要成分判断正确的是
( )
源电极名称和消毒液的主要成分判断正确的是
( )
A.a为正极,b为负极;NaClO和NaCl
B.a为负极,b为正极;NaClO和NaCl
C.a为阳极,b为阴极;HClO和NaCl
D.a为阴极,b为阳极;HClO和NaCl
第Ⅱ卷(非选择题 共78分)
17.对尼古丁和苯并[a]芘的分子组成与结构描述正确的 是 ( )
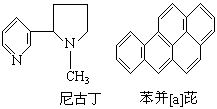 A.尼古丁为芳香族化合物
A.尼古丁为芳香族化合物
B.苯并[a]芘的分子式为C20H18
C.苯并[a]芘分子中含有苯环结构单元, 是苯的
同系物
D.尼古丁分子中的所有碳原子可能不在同一平
面上, 苯并[a]芘分子中的所有氢原子可能都在同一平面上
16.下列说法正确的是 ( )
A.需要加热才能发生的反应一定是吸热反应
B.任何放热反应在常温条件下一定能发生反应
C.反应物和生成物所具有的总能量决定了放热还是吸热
D.吸热反应在一定条件下(如常温、加热等)也能发生反应
15.氧只有35C1和37C1两种稳定同位素,它们在氯气中的原子数之比35C1:37C1为3:1,
则分子量为70、72、74的氯气分子数之比可能是 ( )
A.5:2:1 B.5:2:2 C.9:3:1 D.9:3:2
14.硫酸铵在强热的条件下分解,生成NH3,SO2,N2和H2O,该反应中的氧化产物和还原
产物的物质的量之比为 ( )
A.1:3 B.2:3 C.4:3 D.1:1
13.有关材料分类正确的是 ( )
A.硅酸盐材料属于新型无机非金属材料
B.高温结构陶瓷属于新型无机非金属材料,金属属于金属材料,但都属于结构材料
C.新型无机非金属材料包括半导体材料、光导纤维、氧化铝陶瓷等
D.氮化硅陶瓷属于新型无机非金属材料,但不是高温结构材料
12.将颜色相近的NO2和Br2(气)分别装入注射器中,将活塞同时向外拉,使气体体积扩大
1倍后,下列叙述错误的是 ( )
A.NO2的颜色比Br2(气)颜色深 B.两种气体颜色均比原来浅
C.Br2(气)的压强比NO2变化小 D.Br2(气)的压强比NO2变化大
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com